

2023-2024学年山东省东营市广饶县李鹊中学八年级(上)月考化学试卷(12月份)
展开
这是一份2023-2024学年山东省东营市广饶县李鹊中学八年级(上)月考化学试卷(12月份),共24页。试卷主要包含了选择题,填空题,计算题等内容,欢迎下载使用。
1.(2分)原子失去最外层电子或最外层得到电子后,一定不会引起改变的是( )
①原子种类②化学性质③粒子的电性④原子核⑤电子层数⑥最外层电子数⑦核外电子总数
A.②④⑤B.③④⑦C.①④D.①③⑤⑥
2.(2分)某元素的阳离子A3+的核外有23个电子,核内有30个中子,则该元素原子的核电荷数和相对原子质量分别为( )
A.23,53B.26,30C.26,56D.23,46
3.(2分)下列化学用语中,既能表示一种物质,还能表示一种元素的是( )
A.NaB.HC.Cl2D.2N
4.(2分)2021年赛过黄金价格的贵金属铑的人民币标价是黄金价格的10倍、铂金的19倍。铑被使用在汽车催化转化器的多孔陶瓷结构中,用来帮助氮氧化物分解成无害的氧气和氮气。根据如图下列有关铑的说法正确的是( )
A.铑的元素符号是RH
B.铑是第六周期元素
C.铑的相对原子质量是102.9
D.铑在化学反应中易得电子
5.(2分)某原子得到两个电子后的结构示意图为,则x的值是( )
A.14B.16C.18D.20
6.(2分)化学学习要建构若干基本观念,以下四类化学基本观念中认识正确的是( )
A.变化观:同种元素的原子和离子在一定条件下是可以相互转化的
B.能量观:化学变化中一定伴随能量变化,而物理变化中不伴随能量变化
C.元素观:水和过氧化氢组成元素不同
D.微粒观:一个二氧化硫分子由一个硫原子和一个氧分子构成
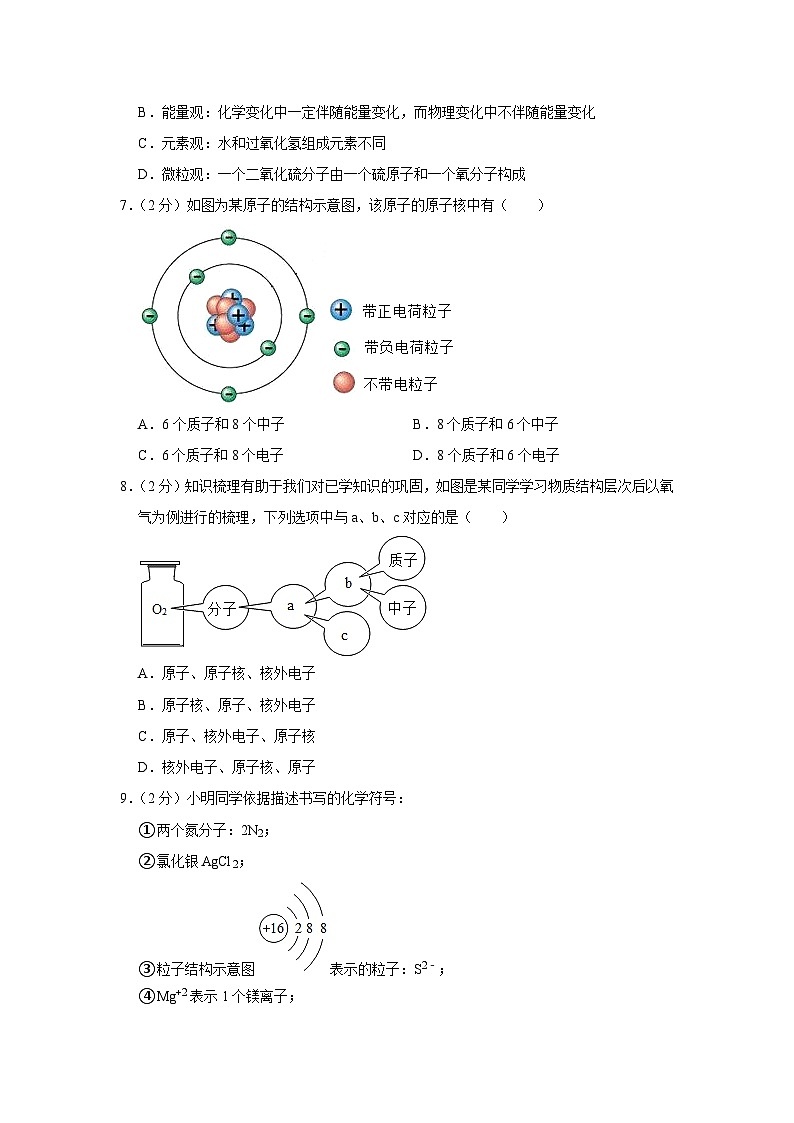
7.(2分)如图为某原子的结构示意图,该原子的原子核中有( )
A.6个质子和8个中子B.8个质子和6个中子
C.6个质子和8个电子D.8个质子和6个电子
8.(2分)知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c对应的是( )
A.原子、原子核、核外电子
B.原子核、原子、核外电子
C.原子、核外电子、原子核
D.核外电子、原子核、原子
9.(2分)小明同学依据描述书写的化学符号:
①两个氮分子:2N2;
②氯化银AgCl2;
③粒子结构示意图表示的粒子:S2﹣;
④Mg+2表示1个镁离子;
⑤铝元素AL;
⑥H2O、OH﹣两种粒子中所含的电子数相等。
其中正确说法的有( )
A.③④⑤B.①④⑤C.①③⑤D.①③⑥
10.(2分)下列四种粒子的结构示意图中,说法正确的是( )
A.②表示的元素在化合物中通常显+2价
B.它们表示四种不同的元素
C.①③④表示的元素都是非金属元素
D.①④表示的是阳离子
11.(2分)已知一个碳12原子的质量为ag,某原子的质量为bg,该原子的相对原子质量为( )
A.B.C.D.
12.(2分)推理是化学学习的一种方法,以下推理正确的是( )
A.单质中只含有一种元素,因此只含有一种元素的物质一定是单质
B.同种元素的原子具有相同的质子数,所以具有相同质子数的原子属于同种元素
C.在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定显负价
D.稀有气体元素的原子最外层电子数为8(氦除外),因此微粒一定是稀有气体元素的原子
13.(2分)连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(分子式为C7H6O5)。关于它的说法正确的是( )
A.一个没食子酸分子由7个碳原子、6个氢原子和5个氧原子构成
B.没食子酸中碳、氢、氧三种元素的质量比为7:6:5
C.没食子酸中质量分数最多的元素是氧元素
D.没食子酸的相对分子质量是170g
14.(2分)对于下列化学用语,有关说法正确的是( )
①NO
②Fe2+
③K2MnO4
④
⑤
A.①表示的是两种元素组成的混合物
B.③中锰元素的化合价为+6
C.②和⑤均表示阳离子
D.④和⑤表示的微粒化学性质相同
15.(2分)如图是表示气体分子的示意图,图中“●”和“〇”分别表示两种不同原子,其中可能表示化合物的是( )
A.B.
C.D.
16.(2分)下列关于Mg、Mg2+两种粒子的判断中不正确的是( )
A.核电荷数相同B.质量几乎相等
C.Mg2+比Mg稳定D.电子层数相同
17.(2分)某纯净物中只含有R和氧两种元素,且R元素与氧元素的质量比为7:16,R的相对原子质量为14( )
A.+1B.+2C.+3D.+4
18.(2分)下列化学用语中,数字“2”的说法正确的是( )
①2H ②2NH3③SO2④O ⑤Mg2+⑥2OH﹣⑦H2O。
A.表示离子个数的是⑤⑥
B.表示离子所带电荷数的是④⑤
C.表示分子中原子个数的是③⑦
D.表示分子个数的是①②
19.(2分)某无人机的动力来源于锂电池,锂电池放电时生成亚锰酸锂( LiMnO2),其中锂元素显+1价,则锰元素的化合价是( )
A.﹣3B.+2C.+3D.+4
20.(2分)磁悬浮的核心技术是利用超导体的反磁性。高温超导物质(Y2Ba4Cu6O13)是以YmOn、BaO和CuO为原料,经研磨烧结而成,此过程中所有元素的化合价均不变。YmOn的化学式为( )
A.Y2O3B.YO3C.Y2O5D.YO
二、填空题(共3个小题,每空2分,共50分)
21.(20分)用化学符号表示:
(1)铜元素 ;
(2)两个氧分子 ;
(3)3个硫酸根离子 ;
(4)由Ca2+和构成的碳酸钙 ;
(5)保持二氧化碳化学性质的粒子 ;
(6)氧化镁中镁元素的化合价为正二价 ;
(7)地壳中含量最多的元素与含量最多的金属元素形成的物质是 ;
(8)氖气 ;
(9)NH3中氮元素的化合价 ;
(10)核电荷数分别为8、13的两种元素所形成的化合物 。
22.(10分)化学与生活密切相关。
①新鲜的苹果切开后因亚铁离子被氧化会很快变黄,亚铁离子的符号 。
②食品袋中的干燥剂为生石灰,主要成分是氧化钙,氧化钙的化学式为 。氧元素的质量分数是 。(精确到0.1%)
③全脂高钙奶粉中的“钙”是指 (填“分子”或“原子”或“元素”)。
④某食盐中“碘”主要以碘酸钾(KIO3)的形式加入,其中碘元素的化合价为 价。
23.(20分)在“宏观—微观—符号”之间建立联系,是化学学科独有的思维方式。
(1)根据下列粒子结构示意图1,回答问题。
①A、B、C、D所示粒子共表示 种元素(填数字)。
②D所示粒子在化学反应中容易 电子(填“得到”或“失去”)。
③若E中X=10时,则该粒子属于 (填“原子”或“离子”)。
④若B、E两种粒子属于同种元素,则X= ,请写出E的化学符号 。
⑤BD形成化合物的化学式 。
(2)原子序数为1~18的元素的原子结构示意图等信息如图2,回答问题。
①原子序数为14的元素位于元素周期表中第 周期,同一周期 数相等。
②根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子 相同,所以氟元素与氯元素的化学性质相似。
③同周期元素(从第二周期开始),从左到右,各元素原子随原子序数的增加 。
三、计算题(本题有1个小题,每空2分,共10分)
24.(10分)我国科学家屠呦呦因为发现青蒿素(化学式为C15H22O5),一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获2015年诺贝尔生理学或医学奖.
(1)青蒿素的相对分子质量为 ;
(2)青蒿素中各原子的原子个数比C:H:O= ;
(3)青蒿素中碳、氢两种元素的质量比为 ;
(4)青蒿素中氧元素的质量分数为 (计算结果保留一位小数);
(5)在1972年发现青蒿素前治疗疟疾的药物主要是金鸡纳霜,又叫奎宁(化学式为C20H24N2O2,相对分子质量为324),求141g青蒿素中所含氧元素的质量与多少克金鸡纳霜中所含氧元素质量相等?(写出计算过程)
2023-2024学年山东省东营市广饶县李鹊中学八年级(上)月考化学试卷(12月份)
参考答案与试题解析
一、选择题(每小题2分,共40分,每小题只有一个正确答案。)
1.(2分)原子失去最外层电子或最外层得到电子后,一定不会引起改变的是( )
①原子种类②化学性质③粒子的电性④原子核⑤电子层数⑥最外层电子数⑦核外电子总数
A.②④⑤B.③④⑦C.①④D.①③⑤⑥
【分析】根据原子得失电子后的变化进行分析解答即可。
【解答】解:原子失去最外层电子或最外层得到电子后,原子的种类;
故选:C。
【点评】本题考查的是原子和离子的转化的知识,完成此题,可以依据已有的知识进行。
2.(2分)某元素的阳离子A3+的核外有23个电子,核内有30个中子,则该元素原子的核电荷数和相对原子质量分别为( )
A.23,53B.26,30C.26,56D.23,46
【分析】阳离子是原子失去电子之后形成的,由阳离子的核外电子数推出原子核内质子数,根据相对原子质量=质子数+中子数求出相对原子质量.
【解答】解:阳离子A3+的核外有23个电子,所以A原子内有26个质子,相对原子质量为26+30=56,所以原子的核电荷数为26。
【点评】了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的.
3.(2分)下列化学用语中,既能表示一种物质,还能表示一种元素的是( )
A.NaB.HC.Cl2D.2N
【分析】根据化学式与元素符号的含义进行分析解答,金属、大多数固体非金属等都是由原子直接构成的,故它们的元素符号,既能表示一种元素,还能表示一种物质.
【解答】解:元素符号能表示一种元素,还能表示该元素的一个原子,当元素符号又是化学式时。
A、Na属于金属元素,还能表示钠这一纯净物。
B、H属于气态非金属元素,但不能表示一种物质。
C、该符号是氯气的化学式,故选项不符合题意。
D、该符号可表示2个氮原子,故选项不符合题意。
故选:A。
【点评】本题难度不大,掌握由原子构成的物质的化学式一般有三层含义(宏观:表示一种元素、一种单质,微观:表示一个原子)是正确解答此类题的关键.
4.(2分)2021年赛过黄金价格的贵金属铑的人民币标价是黄金价格的10倍、铂金的19倍。铑被使用在汽车催化转化器的多孔陶瓷结构中,用来帮助氮氧化物分解成无害的氧气和氮气。根据如图下列有关铑的说法正确的是( )
A.铑的元素符号是RH
B.铑是第六周期元素
C.铑的相对原子质量是102.9
D.铑在化学反应中易得电子
【分析】原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≤4,在化学反应中失去电子,若最外层电子数≥4,在化学反应中得到去电子。根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可。
【解答】解:A、元素符号书写时,则铑的元素符号是Rh;
B、由原子结构示意图可知,因此铑是第五周期元素;
C、根据元素周期表中的一格可知,该元素的相对原子质量为102.9,通常省略不写;
D、由原子结构示意图可知,在化学反应中易失去电子。
故选:C。
【点评】本题难度不大,灵活运用原子结构示意图的含义、元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)是正确解答本题的关键。
5.(2分)某原子得到两个电子后的结构示意图为,则x的值是( )
A.14B.16C.18D.20
【分析】依据原子中质子数等于核外电子数,原子得到两个电子后电子数比质子数多2分析解答即可;
【解答】解:由于该图示是某原子得到两个电子后情况,所以该元素的原子核外电子数为16,所以其核内质子数x为16;
故选:B。
【点评】此题是对原子结构示意图的考查,了解原子结构示意图的意义,掌握离子结构示意图与原子结构示意图的联系与区别是解题的关键所在。
6.(2分)化学学习要建构若干基本观念,以下四类化学基本观念中认识正确的是( )
A.变化观:同种元素的原子和离子在一定条件下是可以相互转化的
B.能量观:化学变化中一定伴随能量变化,而物理变化中不伴随能量变化
C.元素观:水和过氧化氢组成元素不同
D.微粒观:一个二氧化硫分子由一个硫原子和一个氧分子构成
【分析】A、根据原子得失电子变为离子,离子得失电子变为原子进行分析;
B、根据物理变化也伴随能量的变化进行分析;
C、根据水和过氧化氢都是由氧元素和氢元素组成的,组成元素相同进行分析;
D、根据分子是由原子构成的进行分析。
【解答】解:A、原子得失电子变为离子,同种元素的原子和离子在一定条件下是可以相互转化的;
B、物理变化也伴随能量的变化,需要吸热,故B不正确;
C、水和过氧化氢都是由氧元素和氢元素组成的,故C不正确;
D、分子是由原子构成的2分子由一个硫原子和两个氧原子构成,故D不正确。
故选:A。
【点评】解答本题关键是熟悉物质的元素组成,分子、原子、离子的联系。
7.(2分)如图为某原子的结构示意图,该原子的原子核中有( )
A.6个质子和8个中子B.8个质子和6个中子
C.6个质子和8个电子D.8个质子和6个电子
【分析】在原子中,质子数=核外电子数,原子核是由带正电的质子和不带电的中子构成的。
【解答】解:因为原子中,6个质子数=核外电子数,其原子核外有6个电子,原子核是由质子和中子构成的,
故选:A。
【点评】本题考查了原子核的构成,明确原子核是由质子和中子构成的,在原子中,质子数=核外电子数是解题的关键。
8.(2分)知识梳理有助于我们对已学知识的巩固,如图是某同学学习物质结构层次后以氧气为例进行的梳理,下列选项中与a、b、c对应的是( )
A.原子、原子核、核外电子
B.原子核、原子、核外电子
C.原子、核外电子、原子核
D.核外电子、原子核、原子
【分析】根据分子、原子的构成分析,分子是由原子构成的,原子是由原子核和电子构成,原子核是由质子和中子构成的。
【解答】解:由示意图可知,质子和中子构成了b,原子核和电子构成了原子,原子构成了分子,故A正确,B、C。
故选:A。
【点评】本题主要考查了分子、原子的构成,属于基础的知识,难度不大。
9.(2分)小明同学依据描述书写的化学符号:
①两个氮分子:2N2;
②氯化银AgCl2;
③粒子结构示意图表示的粒子:S2﹣;
④Mg+2表示1个镁离子;
⑤铝元素AL;
⑥H2O、OH﹣两种粒子中所含的电子数相等。
其中正确说法的有( )
A.③④⑤B.①④⑤C.①③⑤D.①③⑥
【分析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目。
【解答】解:①分子的表示方法:正确书写物质的化学式,表示多个该分子,所以两个氮分子可表示为2N2,正确;
②氯化银中,银元素显+4价,所以氯化银的化学式为AgCl;
③粒子结构示意图 的质子数为16,核外有18个电子,即S2﹣,正确;
④由离子的表示方法,在表示该离子的元素符号右上角,数字在前,带1个电荷时。所以一个镁离子表示为Mg2+,错误;
⑤元素符号书写时要遵循“一大二小”的原则,铝的元素符号为Al;
⑥每个水分子是由两个氢原子和一个氧原子构成的,含有10个电子,正确。
故选:D。
【点评】本题难度不大,掌握常见化学用语(原子符号、分子符号、化合价、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键。
10.(2分)下列四种粒子的结构示意图中,说法正确的是( )
A.②表示的元素在化合物中通常显+2价
B.它们表示四种不同的元素
C.①③④表示的元素都是非金属元素
D.①④表示的是阳离子
【分析】根据元素的定义及原子和离子的核内质子数与核外电子数的关系分析。 当核电荷数=质子数=核外电子数,为原子;当核电荷数=质子数>核外电子数,为阳离子;当核电荷数=质子数<核外电子数,为阴离子;相对稳定结构是指最外层电子数为8,只有一个电子层时为2的结构。
【解答】解:A、②最外层有两个电子,表示的元素在化合物中通常显+2价;
B、核内质子数是8、11,错误;
C、③④表示的元素都是金属元素;
D、①表示的是阴离子;
故选:A。
【点评】本题考查了原子结构示意图的有关知识,完成此题,可以依据已有的知识进行。
11.(2分)已知一个碳12原子的质量为ag,某原子的质量为bg,该原子的相对原子质量为( )
A.B.C.D.
【分析】根据相对原子质量的定义可以知道:相对原子质量是指以一种碳原子质量的 为标准,其他原子的质量跟它相比较所得到的比,用公式表示为:某原子的相对原子质量=,将数据代入公式计算即可.
【解答】解:根据公式:某原子的相对原子质量=某原子的相对原子质量=,
可以知道该原子的相对原子质量==
分析四个选项可以知道:选项C是正确的。
故选:C。
【点评】解答有关相对原子质量的计算题时,要注意相对原子质量是一个原子的实际质量和碳原子质量的 之比,掌握此知识点就能轻松解题.
12.(2分)推理是化学学习的一种方法,以下推理正确的是( )
A.单质中只含有一种元素,因此只含有一种元素的物质一定是单质
B.同种元素的原子具有相同的质子数,所以具有相同质子数的原子属于同种元素
C.在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定显负价
D.稀有气体元素的原子最外层电子数为8(氦除外),因此微粒一定是稀有气体元素的原子
【分析】A、根据单质是由同种元素组成的纯净物,进行分析判断。
B、根据元素是质子数(即核电荷数)相同的一类原子的总称,进行分析判断。
C、根据化合价的原则,进行分析判断。
D、根据最外层电子数为8的微粒,进行分析判断。
【解答】解:A、单质中只含有一种元素,如氧气和臭氧的混合物。
B、同种元素的原子具有相同的质子数,故选项推理正确。
碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的pH一定大于7;
C、在同一化合物中金属元素显正价,如硫酸铜中硫元素显+6价。
D、原子最外层电子数为7(氦除外)的微粒可能是原子,则微粒不一定是稀有气体元素的原子,也可能是阳离子或阴离子。
故选:B。
【点评】本题难度不大,解答此类题时要根据不同知识的特点类推,不能盲目类推,并要注意知识点与方法的有机结合,做到具体问题能具体分析。
13.(2分)连花清瘟胶囊源自传统中医名方,可用于治疗流感,现代仪器测得其成分之一是没食子酸(分子式为C7H6O5)。关于它的说法正确的是( )
A.一个没食子酸分子由7个碳原子、6个氢原子和5个氧原子构成
B.没食子酸中碳、氢、氧三种元素的质量比为7:6:5
C.没食子酸中质量分数最多的元素是氧元素
D.没食子酸的相对分子质量是170g
【分析】A.根据物质的组成来分析;
B.根据化合物中元素的质量比来分析;
C.根据化合物中元素质量比的计算方法来分析;
D.根据相对分子质量的单位来分析。
【解答】解:A、由化学式可知、6个氢原子和5个氧原子构成;
B、没食子酸中碳、氢,说法错误;
C、没食子酸(化学式为C5H6O5)中,碳、氢、氧元素的质量比为(12×2):(1×6):(16×4)=42:3:40,说法错误;
D、相对分子质量的单位是“1”,通常省略不写;
故选:A。
【点评】本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力。
14.(2分)对于下列化学用语,有关说法正确的是( )
①NO
②Fe2+
③K2MnO4
④
⑤
A.①表示的是两种元素组成的混合物
B.③中锰元素的化合价为+6
C.②和⑤均表示阳离子
D.④和⑤表示的微粒化学性质相同
【分析】A、根据①是一氧化氮的化学式,进行分析判断。
B、根据在化合物中正负化合价代数和为零,进行分析判断。
C、离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子。
D、根据决定元素化学性质的是原子的最外层电子数,进行分析判断。
【解答】解:A、①是一氧化氮的化学式,故选项说法错误。
B、在化合物中钾元素显+1价,设锰元素的化合价是x,可得:(+1)×2+x+(﹣2)×4=7,故选项说法正确。
C、离子的表示方法,标出该离子所带的正负电荷数,正负符号在后,1要省略2+可表示铁离子;⑤质子数=核外电子数=10,故选项说法错误。
D、④和⑤表示的微粒的最外层电子数相同、氖原子,故选项说法错误。
故选:B。
【点评】本题难度不大,掌握常见化学用语(分子符号、化学式、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键。
15.(2分)如图是表示气体分子的示意图,图中“●”和“〇”分别表示两种不同原子,其中可能表示化合物的是( )
A.B.
C.D.
【分析】化合物是由不同种元素组成的纯净物。从微观角度来看是化合物的分子是由不同种原子构成的。
【解答】解:化合物是由不同种元素组成的纯净物。从微观角度来看是化合物的分子是由不同种原子构成的。
A、图中是由同种分子构成的,每个分子由不同的原子构成,故A正确;
B、图中是由两种分子构成;故B错误;
C、图中是由同种分子构成的,属于单质;
D、图中是由两种分子构成的;故D错误;
故选:A。
【点评】掌握化合物的定义注意两点:一是纯净物,二是由不同种元素组成。
16.(2分)下列关于Mg、Mg2+两种粒子的判断中不正确的是( )
A.核电荷数相同B.质量几乎相等
C.Mg2+比Mg稳定D.电子层数相同
【分析】根据Mg2+和Mg两种粒子可以看出它们都是镁元素形成的不同微粒,据此解答.
【解答】解:A、因它们是同种元素形成的微粒,故核电荷数相同;
B、镁原子失去电子形成镁离子,可以忽略不计,正确;
C、镁离子是稳定结构,不稳定,正确;
D、镁原子失去电子形成镁离子,错误;
故选:D。
【点评】本题考查原子和离子的相互转化的知识,完成此题,可以依据已有的知识进行.
17.(2分)某纯净物中只含有R和氧两种元素,且R元素与氧元素的质量比为7:16,R的相对原子质量为14( )
A.+1B.+2C.+3D.+4
【分析】R元素的氧化物中,R元素与氧元素的质量比为7:16,利用原子个数比=,从而写出化学式可计算该物质中R与O元素的原子个数比;然后根据化合物中各元素化合价代数和为0,计算氧化物中R元素的化合价。
【解答】解:由于R元素的氧化物中,R元素与氧元素的质量比为7:16、O元素的原子个数比=:,则R的氧化物的化学式为RO7;
氧元素显﹣2价,设氧化物中R元素化合价为x,则有x+(﹣2)×8=0。
故选:D。
【点评】本题是化学式的推断与化合价的计算相结合的综合题,由元素的质量比进行化学式的推断是计算化合价的基础和关键。
18.(2分)下列化学用语中,数字“2”的说法正确的是( )
①2H ②2NH3③SO2④O ⑤Mg2+⑥2OH﹣⑦H2O。
A.表示离子个数的是⑤⑥
B.表示离子所带电荷数的是④⑤
C.表示分子中原子个数的是③⑦
D.表示分子个数的是①②
【分析】标在元素符号前面的数字表示原子的个数;标在分子符号前面的数字表示分子的个数;标在离子符号前面的数字表示离子的个数;标在元素符号右上角的数字表示离子所带电荷数;标在元素符号右下角的数字表示一个分子中所含原子的个数;标在元素符号正上方的数字表示元素的化合价。
【解答】解:标在元素符号前面的数字表示原子的个数,①2H中的“2”表示两个氢原子,②4NH3中的“2”表示两个氨分子;标在元素符号右下角的数字表示一个分子中所含原子的个数7、⑦H2O中的“2”分别表示5个二氧化硫分子中含有两个氧原子、1个水分子中含有两个氢原子,故④,标在元素符号右上角的数字表示离子所带电荷数2+中的“2”表示一个镁离子带有两个单位的正电荷;标在离子符号前面的数字表示离子的个数。
A、表示离子个数的是⑥。
B、表示离子所带电荷数的是⑤。
C、表示分子中原子个数的是③⑦;
D、表示分子个数的为②。
故选:C。
【点评】本题难度不是很大,主要考查了元素符号不同位置的数字表示的意义,掌握标在元素符号不同位置的数字所表示的意义是正确解答此类题的关键所在。
19.(2分)某无人机的动力来源于锂电池,锂电池放电时生成亚锰酸锂( LiMnO2),其中锂元素显+1价,则锰元素的化合价是( )
A.﹣3B.+2C.+3D.+4
【分析】根据在化合物中正负化合价代数和为零,结合亚锰酸锂的化学式进行解答即可。
【解答】解:锂元素显+1价,氧元素显﹣2价,根据在化合物中正负化合价代数和为零,则x=+3价。
故选:C。
【点评】本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题。
20.(2分)磁悬浮的核心技术是利用超导体的反磁性。高温超导物质(Y2Ba4Cu6O13)是以YmOn、BaO和CuO为原料,经研磨烧结而成,此过程中所有元素的化合价均不变。YmOn的化学式为( )
A.Y2O3B.YO3C.Y2O5D.YO
【分析】根据化学式BaCO3和CuO求出Ba、Cu的化合价,再根据化学式Y2Ba4Cu6O13及Ba、O、Cu的化合价求出Y的化合价,最后根据Y和O的化合价求出m和n的值,然后确定YmOn的化学式。
【解答】解:根据化合价的代数和为0,碳酸根的化合价为﹣27中Ba的化合价为0﹣(﹣2)=+4。
根据化合价的代数和为0,O的化合价为﹣2;
根据化学式Y5Ba4Cu6O13及Ba、O、Cu的化合价;
由于Y为+4价,0为﹣2价,
所以YmOn的化学式为Y5O3。
故选:A。
【点评】求化合物中元素的化合价的基本依据是化合价的代数和为0,掌握化合物中元素化合价的代数和的含义的计算方法是解题的关键。
二、填空题(共3个小题,每空2分,共50分)
21.(20分)用化学符号表示:
(1)铜元素 Cu ;
(2)两个氧分子 2O2 ;
(3)3个硫酸根离子 ;
(4)由Ca2+和构成的碳酸钙 CaCO3 ;
(5)保持二氧化碳化学性质的粒子 CO2 ;
(6)氧化镁中镁元素的化合价为正二价 O ;
(7)地壳中含量最多的元素与含量最多的金属元素形成的物质是 Al2O3 ;
(8)氖气 Ne ;
(9)NH3中氮元素的化合价 H3 ;
(10)核电荷数分别为8、13的两种元素所形成的化合物 Al2O3 。
【分析】化学符号周围的数字表示不同的意义:符号前面的数字,表示原子、分子或离子的个数;右上角的数字表示一个离子所带的电荷数;右下角的数字表示几个原子构成一个分子;元素符号正上方的数字表示元素的化合价。
【解答】解:(1)由两个字母表示的元素符号,第一个字母大写,故铜元素表示为:Cu;
(2)分子用化学式表示,多个分子就是在化学式前面加上相应的数字2;
(3)离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,正负符号在后,1要省略,故2个硫酸根离子表示为:;
(4)碳酸钙由钙离子和碳酸根离子构成,钙离子显+2价,化学式为:CaCO3;
(5)二氧化碳由二氧化碳分子构成,二氧化碳分子是保持物质化学性质的最小粒子,故填:CO5;
(6)氧化镁中镁元素显+2价,元素化合价的表示方法是确定出化合物中所要标出的元素的化合价,正负号在前,所以氧化镁中镁元素的化合价为+2价O;
(7)地壳中含量最多的元素是氧元素,含量最多的金属元素是铝元素,氧化铝中铝元素显+3价,化学式为:Al2O6;
(8)氖气由氖原子构成,化学式为:Ne;
(9)氨气中氢元素显+1价,根据化合物中,正,可得氮元素显﹣3价,然后在其化学式该元素的上方用正负号和数字表示,数字在后H3;
(10)原子序数=质子数=核电荷数,8号元素是氧元素,它们形成的化合物是氧化铝,氧元素显﹣2价2O3。
故答案为:(1)Cu;
(2)8O2;
(3)
(4)CaCO3;
(5)CO6;
(6)O;
(7)Al2O3;
(8)Ne;
(9)H3;
(10)Al7O3。
【点评】本题主要考查化学符号及其周围数字的意义,需要学生掌握标在元素符号不同位置的数字所代表的含义。
22.(10分)化学与生活密切相关。
①新鲜的苹果切开后因亚铁离子被氧化会很快变黄,亚铁离子的符号 Fe2+ 。
②食品袋中的干燥剂为生石灰,主要成分是氧化钙,氧化钙的化学式为 CaO 。氧元素的质量分数是 28.6% 。(精确到0.1%)
③全脂高钙奶粉中的“钙”是指 元素 (填“分子”或“原子”或“元素”)。
④某食盐中“碘”主要以碘酸钾(KIO3)的形式加入,其中碘元素的化合价为 +5 价。
【分析】①根据离子符号的写法分析回答;
②根据化学式的写法和意义分析回答;
③根据物质的组成常用元素来描述分析;
④根据化学式的意义和化合价原则分析回答。
【解答】解:①每个亚铁离子带有2个单位的正电荷,其符号是:Fe2+。
②食品袋中的干燥剂为生石灰,主要成分是氧化钙,氧化钙中氧元素的质量分数是:。
③物质的组成常用元素来描述,全脂高钙奶粉中的“钙”是指元素。
④碘酸钾中钾元素显+7价,氧元素显﹣2价,根据在化合物中正负化合价代数和为零,则x=+5价;
故答案为:(1)Fe4+;
(2)CaO;28.6%;
(3)元素;
(4)+5。
【点评】本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易。
23.(20分)在“宏观—微观—符号”之间建立联系,是化学学科独有的思维方式。
(1)根据下列粒子结构示意图1,回答问题。
①A、B、C、D所示粒子共表示 3 种元素(填数字)。
②D所示粒子在化学反应中容易 得到 电子(填“得到”或“失去”)。
③若E中X=10时,则该粒子属于 原子 (填“原子”或“离子”)。
④若B、E两种粒子属于同种元素,则X= 12 ,请写出E的化学符号 Mg2+ 。
⑤BD形成化合物的化学式 MgCl2 。
(2)原子序数为1~18的元素的原子结构示意图等信息如图2,回答问题。
①原子序数为14的元素位于元素周期表中第 三 周期,同一周期 原子核外电子层 数相等。
②根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子 最外层电子数 相同,所以氟元素与氯元素的化学性质相似。
③同周期元素(从第二周期开始),从左到右,各元素原子随原子序数的增加 从1到8依次递增 。
【分析】(1)根据元素的概念、最外层电子数、质子数与电子数的关系、化学符号的写法来分析;
(2)根据元素周期表的规律、最外层电子数决定元素的化学性质以及元素周期表的规律来分析。
【解答】解:(1)①质子数决定元素的种类,A、B、C、D所示粒子的质子数有三种;故答案为:3;
②D所示粒子的最外层有7个电子,多于3个;故答案为:得到;
③若E中X=10时,该粒子的质子数等于电子数;故答案为:原子;
④质子数决定元素的种类,若B,则X=12,核外有10个电子,镁离子的化学符号为Mg2+;故答案为:12;Mg2+;
⑤B是12号元素,是镁元素,D是17号元素,在化合物中显﹣5价2;故答案为:MgCl2;
(2)①原子序数为14的元素位于元素周期表中第三周期,同一周期原子核外电子层数相等;原子核外电子层;
②根据氟原子和氯原子的结构示意图分析,由于氟原子和氯原子最外层电子数相同;故答案为:最外层电子数;
③同周期元素(从第二周期开始),从左到右,最外层电子数从5到8依次递增。
【点评】本题主要考查粒子结构示意图的意义,由题目给出信息,推断该元素的原子构成,对于原子构成的一些规律应当熟记.了解元素周期表的有关知识。
三、计算题(本题有1个小题,每空2分,共10分)
24.(10分)我国科学家屠呦呦因为发现青蒿素(化学式为C15H22O5),一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命而荣获2015年诺贝尔生理学或医学奖.
(1)青蒿素的相对分子质量为 282 ;
(2)青蒿素中各原子的原子个数比C:H:O= 15:22:5 ;
(3)青蒿素中碳、氢两种元素的质量比为 90:11 ;
(4)青蒿素中氧元素的质量分数为 28.4% (计算结果保留一位小数);
(5)在1972年发现青蒿素前治疗疟疾的药物主要是金鸡纳霜,又叫奎宁(化学式为C20H24N2O2,相对分子质量为324),求141g青蒿素中所含氧元素的质量与多少克金鸡纳霜中所含氧元素质量相等?(写出计算过程)
【分析】(1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据青蒿素的化学式为C15H22O5,推测青蒿素中各原子的原子个数比;
(3)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
(4)根据化合物中元素的质量分数=×100%,进行分析解答.
(5)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
【解答】解:(1)C15H22O5的相对分子质量为12×15+1×22+16×4=282.
(2)根据青蒿素的化学式为C15H22O5,故青蒿素中各原子的原子个数比15:22:5;
(3)青蒿素中碳、氢元素的质量比为(12×15):(2×22)=90:11.
(4)青蒿素中氧元素的质量分数为×100%≈28.4%.
(5)141g青蒿素中含有氧元素的质量为141g××100%=40g;
C20H24N8O2的相对分子质量为324,故其氧元素的质量分数为,故需要金鸡纳霜的质量为40g÷.
故答案为:
(1)282;(2)15:22:5;(4)28.4%
【点评】本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.
相关试卷
这是一份2023-2024学年山东省东营市广饶县大王镇中心初中学八年级(上)月考化学试卷(12月份),共7页。试卷主要包含了选择题,填空与简答题等内容,欢迎下载使用。
这是一份2023-2024学年山东省东营市广饶县八年级(上)期中化学试卷,共30页。试卷主要包含了选择题,填空题等内容,欢迎下载使用。
这是一份2023-2024学年山东省东营市广饶县九年级(上)期中化学试卷,共20页。试卷主要包含了单选题,填空题,简答题,科普短文题,实验题,探究题,计算题等内容,欢迎下载使用。









