





初中化学人教版(2024)九年级下册(2024)课题2 常见的酸和碱获奖课件ppt
展开1.以盐酸、硫酸为例,通过实验探究认识酸的化学性质和用途,并能用化学方程式表示2.能从物质类别的角度初步形成对“酸类”性质的认识,建立“同类物质在性质上具有一定的相似性”的概念
你吃过这些食物吗?有什么感受?
“酸”最早指“有酸味的酒”。在酿酒的时候,有时把比较珍贵的酒放在窖中保存,酒在微生物的作用下会产生酸味。
在实验室,我们经常用到的酸是盐酸和硫酸
盐酸和硫酸有哪些性质和用途呢?
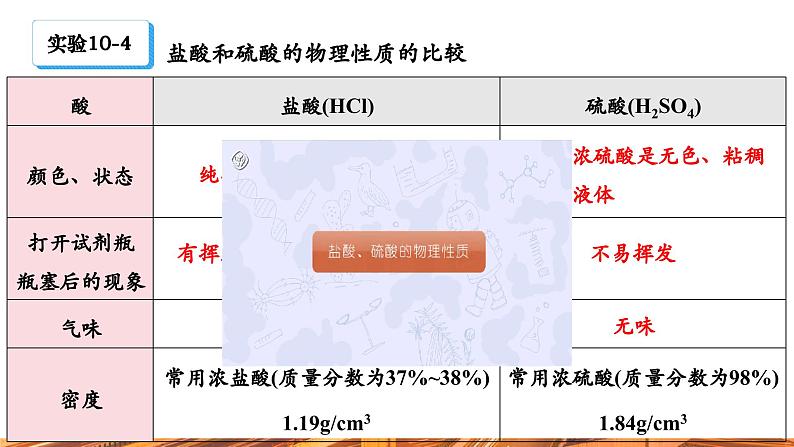
盐酸和硫酸的物理性质的比较
纯净的浓盐酸是无色的液体
纯净的浓硫酸是无色、粘稠的油状液体
有挥发性,能在空气中形成白雾
实验中打开盛装浓盐酸的瓶盖,瓶口处就会出现白雾,白雾是如何形成的呢?
浓盐酸具有很强的挥发性,挥发出来的HCl气体溶解在空气中的水蒸气中,形成盐酸小液滴。
用浓盐酸使制得的CO2气体中含有较多的HCl气体
浓盐酸需要密封保存,那浓硫酸需要密封保存吗?为什么?
浓硫酸也需要密封保存,因为其具有吸水性
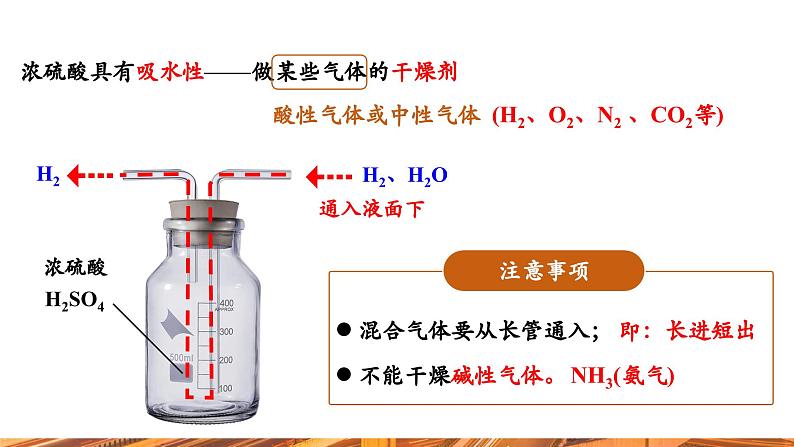
浓硫酸具有吸水性——做某些气体的干燥剂
(H2、O2、N2 、CO2等)
混合气体要从长管通入;
敞口放置在空气中的浓盐酸和浓硫酸的比较
将滤纸、小木条、纱布放在玻璃片上,完成下列实验
浓硫酸有强烈的腐蚀性。它能夺取纸张、木材、布料、皮肤(都由含碳、氢、氧等元素的化合物组成)里的水分,生成黑色的炭。
也可称为浓硫酸的脱水性
如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后涂上质量分数为3%~5%的碳酸氢钠溶液
也需要处理,稀硫酸随着水分的蒸发会变成浓度较高的硫酸,同样具有强腐蚀性
实验室一般使用稀硫酸进行实验,那么如何将浓硫酸进行稀释呢?
浓硫酸溶于水____热
玻璃棒作用:_____________________
酸入水;沿器壁,慢慢倒,不断搅
小组讨论:浓硫酸稀释时要注意“酸入水”,为什么不能将水注入浓硫酸中呢?
如果将水注入浓硫酸,由于水的密度较小,水会浮在浓硫酸上面,浓硫酸溶解时放出的热能使水立刻沸腾,使浓硫酸液滴向四周飞溅。这是非常危险的操作!
盐酸、硫酸等酸具有非常广泛的用途。
实验室和工业生产中常用的酸除了盐酸、硫酸,还有硝酸(HNO3)、醋酸(CH3COOH)等。 另外,生活中常见的许多物质中也含有酸。
柠檬、柑橘等水果中含有柠檬酸
汽车用铅酸蓄电池中含有硫酸
1.下列有关酸的性质说法正确的是( )A. 浓盐酸和浓硫酸均有刺激性气味B. 打开盛有浓硫酸和浓盐酸的试剂瓶均看到白雾C. 浓盐酸和浓硫酸都可用来干燥二氧化碳D. 敞口放置一段时间的浓盐酸和浓硫酸,溶质的质量分数都变小
Ⅱ 酸的化学性质
酸能使紫色的石蕊溶液变红,不能使无色酚酞溶液变色。
结合前面所学内容,预测稀盐酸、稀硫酸能使石蕊溶液和酚酞溶液分别呈现什么颜色。
回忆金属分别与稀盐酸和稀硫酸的反应,写出化学方程式。
2. 酸与活泼金属反应
Mg + 2HCl === MgCl2 + H2↑
Zn + 2HCl === ZnCl2 + H2↑
Fe + 2HCl === FeCl2 + H2↑
Mg + H2SO4 === MgSO4 + H2↑
Zn + H2SO4 === ZnSO4 + H2↑
Fe + H2SO4 === FeSO4 + H2↑
酸能与较活泼的金属(排在H前的金属)反应产生对应的金属化合物和氢气
在分别盛有稀盐酸和稀硫酸的试管中各放入生锈的铁钉,过一会儿取出铁钉,用水洗净,铁钉表面和溶液颜色有什么变化?
Fe2O3 + 3H2SO4 === Fe2(SO4) 3 + 3H2O
铁锈消失,铁钉变得光亮,无色溶液变黄
Fe2O3 + 6HCl === 2FeCl3 + 3H2O
酸能与某些金属氧化物反应对应的金属化合物和水
3. 酸与金属氧化物反应
除锈时能否将铁制品长时间浸在酸中?
Fe2O3 + 6HCl === 2FeCl3+ 3H2O
Fe2O3+3H2SO4 === Fe2(SO4)3+ 3H2O
Fe + 2HCl === FeCl2 + H2↑
1. Al2O3 + HCl === ______________
3. 将铜丝和氧化铜固体加入稀硫酸中,发生的化学反应有_____________________________
2. 未打磨的镁条放入足量盐酸中,发生的化学反应:______________________________________________________
2AlCl3+3H2O
MgO + 2HCl === MgCl2 + H2O、Mg + 2HCl === MgCl2 + H2↑
CuO +H2SO4 === CuSO4+ H2O
与金属氧化物反应 ,反应前后化合价不变;与金属活动性无关
现象:黑色粉末溶解,溶液由无色变蓝色
酸能与活泼金属反应生成对应的金属化合物和氢气
酸能与金属氧化物反应生成对应的金属化合物和水
Fe2+的化合溶液呈______色, Fe3+的化合物溶液呈_____色,Cu2+的化合物溶液呈_____色
稀盐酸、稀硫酸等酸为什么会有相似的化学性质呢?
在稀盐酸、稀硫酸中存在带电荷的粒子
通过研究和分析可知,像盐酸、硫酸这样的酸,在水中都能解离出H+和酸根离子。
酸具有相似化学性质的原因是溶液中都含有_____
HCl在水中解离出离子示意图
H2SO4在水中解离出离子示意图
硫酸:无色、粘稠的油状液体;有吸水性、腐蚀性、溶于水放热,稀释时“酸入水”
盐酸:无色液体,有挥发性,有刺激性气味
与活泼金属反应生成对应的金属化合物和氢气
石蕊溶液遇酸变红色,酚酞溶液遇酸不变色
与金属氧化物反应生成对应的金属化合物和水
1. 根据以上实验和讨论,同学们对酸的通性有了一定的了解。下列有关酸的通性说法正确的是( )A. 酸均能使紫色石蕊溶液变红B. 酸均能使无色酚酞溶液变蓝C. 酸均能用铁质容器盛放D. 酸均能与金属氧化物反应生成有色溶液
如MgO + 2HCl === MgCl2 + H2O
2.盐酸和硫酸是初中化学常见的两种酸,下列相关说法不正确的是( )A. 盐酸和硫酸均由氢离子和酸根离子构成B. 盐酸和硫酸都可用于金属表面除锈C. 稀释浓硫酸时需将水缓慢加入浓硫酸中,并用玻璃棒搅拌D.稀盐酸和稀硫酸有相似的化学性质,是因为溶液中都有H+
3.在天平左右两端分别放着两个盛有浓盐酸和浓硫酸的烧杯,调至平衡,一段时间后,判断天平的变化情况是( )A. 指针左偏B. 指针右偏C. 无变化D. 无法判断
浓盐酸具有挥发性,易挥发出氯化氢气体导致溶质质量减少,因此天平左侧质量减少,浓硫酸具有吸水性,易吸收空气中水蒸气导致溶剂质量增大。
4.实验室为了收集干燥的二氧化碳气体,将制取的气体先后通过甲、乙两装置。下列关于甲、乙两装置导管的连接方式正确的是( )A. a接c B. a接d C. b接c D. b接d
浓硫酸具有吸水性,二氧化碳的密度比空气大。为了收集干燥的二氧化碳气体,应将制取的气体先通过甲装置,且气体应该从长导管通入。
5.学习完酸的化学性质,小凯构建了如图所示的知识网络图。请回答:(1)溶液X是一种酸,试剂A的名称是_____________。(2)若X是稀硫酸、B是氧化物,B的化学式为_______。(3)若X是稀盐酸、C是单质,则C的名称为____。(4)若X是稀盐酸、D是碳酸钙,则X与D反应的化学方程式为___________________________________。
2HCl + CaCO3 === CaCl2 + H2O + CO2↑
初中化学人教版(2024)九年级下册(2024)课题3 常见的盐精品ppt课件: 这是一份初中化学人教版(2024)九年级下册(2024)<a href="/hx/tb_c4056743_t3/?tag_id=26" target="_blank">课题3 常见的盐精品ppt课件</a>,共28页。PPT课件主要包含了写出下列化学方程式,澄清溶液变浑浊,化学方程式,化合反应,分解反应,置换反应,复分解反应,单换单,多变一,酸和碱的反应等内容,欢迎下载使用。
初中化学人教版(2024)九年级下册(2024)课题2 常见的酸和碱公开课ppt课件: 这是一份初中化学人教版(2024)九年级下册(2024)<a href="/hx/tb_c4056742_t3/?tag_id=26" target="_blank">课题2 常见的酸和碱公开课ppt课件</a>,共31页。PPT课件主要包含了观察到什么现象,没有明显现象,反应的实质,化学方程式,盐酸+氢氧化铁,盐酸+氢氧化铜,发生了反应,Ⅰ中和反应,文字表达式,中和反应是放热反应等内容,欢迎下载使用。
人教版(2024)九年级下册(2024)课题2 常见的酸和碱试讲课课件ppt: 这是一份人教版(2024)九年级下册(2024)<a href="/hx/tb_c4056742_t3/?tag_id=26" target="_blank">课题2 常见的酸和碱试讲课课件ppt</a>,共29页。PPT课件主要包含了生活中常见的碱,因为其中含有碱性物质,氢氧化钠,化学式NaOH,白色固体,表面潮湿并逐渐溶解,容易吸收水分,密封保存,氢氧化钠的用途,氢氧化钙等内容,欢迎下载使用。














