













化学九年级下册(2024)课题2 金属的化学性质评课ppt课件
展开1.知道铁、铝、铜等常见金属与氧气的反应;2.初步认识常见金属与稀盐酸、稀硫酸的置换反应;3.知道置换反应的概念与特征。
为什么出土的文物中,金器总是保存得基本完好,铜器表面有锈迹,而铁器锈迹斑斑?
知识点1 金属与氧气的反应
大多数金属都能与氧气发生反应,但反应的难易和剧烈程度不同。
(1)常温或点燃时能反应:
常温下:4Al + 3O2 2Al2O3 在空气中点燃:2Mg + O2 2MgO
在氧气中点燃:在空气中加热:
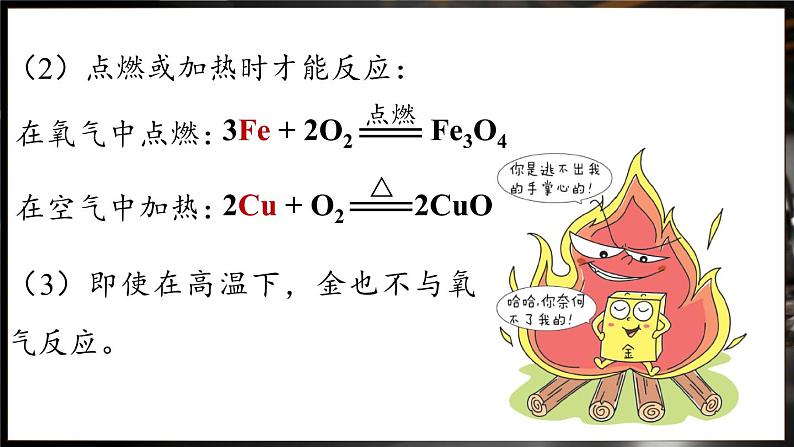
(2)点燃或加热时才能反应:
(3)即使在高温下,金也不与氧气反应。
(1)镁、铝比较活泼;(2)铁、铜次之;(3)金最不活泼。
我们从上述实验事实可以发现:
想一想,为什么铝具有优良的抗腐蚀性能?
典例1 下列有关金属与氧气反应的说法正确的是( )
A.铁丝在氧气中剧烈燃烧、火星四射,生成三氧化二铁B.金属与氧气的反应必须加热或点燃C.铝的抗腐蚀性好是因为铝的化学性质稳定D.“真金不怕火炼”说明即使在高温下金也不和氧气反应
镁、铝常温下也可与氧气反应
知识点2 金属与稀盐酸、稀硫酸的反应
迅速产生大量气泡,反应速率最快
Mg + 2HCl MgCl2 + H2↑Mg + H2SO4 MgSO4+ H2↑
产生大量气泡,反应速率较快
Zn + 2HCl ZnCl2 + H2↑Zn + H2SO4 ZnSO4 + H2↑
产生少量气泡,反应速率较慢,溶液由无色变为浅绿色
Fe + 2HCl FeCl2 + H2↑Fe + H2SO4 FeSO4 + H2↑
(1)镁、锌、铁三种金属都能与盐酸或稀硫酸反应,生成氢气,但反应的剧烈程度不同,铜不与盐酸或稀硫酸反应;(2)根据金属能否与稀盐酸、稀硫酸反应,可判断它们的活动性强弱:能反应的金属比不能反应的金属活动性强。
仔细观察这些反应,你有什么发现?
概念:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应叫置换反应。
特征:单质 + 化合物 → 新化合物 + 新单质。
置换反应中一定有元素化合价的变化
通式:A+BC →AC+B
化合反应、分解反应和置换反应的比较
典例2 下列属于置换反应的是( )
A.2H2O 2H2 ↑ + O2 ↑B.S + O2 SO2C.NaOH + HCl NaCl + H2OD.2Al + 6HCl 2AlCl3 + 3H2 ↑
1.黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。“真金不怕火炼”主要是指金( )A.熔点高B.延展性好C.有金属光泽 D.化学性质稳定
2.下列几项物质中,不能用金属和稀硫酸直接反应制得的是( )A.硫酸镁 B.硫酸锌C.硫酸亚铁 D.硫酸铜
A. Al B.Mg C. Fe D.Zn
3.下列金属各2g,分别与足量稀盐酸反应,生成氢气最多的是( )
初中课题 2 金属的化学性质优秀课件ppt: 这是一份初中<a href="/hx/tb_c9862_t3/?tag_id=26" target="_blank">课题 2 金属的化学性质优秀课件ppt</a>,共27页。PPT课件主要包含了金属与氧气反应,你知道吗,金属与酸反应,你有什么发现,置换反应,活动性Fe﹥Cu,金属与盐溶液反应等内容,欢迎下载使用。
初中化学人教版九年级下册课题 2 金属的化学性质试讲课课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9862_t3/?tag_id=26" target="_blank">课题 2 金属的化学性质试讲课课件ppt</a>,共27页。PPT课件主要包含了金属与氧气反应,你知道吗,金属与酸反应,你有什么发现,置换反应,活动性Fe﹥Cu,金属与盐溶液反应等内容,欢迎下载使用。
初中化学人教版九年级下册课题 2 金属的化学性质课文ppt课件: 这是一份初中化学人教版九年级下册课题 2 金属的化学性质课文ppt课件,共15页。PPT课件主要包含了学习目标,探究活动,活动探究,反应化学方程式,上述反应有什么特点,友情提示等内容,欢迎下载使用。













