






所属成套资源:新人教版化学必修第一册PPT课件+教学设计全册
高中化学人教版 (2019)必修 第一册第二节 氯及其化合物教学ppt课件
展开
这是一份高中化学人教版 (2019)必修 第一册第二节 氯及其化合物教学ppt课件,文件包含核心素养人教版高中化学必修一《氯及其化合物》第二课时课件pptx、核心素养人教版高中化学必修一《氯及其化合物》第二课时教学设计含教学反思docx等2份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
宏观辨识与微观探析: 掌握氯气的实验室制法,氯离子的检验方法。证据推理与模型认知: 通过实验探究氯气的实验室制法,观察、分析实验现象,增强发现问题和解决问题的能力。科学探究与创新意识:能结合实验室制取氯气的装置特点设计制备其他气体的实验装置,提升实验能力。
1.掌握氯气的实验室制法。2.掌握氯离子的检验方法。重点:氯气的实验室制法,氯离子的检验方法。难点:氯气的实验室制法,氯离子的检验方法。
思考:你能否根据舍勒制备氯气的方法来制备氯气?
思考:根据舍勒发现氯气的过程,你能找到氯气的制备方法吗?已知反应中MnO2被还原为MnCl2,请写出反应的化学方程式和离子方程式,画出双线桥。
注意:(1)加热条件下进行, MnO2不和稀盐酸反应,盐酸变稀,反应停止(2)浓盐酸的作用:还原性与酸性(1:1)
浓盐酸能够全部消耗吗?起什么作用(氧化剂/还原剂)?
实验中需缓慢加热且加热温度不宜过高,为什么?
可以用其他氧化剂来代替MnO2吗?
浓盐酸易挥发,故必须缓慢加热且控制温度,避免Cl2中混有大量的HCl杂质,同时以免降低了HCl的利用率。
可以, KMnO4、 KClO3 、Ca(ClO)2等也可作该反应的氧化剂。
小结实验室用软锰矿制取氯气的反应特点:
2KMnO4+16HCl ( 稀 ) = 2KCl+2MnCl2+5Cl2↑+8H2O
KClO3 + 6HCl(浓) = KCl + 3Cl2↑ + 3H2O
Ca(ClO)2+4HCl(浓)= CaCl2+2Cl2↑+2H2O
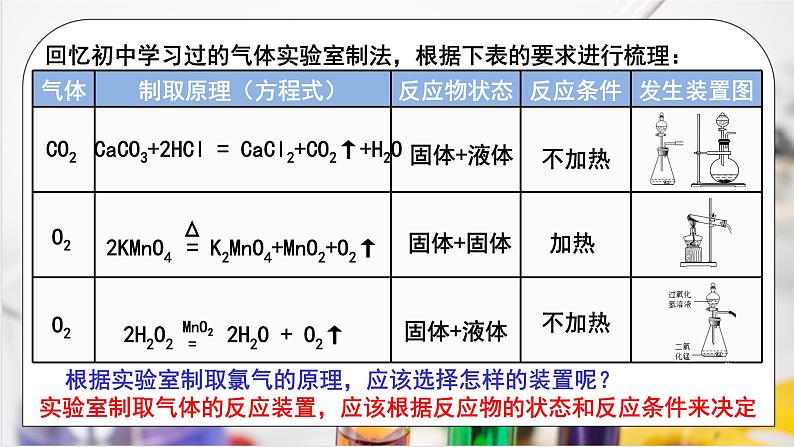
回忆初中学习过的气体实验室制法,根据下表的要求进行梳理:
CaCO3+2HCl = CaCl2+CO2↑+H2O
根据实验室制取氯气的原理,应该选择怎样的装置呢?
实验室制取气体的反应装置,应该根据反应物的状态和反应条件来决定
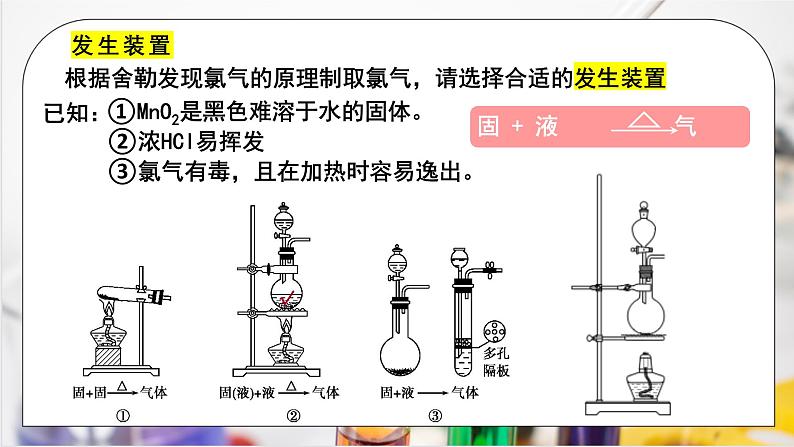
①MnO2是黑色难溶于水的固体。
③氯气有毒,且在加热时容易逸出。
根据舍勒发现氯气的原理制取氯气,请选择合适的发生装置
①Cl2 有毒,且密度比空气大②Cl2能溶于水,难溶于饱和食盐水
根据舍勒发现氯气的原理制取氯气,请选择合适的收集装置
收集装置:1、向上排空气法 2、排饱和食盐水法
用向上排空气法收集的Cl2如何验满?
①集体瓶中充满黄绿色气体。②将湿润的淀粉碘化钾试纸靠近瓶口,观察到试纸立即变蓝③湿润的蓝色石蕊试纸放在瓶口,观察到试纸先变红后褪色
实验室制氯气是否需要进行尾气吸收?如果需要,那该用什么吸收氯气呢?
需要,用NaOH等强碱进行吸收 Cl2+2NaOH=NaCl+NaClO+H2O
思考:用以下装置收集到的氯气纯净吗?有哪些杂质?如何除去?有没有先后顺序?
①Cl2能溶于水,难溶于饱和食盐水;②HCl易溶于饱和食盐水
装置Ⅰ(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。装置Ⅱ(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
浓硫酸或干燥的CaCl2
仪器组装顺序:
自下而上、从左到右
注意导气管的进出方式(长进短出)为什么?
尾气处理时,能用澄清石灰水吸收氯气吗?
尾气处理时,不能用澄清石灰水吸收氯气,因为澄清石灰水中Ca(OH)2的含量少,吸收不完全。
请同学们画出实验室制取氯气的实验装置图
①固固加热型②固液不加热型③固液加热型④液液加热型
反应物状态以及是否需要加热
考虑气体的密度、溶解度以及是否与水反应
依据气体及所含杂质的性质
思考:请同学们根据实验室制取氯气的过程,从发生装置、收集装置、除杂、尾气处理等方面总结实验室制取干燥纯净气体的方法模型。
[实验2-9]在三只试管中分别加入2~3mL稀盐酸、NaCl溶液、Na2CO3溶液,然后各滴入几滴AgNO3溶液,观察现象。再分别加入少量稀硝酸,观察现象。
产生白色沉淀,沉淀不溶解
产生白色沉淀,后沉淀溶解,产生气泡
Ag++Cl-===AgCl↓
2Ag++CO32-===Ag2CO3↓
Ag2CO3+2H+===CO2↑+H2O
检验氯离子方法:取少量待测液加入试管中,先加入足量的稀硝酸酸化,再滴加硝酸银溶液,若有白色沉淀产生,则有Cl-。
酸化的试剂能不能选用稀盐酸或者稀硫酸?
不能。稀盐酸酸化,引入Cl-,也会产生白色沉淀,对实验造成干扰。稀硫酸酸化,引入SO42-,会产生白色的硫酸银沉淀,对实验造成干扰。
向溶液中加入过量稀硝酸,防止溶液中含有碳酸根离子、碳酸氢根离子等的干扰。
练习1、下列检验Cl-的方法正确的是 ( )A.向某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-B.向某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-C.向某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-D.向某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl-
A.Ⅰ图中:如果MnO2过量,盐酸就可全部消耗B.Ⅱ图中:如果倒置的量筒充满了氯气,水槽内装满水,经足够长的时间光照,量筒内最后剩余气体为HCl和氧气C.Ⅲ图中:生成蓝色的烟D.Ⅳ图中:b能褪色,反应后将硫酸溶液滴入烧杯中至溶液呈酸性,结果有Cl2生成
练习2、某同学用下列装置制备并检验Cl2的性质。下列说法正确的是( )
练习3、ClO2是一种黄绿色气体,在空气中浓度超过10%时会有很强的爆炸性。依据反应3NaClO3+2H2SO4 NaClO4+2ClO2↑+2NaHSO4+H2O,实验室可制备少量NaClO2溶液。回答下列问题:
(1)组装好仪器后,应先___________________,再加入药品,然后操作顺序为_______。 a.打开K b.滴加浓硫酸 c. 通入N2 (2)通N2的主要目的是_________________________________________________;装置②的作用____________________;装置③中氧化产物与还原产物的个数比为_______。
稀释ClO2 ,防止爆炸,
并使生成的ClO2进入后续装置
相关课件
这是一份高中人教版 (2019)第三节 物质的量教学课件ppt,文件包含核心素养人教版高中化学必修一《物质的量》第三课时课件pptx、核心素养人教版高中化学必修一《物质的量》第三课时教学设计含教学反思docx等2份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学ppt课件,文件包含核心素养人教版高中化学必修一《物质的量》第二课时课件pptx、核心素养人教版高中化学必修一《物质的量》第二课时教学设计含教学反思docx等2份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册第三节 物质的量教学课件ppt,文件包含核心素养人教版高中化学必修一《物质的量》第一课时课件pptx、核心素养人教版高中化学必修一《物质的量》第一课时教学设计含教学反思docx等2份课件配套教学资源,其中PPT共25页, 欢迎下载使用。









