



化学鲁科版 (2019)第2节 醇和酚图文课件ppt
展开
这是一份化学鲁科版 (2019)第2节 醇和酚图文课件ppt,共28页。PPT课件主要包含了学习目标,联想质疑,课堂小结等内容,欢迎下载使用。
1、熟知乙醇的结构与性质,了解乙醇的工业制法。2、了解醇的分类与命名,熟知醇和酚结构特点的不同并能通过乙醇的性质分析理解醇的化学性质。3、能够设计醇到烯烃、卤代烃、醛、酮、酯的转化路线。
醇和酚都是重要的有机化合物。例如,常用作燃料和饮料的酒精(乙醇)、汽车发动机防冻液中的乙二醇、化妆品中的丙三醇含有醇羟基,茶叶中的茶多酚、用于制药皂的苯酚、漆器上涂的漆酚含有酚羟基。 一位著名的有机化学家曾说过,假如让一个有机化学家带上10 种有机化合物到荒岛上独自工作,他的选择里一定会有醇。有了醇,他就能合成出各种各样的有机化合物。那么,在有机化合物的合成中醇为什么会有如此重要的作用?
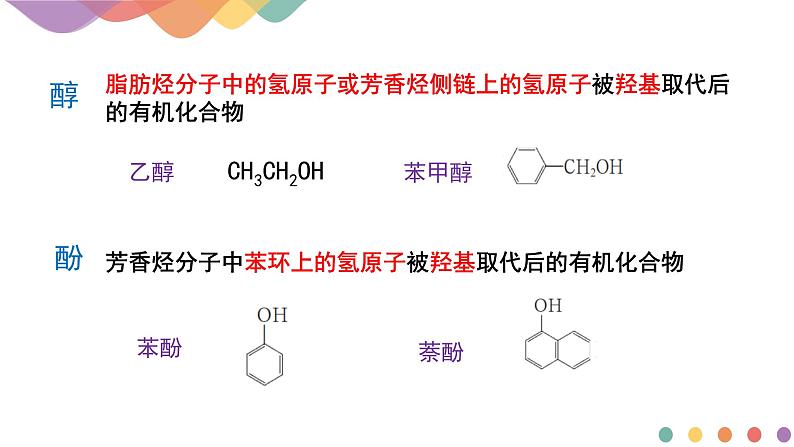
脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基取代后的有机化合物
芳香烃分子中苯环上的氢原子被羟基取代后的有机化合物
乙醇 CH3CH2OH
⑴定义:脂肪烃烃分子中的氢原子或芳香烃侧链上的氢原子被羟基取代后的有机化合物称为醇。
⑵醇的官能团: 名称:羟基 结构简式:—OH 电子式:
⑷注意:①羟基如果连在双键碳或三键碳上不稳定 ②两个羟基不能连在同一个碳上。
⑶饱和一元醇的通式:CnH2n+1OH(或CnH2n+2O)
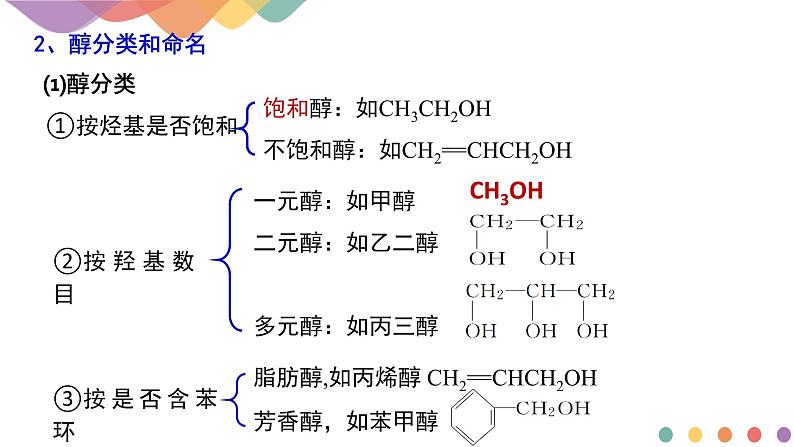
饱和醇:如CH3CH2OH不饱和醇:如CH2==CHCH2OH
一元醇:如甲醇二元醇:如乙二醇多元醇:如丙三醇
脂肪醇,如丙烯醇 CH2==CHCH2OH芳香醇,如苯甲醇
1,2,3-丙三醇(甘油)
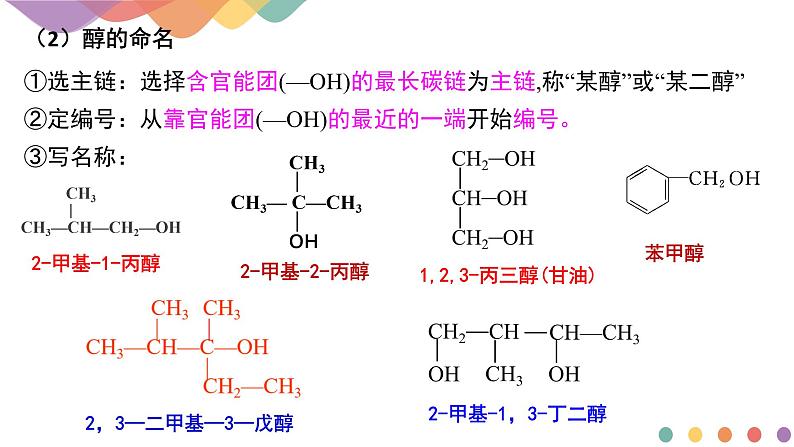
①选主链:选择含官能团(—OH)的最长碳链为主链,称“某醇”或“某二醇”②定编号:从靠官能团(—OH)的最近的一端开始编号。③写名称:
苯甲醇
2,3—二甲基—3—戊醇
2-甲基-1,3-丁二醇
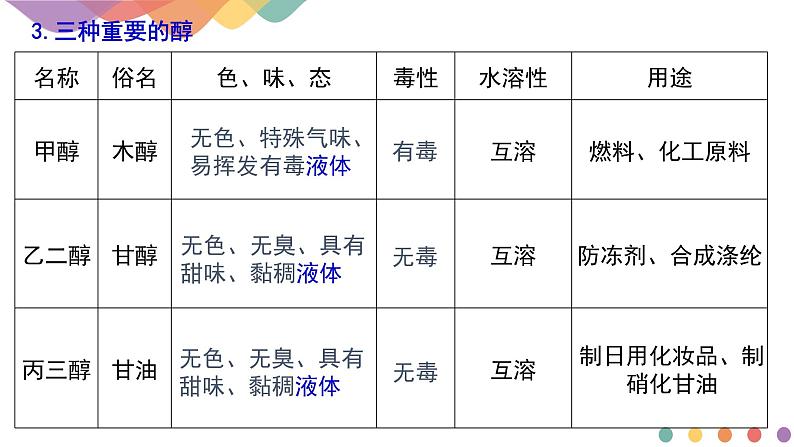
无色、特殊气味、易挥发有毒液体
无色、无臭、具有甜味、黏稠液体
(2)溶解性①碳原子数为1~3的饱和一元醇和多元醇能与水以任意比例互溶。碳原子数为4~11的饱和一元醇为油状液体,仅可部分溶于水。碳原子数目更多的高级醇为固体,不溶于水。②含羟基较多的醇易溶于水。
(1)沸点①相对分子质量接近的饱和一元醇和烷烃或烯烃相比,饱和一元醇的沸点远远高于烷烃或烯烃。②饱和一元醇,随分子中碳原子数的增加沸点逐渐升高。③碳原子数相同时,羟基个数越多,沸点越高。
1.今有四种有机物:①丙三醇;②丙烷;③乙二醇;④乙醇。它们的沸点由高到低排列顺序正确的是 ( ) A.①②③④ B.④③②① C.①③④② D.①③②④
醇的羟基之间易形成氢键,故醇的沸点比同碳原子数的烃要高,醇中碳原子数越多,其沸点越高,碳原子数相同的醇,所含羟基数目越多,形成氢键的几率越高,其沸点越高,故四种物质的沸点由高到低的顺序为①③④②,C项正确。
CH3CH2OH + Na →
CH3CH2ONa + H2↑
2ml -OH ~ 2ml Na ~ 1mlH2
乙醇和水分别与金属钠反应,哪个现象更为剧烈?说明了什么?
水与金属钠反应更为剧烈,说明水中羟基氢更活泼
向试管里先加入碎瓷片,再加入3mL乙醇,然后一边摇动试管一边慢慢地加入2mL浓硫酸,最后加入2mL乙酸的混合物。按图所示连接装置,用酒精灯均匀地加热试管,将产生的气体经导管通到滴有酚酞试液饱和碳酸钠溶液的液面上。
2、醇的取代反应(1)酯化反应
定义:酸和醇起作用,生成酯和水的反应叫做酯化反应。
实验现象:Na2CO3饱和溶液的液面上有透明的油状液体产生,并可闻到香味,振荡后溶液红色变浅或消失。
催化剂:提高反应速率;
吸水性:浓硫酸可以吸收生成物中的水使反应向正反应方向进行.
(2)饱和碳酸钠溶液的作用:
c.降低乙酸乙酯的溶解度,便于酯的析出。
不能用NaOH代替Na2CO3,因为NaOH碱性太强,使乙酸乙酯水解
练习: ①CH3CH2OH +
② CH3CH=CH-COOH +
CH3CH2OH + HBr
CH3CH2Br + H2O
2、醇的取代反应(2)与氢卤酸(HX)反应
强碱水溶液,加热—X被—OH取代
氢卤酸,加热—OH被—X取代
乙醚是一种无色、易挥发的液体,沸点34.5℃,有特殊气味,有麻醉作用。乙醚微溶于水,易溶于有机溶剂,本身是一种优良溶剂,能溶解多种有机物。【醚类物质】醚的结构可用R—O—R′来表示,R和R′都是烃基,可以相同,也可以不同。官能团:醚键饱和一元醚的通式:CnH2n+2O (n≥2)
2、醇的取代反应(3)醇分子间脱水成醚
3、消去反应(分子内脱水成烯)
2CH3CH2OH + O2
2CH3CHO + 2H2O
紫红色(MnO4—)退去(Mn2+)
(3) 被强氧化剂氧化
醇使酸性高锰酸钾褪色的条件:羟基相连的碳上要有氢(存在а-H)
乙醇的化学反应与断键位置
1.与活泼金属置换反应
2、乙醇、乙二醇(HOCH2CH2OH)、甘油(丙三醇:HOCH2CHOHCH2OH)分别与足量金属钠作用,产生等量的氢气,则三种醇的物质的量之比为( ) A.6∶3∶2 B.1∶2∶3 C.3∶2∶1 D.4∶3∶2
3、丙烯醇(CH2==CH—CH2OH)可发生的化学反应有( ) ①加成 ②氧化 ③燃烧 ④加聚 ⑤取代 A.①②③ B.①②③④ C.①②③④⑤ D.①③④
4、下列醇既能被催化氧化生成醛,又能发生消去反应生成烯烃的是( ) A.CH3OH B. C. D.
相关课件
这是一份高中化学苏教版 (2019)选择性必修3第一单元 醇和酚一等奖ppt课件,文件包含411醇同步课件pptx、乙醇水与钠的反应比较实验mp4、乙醇的氧化反应实验wmv、乙醇的消去反应实验wmv等4份课件配套教学资源,其中PPT共42页, 欢迎下载使用。
这是一份高中鲁科版 (2019)第2章 官能团与有机化学反应 烃的衍生物第2节 醇和酚获奖课件ppt,共20页。PPT课件主要包含了素养目标,醇的概述,三种重要的醇,②溶解性,-甲基-2-,醇的命名,-甲基-2-戊醇,醇的化学性质,醇化学性质难点突破,醇的消去反应规律等内容,欢迎下载使用。
这是一份高中化学鲁科版 (2019)选择性必修3第2节 醇和酚教学ppt课件,文件包含新教材精创221醇概述醇的化学性质课件鲁科版选择性必修3共23页PPTpptx、新教材精创221醇概述醇的化学性质教学设计鲁科版选择性必修3docx、新教材精创221醇概述醇的化学性质学案鲁科版选择性必修3docx等3份课件配套教学资源,其中PPT共23页, 欢迎下载使用。










