

所属成套资源:2025安康高二上学期10月月考试题及答案(九科)
2025安康高二上学期10月月考化学试题无答案
展开
这是一份2025安康高二上学期10月月考化学试题无答案,共10页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
命题人:牟宁考试时长:75分钟 满分:100分
可能用到的相对原子质量:
一、选择题(本题共16小题,每小题3分,共48分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1.化学与生活、工农业生产息息相关,下列说法正确的是( )。
A.洁厕灵和食醋是家庭中常见的两种生活用品,食醋比洁厕灵的酸性强
B.增大空气的进入量,可以减少汽车尾气中由于不完全燃烧排放的氮氧化物
C.在冰醋酸中加水制成食醋的过程中,pH随加水量的增大而增大
D.利用反应制氢,相同时间内,使用纳米(催化剂)比微米产率更高
2.下列叙述中一定能判断某化学平衡发生移动的是( )。
A.混合物中各组分的浓度改变B.正、逆反应速率改变
C.混合物中各组分的含量改变D.混合体系的压强发生改变
3.下列说法中不正确的是( )。
A.已知Sn(s,灰锡)(s,白锡) ,则灰锡更稳定,且常温常压下为灰锡状态
B.只有活化分子之间发生的碰撞才可能是有效碰撞
C.升高温度,使单位体积内活化分子数增多,因而反应速率加快
D.对于且一定条件下能自发进行的化学反应,其
4.为阿伏加德罗常数的值,下列说法正确的是( )。
A.和的混合气体中所含氮原子数为
B.熔融的中含有个阳离子
C.和于密闭容器中充分反应,生成HI分子为
D.常温下,的磷酸溶液中数目为
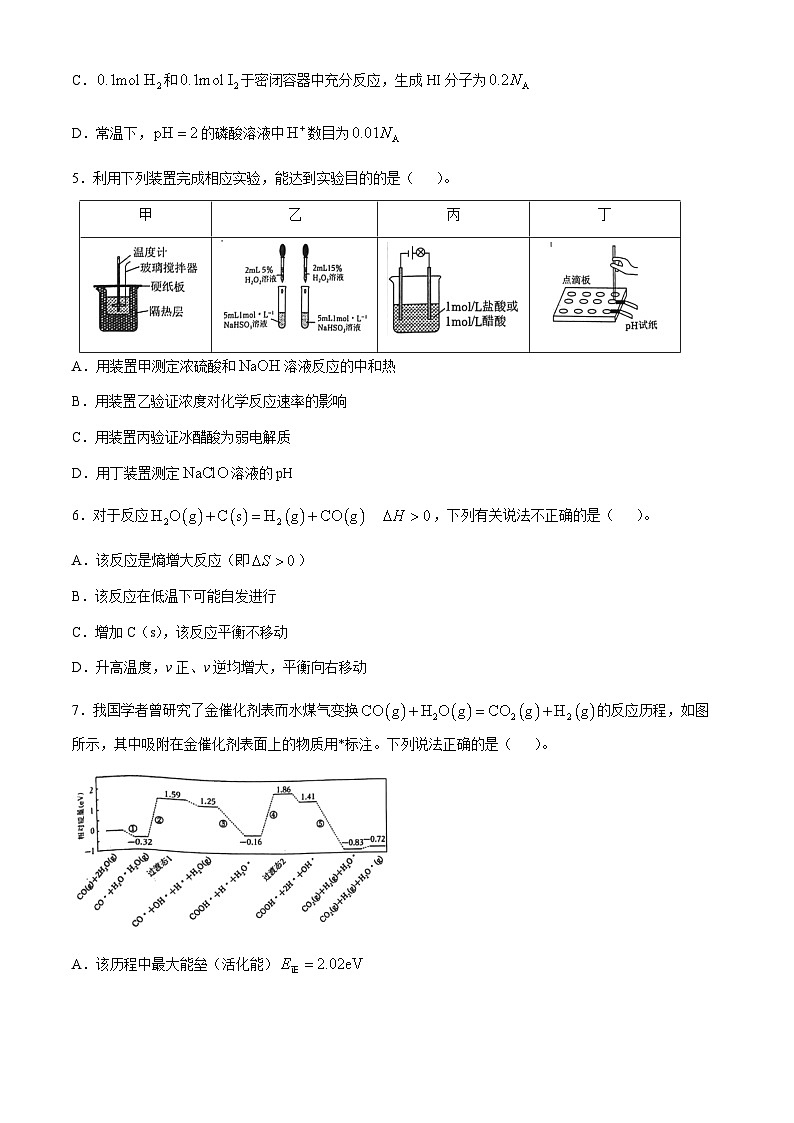
5.利用下列装置完成相应实验,能达到实验目的的是( )。
A.用装置甲测定浓硫酸和溶液反应的中和热
B.用装置乙验证浓度对化学反应速率的影响
C.用装置丙验证冰醋酸为弱电解质
D.用丁装置测定溶液的pH
6.对于反应 ,下列有关说法不正确的是( )。
A.该反应是熵增大反应(即)
B.该反应在低温下可能自发进行
C.增加C(s),该反应平衡不移动
D.升高温度,v正、v逆均增大,平衡向右移动
7.我国学者曾研究了金催化剂表而水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物质用*标注。下列说法正确的是( )。
A.该历程中最大能垒(活化能)
B.步骤①:
C.步骤③的化学方程式为
D.步骤⑤只有极性键H—O的形成
8.下列离子方程式书写正确的是( )。
A.溶液中加入浓盐酸:
B.硫氰化铁溶液中加溶液产生沉淀:
C.用白醋浸泡过的淀粉—KI试纸在空气中放置一段时间后,溶液呈蓝色:
D.向溶液中通入过量:[已知:的,;的,]
9.化学社的同学在做探究实验时,将未经砂布打磨的铝条放入盛有一定量稀盐酸的密闭容器中,用压强传感器测得容器内气体压强和反应时间的变化曲线如图所示,下列分析中正确的是( )。
A.AB段的化学反应是:
B.A点盐酸浓度最低,C点盐酸浓度最高
C.CD段压强变化的主要影响因素是气体温度
D.DE段反应处于动态平衡状态,反应并未停止
10.下列各组离子在指定溶液中一定能大量共存的是( )。
A.加水后值会变大的溶液中:、、、
B.能使pH试纸变深蓝色的溶液:、、、
C.由水电离出的的溶液中:、、、
D.的溶液中:、、、
11.已知常温下的电离平衡常数,;的电离平衡常数,。下列说法不正确的是( )。
A.稀释溶液,减小
B.酸性:
C.用溶液吸收,当溶液呈中性时,
D.的溶液,加水稀释到500倍,则稀释后与的比值为
12.在某一恒容容器中发生反应: 。当反应达到平衡时,、、、改变某一条件,反应速率与反应时间的曲线关系如图。下列说法错误的是( )。
A.时刻,改变的条件可能是适当降低温度 B.时可能增大了反应物活化分子百分数
C.时刻,改变的条件一定是催化剂 D.的体积分数最高的时间段是
13.某温度下,等体积、相同的盐酸和醋酸溶液分别加水稀释,溶液中的随溶液体积变化的曲线如图所示。据图判断下列说法正确的是( )。
A.曲线Ⅱ表示的是盐酸的变化曲线
B.取等体积的a点、b点对应的溶液,消耗的的物质的量相同
C.b点溶液的导电性比c点溶液的导电性强
D.分别加入足量的锌粉充分反应后,两溶液中产生的一样多
14.下列有关图像分析和说法正确的是( )。
A.图甲表示合成氨反应在恒温恒容下进行的速率-时间图,Ⅰ、Ⅱ两过程达到平衡时,的体积分数:Ⅰ<Ⅱ
B.图乙表示 ,在恒温恒容条件下,按投入NO和CO的混合气体建立平衡的过程,当CO与NO的转化率为时,无法说明反应已达到平衡
C.图丙表示在不同温度下平衡时的体积分数-压强图,则气体密度:A点>C点
D.图丁表示不同温度下水溶液中与的关系,a点和d点,溶液都呈中性
15.常温下某同学将一定量的充入注射器中后封口,测得拉伸和压缩注射器的活塞过程中气体透光率随时间的变化如图所示(已知气体颜色越深,透光率越小; )。下列说法正确的是( )。
A.b点操作为压缩针管,因此:b>d B.d点的操作为拉伸注射器到任意位置
C.e点平均相对分子质量与a点相等 D.若注射器绝热,
16.在3个初始温度相同的密闭容器中发生反应: 。3个容器内反应的相关信息如下表所示。下列说法正确的是( )。
A.,
B.平衡时,Ⅰ容器中的小于Ⅱ容器中的
C.无法比较Ⅰ与Ⅱ容器中平衡时压强的大小
D.若起始时向容器Ⅰ中充入、和,则反应将向正反应方向进行
二、非选择题(本题共4小题,共52分)
17.(15分)按要求回答下列问题
(1)以下是生产、生活中常见的物质:①冰醋酸;②;③;④盐酸;⑤;⑥熔融;⑦石墨;⑧酒精;⑨;⑩。属于强电解质的有__________(用序号填空),将①、④分别配制成等pH的溶液,分别取等体积溶液于A、B试管中,分别加入足量且等量的锌粉,产生氢气更多的是__________(填“A”或“B”)。
(2)次磷酸是一种精细化工产品,向溶液中加入等物质的量浓度的溶液后,所得的溶液中只有和两种阴离子。已知常温下,,磷酸的各级电离平衡常数为,,。
①由此分析,次磷酸是__________元酸,写出次磷酸的电离方程式__________。
②溶液加水稀释过程中,的数值__________(填“变大”“变小”或“不变”)。
③常温下,向一定浓度的溶液中加入足量溶液,写出离子反应方程式:__________。
(3)酸碱质子理论认为,在反应过程中凡能给出质子的分子或离子都是酸,凡能接受质子的分子或离子都是碱。例如,,。已知几种酸在醋酸中的电离常数如表所示:
①上表中四种酸在醋酸中的酸性最弱的是__________(填化学式)。
②在液态中表现__________性(填“酸”“碱”或“中”)。
(4)已知:,,常温下,的溶液其。则的溶液中HA的电离度__________。
18.(14分)根据已有知识,回答下列问题。
(1)浓度均为的和混合溶液中,__________。
(2)可向氯水中加入__________(填序号)增强漂白性。已知各酸电离平衡常数如表
① ② ③石灰乳 ④ ⑤ ⑥
⑦ ⑧ ⑨
(3)将足量固体置于真空恒容容器中,发生反应。反应达平衡时体系总压为。保持温度不变,开始时在体系中先通入一定量,再加入足量,欲使平衡时体系中水蒸气的分压小于,的初始压强应大于__________kPa。
(4)将常温下溶液加热(不考虑挥发),pH__________(填“升高”“降低”或“不变”),若改成加热溶液,pH__________(填“升高”“降低”或“不变”)。
(5)95℃下,,若100体积的某强酸溶液与1体积的某强碱溶液混合后溶液,则__________。
(6)常温下,溶液和溶液混合,恰好完全沉淀,溶液,则__________。
19.(13分)滴定实验是化学学科中重要的定量实验。
Ⅰ.酸碱中和滴定——已知某试样中含有杂质,为测定试样中的质量分数,进行如下步骤实验:
①称量样品溶于水,配成溶液;
②准确量取所配溶液于锥形瓶中;
③滴加几滴甲基橙指示剂;
④用的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
(1)该酸碱中和滴定(题干中②③④步)所需仪器有__________(填字母)。
A.酸式滴定管 B.碱式滴定管 C.量筒
D.铁架台E.滴定管夹F.玻璃棒
(2)排去碱式滴定管中气泡的方法应采用__________操作(填“甲”“乙”或“丙”)。
(3)滴定达到终点的现象是__________。
(4)试样中的质量分数为__________。
(5)若出现下列情况,测定结果偏高的是__________。
a.滴定前用蒸馏水冲洗锥形瓶
b.酸式滴定管滴至终点时,俯视读数
c.酸式滴定管用蒸馏水洗后,未用标准液润洗
d.酸式滴定管尖嘴部分有气泡,滴定后消失
Ⅱ.氧化还原滴定——取草酸(,弱酸)溶液置于锥形瓶中,加入适量稀硫酸,用浓度为的高锰酸钾溶液滴定。
(6)发生反应的离子方程式为:__________。
(7)滴定时,溶液应装在酸式滴定管中,滴定终点时锥形瓶内的颜色变化为:由__________。
20.(10分)世界卫生组织国际癌症研究机构公布的致癌物清单中,一碘甲烷属于三类致癌物。用化学反应原理研究一碘甲烷具有重要意义,一碘甲烷热裂解时主要发生如下反应。回答下列有关问题:
反应Ⅰ:
反应Ⅱ:(丁烯)
反应Ⅲ:
(1)几种化学键的键能数据如表所示:
则反应Ⅱ的__________,若反应Ⅰ正反应活化能为,则逆反应活化能为__________(用含a的代数式表示)。
(2)在恒容密闭容器中投入,实验测得平衡体系中、HI和的物质的量分数与反应温度的关系如图所示:
①随着体系温度升高,HI的物质的量分数先增大后减小的原因可能是__________。
②条件下,的平衡转化率为__________,若起始压强为,则反应Ⅱ的标准平衡常数__________(已知:分压=总压×该组分的物质的量分数,对反应,,其中,、、、为各组分的平衡分压)。甲
乙
丙
丁
容器编号
容器类型
初始体积
起始物质的量/ml
平衡时物质的量/ml
Ⅰ
恒温恒容
2
1
0
1.6
Ⅱ
绝热恒容
2
1
0
a
Ⅲ
恒温恒压
0
0
4
b
酸
5.8
8.2
8.8
9.4
酸
滴定序号
待测液体积(mL)
消耗盐酸标准的体积(mL)
滴定前
滴定后
1
25.00
0.50
20.60
2
25.00
6.00
26.00
3
25.00
1.10
21.00
化学键
C—H
C=C
C—C
键能/
413
612
348
相关试卷
这是一份2025沧州泊头一中高二上学期10月月考化学试题无答案,共8页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。
这是一份陕西省安康市2024-2025学年高二上学期10月月考化学试题(无答案),共10页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份安徽省绩溪中学2024-2025学年高二上学期10月月考化学试题(无答案),共9页。试卷主要包含了11-10,下列说法正确的是,在一密闭容器中进行反应,根据体系的能量循环图,某化学反应分两步进行,已知等内容,欢迎下载使用。









