

【高考化学】11个题型突破高考化学实验题 题型03 物质的分离、提纯与检验(原卷版)
展开
这是一份【高考化学】11个题型突破高考化学实验题 题型03 物质的分离、提纯与检验(原卷版),共12页。试卷主要包含了苯甲酸是一种常用的食品防腐剂,1-丁醇等内容,欢迎下载使用。
题型03 物质的分离、提纯与检验
在近几年的高考中,常会以化学实验室常用仪器的主要用途及使用方法、化学品安全使用作为考查点口进行考查,涉及实验室物品的分类、安全保存、废弃物的处理方法及突发事件的处理措施等。
1、(2023·辽宁卷)下列鉴别或检验不能达到实验目的的是
A.用石灰水鉴别Na2CO3与NaHCO3
B.用KSCN溶液检验FeSO4是否变质
C.用盐酸酸化的BaCl2溶液检验Na2SO3是否被氧化
D.加热条件下用银氨溶液检验乙醇中是否混有乙醛
2、(2023·浙江卷)苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下:
下列说法不正确的是
A.操作I中依据苯甲酸的溶解度估算加水量
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.操作Ⅲ缓慢冷却结晶可减少杂质被包裹
D.操作IV可用冷水洗涤晶体
3、(2022·海南卷)《医学入门》中记载我国传统中医提纯铜绿的方法:“水洗净,细研水飞,去石澄清,慢火熬干”,其中未涉及的操作是( )
A.洗涤 B.粉碎 C.萃取 D.蒸发
4、(2022·山东卷)已知苯胺(液体)、苯甲酸(固体)微溶于水,苯胺盐酸盐易溶于水。实验室初步分离甲苯、苯胺、苯甲酸混合溶液的流程如下。下列说法正确的是( )
A.苯胺既可与盐酸也可与NaOH溶液反应
B.由①、③分别获取相应粗品时可采用相同的操作方法
C.苯胺、甲苯、苯甲酸粗品依次由①、②、③获得
D.①、②、③均为两相混合体系
5、(2021·湖南卷)1-丁醇、溴化钠和70%的硫酸共热反应,经过回流、蒸馏、萃取分液制得1-溴丁烷粗产品,装置如图所示:
已知:CH3(CH2)3OH+NaBr+H2SO4△ CH3(CH2)3Br+NaHSO4+H2O
下列说法不正确的是( )
A.装置Ⅰ中回流的目的是减少物质的挥发,提高产率
B.装置Ⅱ中a为出水口,b为进水口
C.用装置Ⅲ萃取分液时,将分层的液体依次从下口放出
D.经装置Ⅲ得到的粗产品干燥后,使用装置Ⅱ再次蒸馏,可得到更纯的产品
6、(2020·全国Ⅰ卷)下列气体去除杂质的方法中,不能实现目的的是( )
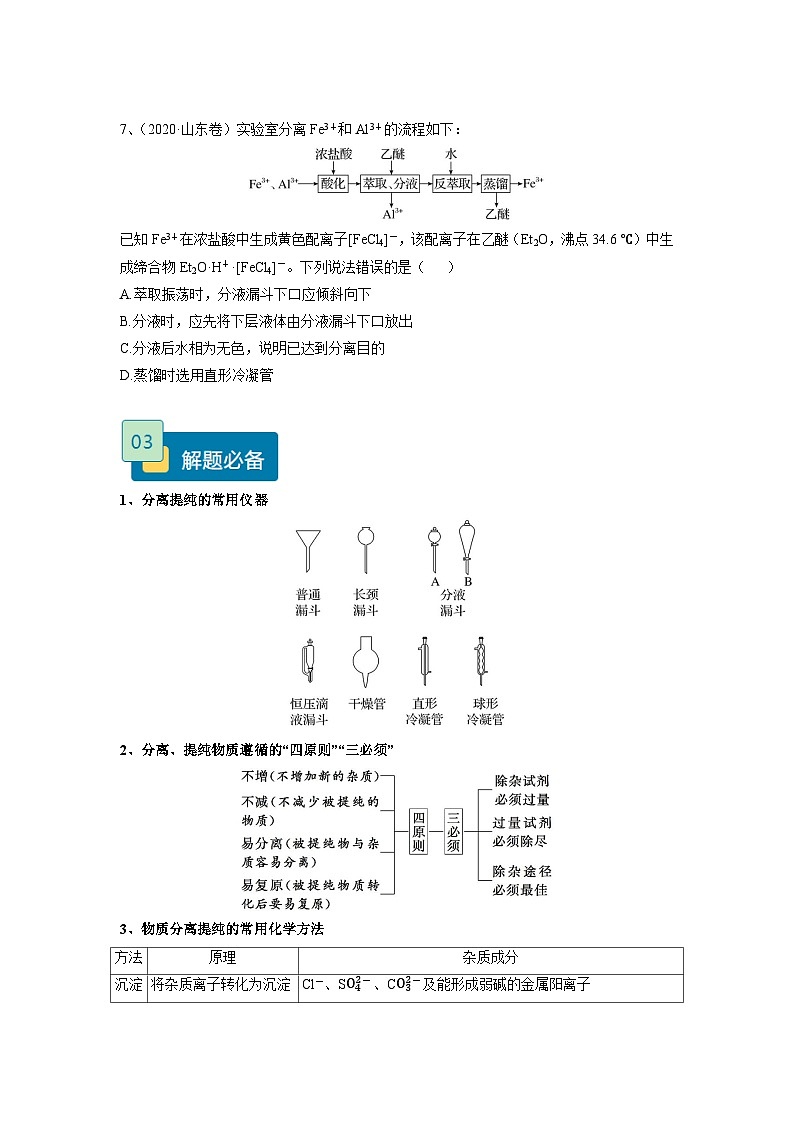
7、(2020·山东卷)实验室分离Fe3+和Al3+的流程如下:
已知Fe3+在浓盐酸中生成黄色配离子[FeCl4]-,该配离子在乙醚(Et2O,沸点34.6 ℃)中生成缔合物Et2O·H+·[FeCl4]-。下列说法错误的是( )
A.萃取振荡时,分液漏斗下口应倾斜向下
B.分液时,应先将下层液体由分液漏斗下口放出
C.分液后水相为无色,说明已达到分离目的
D.蒸馏时选用直形冷凝管
1、分离提纯的常用仪器
2、分离、提纯物质遵循的“四原则”“三必须”
3、物质分离提纯的常用化学方法
4、物质的分离除杂示例
5、气体混合物的分离与提纯
(1)流程分析
(2)除杂方法
6、液体混合物的分离与提纯
7、固体混合物的分离与提纯
明确分离目的 分析溶质或固体杂质的溶解度或性质 确定分离提纯方法
1、(2023上·福建漳州·高三福建省漳州第一中学期中)下列实验中,所采取的分离方法与对应原理都正确的是
2、(2023·四川绵阳·统考一模)实验室用化学沉淀法除去粗盐中的Ca2+、Mg2+、获得精制盐。下列叙述有误的是
A.杂质离子除去顺序可确定为:SO、Mg2+、Ca2+
B.加入试剂顺序可依次为:NaOH、Na2CO3、BaCl2、盐酸四种溶液
C.杂质离子沉淀完后,采取的分离操作用到的仪器是a、b、c、d
D.沉淀分离完成后,调整溶液pH时用到的全部仪器为a、c、e、f
3、(2023上·福建福州·高三福建省罗源第一中学校联考期中)下列物质的分离方法正确的是
A.装置A可用于分离汽油和水的混合物
B.装置B可用于四氯化碳提取溴水中的溴
C.装置C可用于灼烧胆矾,制备无水硫酸铜
D.装置D可用于分离丁醇(沸点117.5℃)与甲苯(沸点110.6℃)
4、(2024上·广东深圳·高三红岭中学校考期中)为除去括号内的杂质,所选用的试剂或方法错误的是
A.MnO2粉末(KCl),溶于水,过滤
B.CO2气体(HCl),饱和Na2CO3溶液
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.氢氧化铁胶体(沙粒),过滤
5、(2023·河北·模拟)卤水中含有较多的碘元素(以形式存在),一种利用高分子吸附树脂吸附来提取卤水中碘元素的工艺流程如下。
下列说法错误的是
A.步骤①到④的目的是将碘富集
B.将步骤⑤中换成,产量会更高
C.步骤⑥过滤后最好使用酒精洗涤
D.得到的粗碘可通过如图装置进行纯化
6、(2023·重庆·统考三模)下列实验中采取的分离或提纯方法能达到实验目的的是
7、(2023·山东·济南一中校联考三模)实验室利用醋酸()与双氧水()在固体酸的催化下共热制备过氧乙酸(,沸点)。实验过程中,逐滴滴入浓度为的双氧水,温度维持在,待反应结束后分离反应器中的混合物,得到粗产品。下列说法错误的是
A.逐滴滴入的目的是提高双氧水的利用率
B.温度维持在的理由之一是防止分解
C.使用磁力搅拌器的目的是为了提高平衡产率
D.常压蒸馏可以分离提纯
8、(2023·江西·江西师大附中校联考模拟)近日,天津大学钟澄团队制备锌镍电池的负极材料——,流程如下,已知:离心分离是借助于离心力,使比重不同的物质进行分离的方法,下列叙述错误的是
A.“反应池1”中发生的离子反应为
B.“反应池1”和“反应池2”可通过搅拌加快反应
C.“加热”时选择蒸发皿盛放ZnO和BiOI固体
D.“操作1”可以为离心分离,用于分离固体和液体混合物
9、(2023·广东广州·统考三模)菠菜是一道平民小菜,价格便宜却营养丰富,菠菜中铁元素的检验可经过“研磨→溶解→过滤→检验”等步骤。下列操作方法不正确的是
A.A B.B C.C D.D
10、(2023上·江苏泰州·高三统考期中)某化学兴趣小组拟探究碳与浓反应,并检验气体产物。下列说法正确的是
A.用装置甲进行碳与浓反应
B.将检验过后的气体再通入装置丁中检验产物
C.将反应产生的气体通入装置丙,可直接检验产物
D.将反应产生的气体通入装置乙,可直接检验产物
11、(2023上·辽宁丹东·高三统考期中)下列除杂试剂、除杂方法和除杂装置均正确的是
12、(2023上·福建漳州·高三校联考期中)实验室按以下方案从某海洋动物提取抗肿瘤活性的天然产物(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶;甲苯的密度比水小;溶液为低浓度溶液)。
下列说法错误的是
A.步骤(1)需要用到的玻璃仪器有漏斗、玻璃棒、烧杯
B.步骤(2)分液时水层从分液漏斗上口倒出
C.步骤(3)主要过程有蒸发结晶、趁热过滤
D.步骤(4)可利用物质的沸点不同分离
13、(2023上·湖北·高三校联考)下列物质分离提纯的方法错误的是
A.分液用装置④,萃取振荡时,分液漏斗下口应倾斜向下
B.分离乙二醇(沸点为)和乙酸(沸点为)选择装置③
C.提纯含不溶性杂质的粗苯甲酸要用装置①②
D.用装置①除去氢氧化铁胶体中的沉淀物
14、(2023上·福建福州·高三福建省罗源第一中学校联考期中)除去下列物质中的杂质(括号内为杂质),选用试剂及操作方法均正确的一组是
15、(2023上·浙江金华·高三校联考)实验室合成并提纯山梨酸乙酯(密度,沸点195.5℃)的过程如下图所示。下列说法正确的是
A.操作①控温110℃,目的是除去生成的水
B.操作③可以通过观察气泡现象控制试剂a的用量
C.操作③④均应收集下层液体
D.操作②⑤可用玻璃棒轻轻拨散固体,以加快过滤速率
选项
气体(杂质)
方法
A
SO2(H2S)
通过酸性高锰酸钾溶液
B
Cl2(HCl)
通过饱和的食盐水
C
N2(O2)
通过灼热的铜丝网
D
NO(NO2)
通过氢氧化钠溶液
方法
原理
杂质成分
沉淀法
将杂质离子转化为沉淀
Cl-、SO42-、CO32-及能形成弱碱的金属阳离子
气化法
将杂质离子转化为气体
CO32-、HCO3-、SO32-、HSO3-、S2-、NH4+等
杂转纯法
将杂质转化为需要提纯的物质
杂质中含不同价态的相同元素(用氧化剂或还原剂)、同一种酸的正盐与酸式盐(用对应的酸或碱)
氧化还原法
用氧化剂(或还原剂)除去具有还原性(或氧化性)的杂质
如用酸性KMnO4溶液除去CO2中的SO2,用灼热的铜网除去N2中的O2
热分解法
加热使不稳定的物质分解除去
如除去NaCl中的NH4Cl等
酸碱溶解法
利用物质与酸或碱溶液反应的差异进行分离
如用过量的NaOH溶液可除去Fe2O3中的Al2O3
调pH法
加入试剂调节溶液pH,使溶液中某种成分生成沉淀而分离
如向含有Cu2+和Fe3+的溶液中加入CuO、Cu(OH)2或Cu2(OH)2CO3等,调节pH使Fe3+转化为Fe(OH)3沉淀而除去
吸收法
常用于气体的净化和干燥,可根据被提纯气体中所含杂质气体的性质,选择适当固体或溶液作吸收剂,常用的实验装置是洗气瓶或干燥管
CO2中混有HCl气体可通过饱和NaHCO3溶液除去
序号
原物质
所含杂质
除杂质试剂
主要操作方法
①
N2
O2
灼热的铜网
固体吸收气体
②
CO
CO2
NaOH溶液或碱石灰
洗气或固体吸收气体
③
CO2
CO
灼热的CuO
用固体转化气体
④
CO2
HCl
饱和NaHCO3溶液
洗气
⑤
Cl2
HCl
饱和食盐水
洗气
⑥
碳粉
CuO
稀盐酸
过滤
⑦
Fe2O3
Al2O3
过量NaOH溶液
过滤
⑧
NaHCO3溶液
Na2CO3
CO2
加酸转化
⑨
FeCl3溶液
FeCl2
Cl2
加氧化剂转化
⑩
FeCl2溶液
FeCl3
Fe
加还原剂转化
⑪
MgCl2溶液
FeCl3
MgO
过滤
⑫
NaCl晶体
NH4Cl
加热分解
⑬
乙酸乙酯
乙酸
饱和Na2CO3溶液
分液
方法
仪器简图
说明
洗气法
气体流向:长“进”短“出”。例如除去CO2中SO2的方法:将混合气体通入盛有饱和NaHCO3溶液或酸性KMnO4溶液的洗气瓶
加热法
利用气体与固体物质反应,除去气体中的某种杂质。例如硬质玻璃管中盛放铜网,在加热时可以除去N2中的O2
冷凝法
利用物质的沸点不同使杂质气体液化或凝华而除去。例如除去SO2气体中的SO3蒸气等
干燥法
(1)球形干燥管、U形干燥管中盛放颗粒状干燥剂。注意颗粒状干燥剂的颗粒太小容易堵塞干燥管管口,颗粒太大气体杂质不容易被除尽。若要盛放粉末状干燥剂,则应该附着在石棉绒上。
(2)常用的干燥剂碱石灰的主要成分为氧化钙与氢氧化钠,碱石灰可除去杂质CO2、H2O、Cl2等。
(3)无水氯化钙不能干燥氨气,浓硫酸不能干燥NO2、H2S、HBr等。
(4)球形干燥管:气体应从大口进小口出
选项
目的
分离方法
原理
A
除去中的
蒸发结晶
溶解度不同
B
除去固体碘中的
加热、升华
的熔点高,碘易升华
C
分离淀粉溶液和溶液
过滤
分散质粒子的大小不同
D
分离汽油和柴油
分液
汽油和柴油的密度不同
选项
实验目的
分离或提纯方法
A
分离碘的四氯化碳溶液中的碘
用苯萃取
B
除去乙酸乙酯中的乙酸
加入饱和溶液后分液
C
除去蛋白质溶液中少量NaCl
过滤
D
从高级脂肪酸钠和甘油的混合水溶液中分离出高级脂肪酸钠
加入乙醇和浓硫酸并加热,然后蒸馏
A.研磨
B.溶解
C.过滤
D.检验
被提纯的物质(杂质)
Cl2(HCl)
Fe(I2)
Na2CO3固体(NaHCO3)
Al(OH)3胶体(AlCl3)
方法
洗气
升华
加热
渗析
除杂试剂及装置
选项
A
B
C
D
选项
待提纯的物质
选用的试剂
操作的方法
A
CO2(HCl)
氢氧化钠溶液
洗气
B
Cu(Fe)
稀盐酸
溶解、过滤、洗涤、干燥
C
FeSO4(H2SO4)
氢氧化钠溶液
过滤
D
N2(CO)
氧气
点燃
相关试卷
这是一份【高考化学】11个题型突破高考化学实验题 题型04 常见气体的制备原理与装置选用(原卷版),共15页。试卷主要包含了SO2等内容,欢迎下载使用。
这是一份【高考化学】11个题型突破高考化学实验题 题型02 实验操作与装置的正误判断(原卷版),共11页。试卷主要包含了下列装置可以用于相应实验的是,下列说法正确的是等内容,欢迎下载使用。
这是一份【高考化学】11个题型突破高考化学实验题 题型01 常用仪器的使用、药品保存和实验安全(原卷),共13页。试卷主要包含了实验室将粗盐提纯并配制的溶液,名称为“吸滤瓶”的仪器是,下列试剂实验室保存方法错误的是,下列说法不正确的是,关于下列仪器使用的说法错误的是,下列图示表示灼烧操作的是等内容,欢迎下载使用。









