





所属成套资源:2023-2024学年高一下学期化学人教版(2019)必修第二册
- 7.2.2 烃 课件 2023-2024学年高一下学期化学人教版(2019)必修第二册 课件 0 次下载
- 7.2.3高分子材料 课件 2023-2024学年高一下学期化学人教版(2019)必修第二册 课件 0 次下载
- 7.3.2乙醇和乙酸第二课时 乙酸 课件 2023-2024学年高一下学期化学人教版(2019)必修第二册 课件 0 次下载
- 7.4.1基本营养物质第一课时 糖类 课件 2023-2024学年高一下学期化学人教版(2019)必修第二册 课件 0 次下载
- 7.4.2基本营养物质 第二课时 蛋白质和油脂 课件 2023-2024学年高一下学期化学人教版(2019)必修第二册 课件 0 次下载
高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸一等奖ppt课件
展开
这是一份高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸一等奖ppt课件,共46页。PPT课件主要包含了烃的衍生物,官能团,常见官能团,乙醇的结构,乙醇的物理性质,思考与讨论,针对练习,乙醇的化学性质,醇催化氧化机理,补充乙醛等内容,欢迎下载使用。
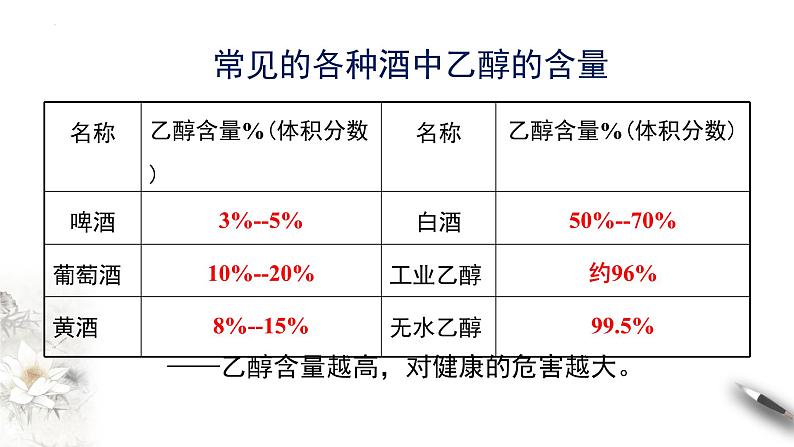
常见的各种酒中乙醇的含量
——乙醇含量越高,对健康的危害越大。
第七章 有机化合物第三节 乙醇和乙酸第一课时 乙醇
C2H6、CH3CH=CH2、CH3Cl、C6H6、 CH3CH2OH、CH3COOH
1.定义:烃分子中的________被其他原子或原子团所取代而生成的一系列化合物。
2.示例:CH3Cl可以看做是CH4中的一个氢原子被氯原子取代生成的;
CH3OH可以看做是CH4中的一个氢原子被—OH取代生成的。
C + 其他元素 [H 、N、 P、 O、 S 、 X(F、 Cl、 Br、 I )等等]组成的有机化合物
烃的衍生物制取途径较多,不但可由取代反应制得,也可由加成反应等制得,
(1)烃的衍生物是否只能由取代反应制得?
(2)卤代烃是否属于烃?
卤代烃(如CH3Cl、CCl4、CH2=CHCl等)不属于烃,
如氯乙烷可由乙烷和氯气发生取代反应制得,也可由乙烯和氯化氢发生加成反应制得。
因为烃中只含碳、氢两种元素,而卤代烃中还有卤素。
烷烃易取代,烯烃易加成。
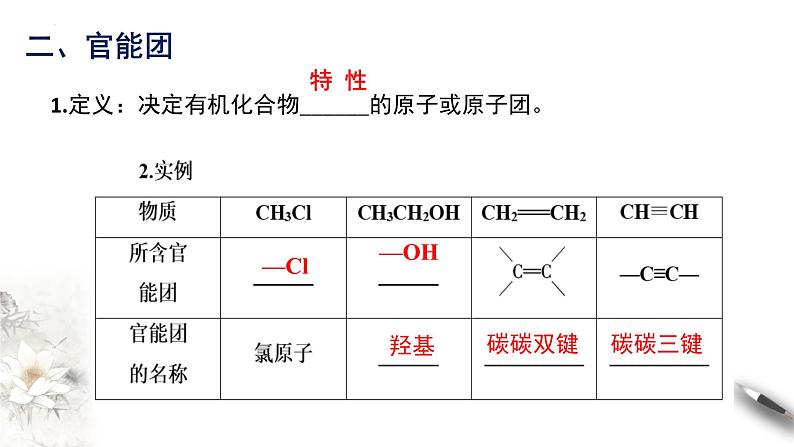
1.定义:决定有机化合物______的原子或原子团。
稳定离子稳定存在溶液中
不稳定不能独立存在,必须和其他基团或原子结合
羟基(—OH)与氢氧根(OH-)一样吗?
1.定义:烃分子失去1个H原子后所剩余的部分。
如—CH3叫______,—CH2CH3叫______。
2.烃的衍生物一般可以看成是由烃基和官能团相互结合组成的。
如乙醇分子可看成由______和______组成的。
酒的历史悠久,早在几千年前,人类就掌握了发酵法酿酒的技术。
你能想起哪些含有酒的诗句?
能溶解多种有机物和无机物
与水形成分子间氢键,增大水溶性
乙醇是良好的有机溶剂,不可萃取水中溶质
2.如何只用一种试剂鉴别乙醇、苯和CCl4?
1.如何分离水和酒精?
由于水和酒精是互溶的,所以通常用蒸馏的方法分离水和酒精。
3.如何由工业乙醇制取无水乙醇?(除去乙醇中的水)
在工业酒精中加入生石灰(CaO),生石灰与水反应生成氢氧化钙,再加热蒸馏,即可得到无水乙醇。
4.无水乙醇真的不含水吗?如何检验无水乙醇中是否含有水?
加白色的无水CuSO4,若无水CuSO4变蓝,则证明无水乙醇中含有水;
2.乙醇的分子式:C2H6O,结构简式:CH3CH2OH,分子中的6个氢原子是否完全相同?
3.比较乙烷与乙醇的结构,下列说法不正确的是( )A.两个碳原子都与单键相连B.分子里都含有6个相同的氢原子C.CH3CH2-与1个氢原子相连就是乙烷分子D.CH3CH2-与1个羟基相连就是乙醇分子
官能团:羟基(-OH)
乙醇分子是由乙基(—C2H5)和羟基(—OH)组成的,羟基比较活泼,它决定着乙醇的主要性质。
在后面的化学性质中要注意是在哪里断键的。
乙醇的化学性质较活泼,分子中的C-O键、O-H键和C-H键都有断键的可能。
实验7-4:乙醇与钠的反应
实验7-4:乙醇与钠反应
①钠开始沉于试管底部,最终慢慢消失,产生无色可燃性气体,火焰呈淡蓝色;
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
金属钠置换了乙醇中羟基上的氢,生成氢气和乙醇钠
②烧杯内壁有水珠产生;
③向烧杯中加入澄清石灰水不变浑浊
钠与水、乙醇反应的比较
钠沉于试管底部,未熔化,慢慢消失
注意:ρ水>ρ钠 > ρ乙醇
2Na+2H2O=2NaOH+H2↑
2Na+2CH3CH2OH→2CH3CH2ONa+H2↑
思考:为什么乙醇与钠反应不如钠与水反应剧烈?
2Na+2H-O-H = 2NaOH+H2↑
钠与水的反应更剧烈,说明水分子中的氢原子比乙醇羟基中的氢原子更活泼。
1、置换反应(乙醇与钠反应)
与活泼金属(K、Ca、Na、Mg、Al等)反应置换羟基上的H生成H2。
2CH3CH2OH +2Na → 2CH3CH2ONa + H2↑
2-OH ~ 2Na ~ 1H2
思考:多少ml乙醇与Na反应才能产生1ml H2?
2 ml乙醇与足量的Na反应得到1ml H2
7.能证明乙醇分子中含有一个羟基的事实是 ( )A. 乙醇容易挥发B. 乙醇能与水以任意比例互溶C. 乙醇完全燃烧生成CO2和H2OD. 0.1 ml乙醇与足量Na反应生成 0.05 ml H2
A.6∶3∶2 B.1∶2∶3C.3∶2∶1D.4∶3∶2
产生淡蓝色火焰,放出大量的热。
实验7-5:乙醇的催化氧化
变红色,闻到刺激性气味
乙醇在加热和催化剂(Cu或Ag)存在的条件下,被空气中的氧气氧化成乙醛。
☞ 有机反应中:有机物“去氢”或“得氧”的反应称为氧化反应;有机物“加氢”或“去氧”的反应称为还原反应。
①与-OH相连的C上有2个H,氧化成醛。
②与-OH相连的C上有1个H,氧化成酮。
③与-OH相连的C上没有H,不能催化氧化。
连接-OH官能团的碳原子上必须有H,醇才能发生催化氧化。
②-C原子上有一个H,醇被氧化成酮
①-C原子上有两个H,醇被氧化成醛
11.下列各醇,能发生催化氧化的是( )
1.乙醇的结构特点、断键与性质的关系
断①②③④⑤键(所有化学键)
2.乙醇催化氧化反应的实质
总的化学方程式:2CH3CH2OH+O2 2CH3CHO+2H2O,
反应中铜(也可用银)作催化剂。
在适当的条件下,乙醛可以继续被O2氧化,最终生成乙酸。
无色液体,有刺激性气味,能跟水、乙醇、乙醚、氯仿等互溶。
K2Cr2O7 Cr3+ 重铬酸钾(橙色) 三价铬离子 (绿色)
高锰酸钾(紫色) 锰离子(无色)
15.酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是( )①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物A.②④ B.②③ C.①③ D.①④
★条件控制在有机反应中的作用
2.是重要的有机化工原料和溶剂,用于生产医药、香料、化妆品、涂料等。
3.医疗上常用体积分数为75%的乙醇溶液作消毒剂。
并非乙醇的浓度越大,消毒效果越好
高温焊接银器或铜器时,表面会生成黑色的氧化物,师傅说:把铜、银器具趁热蘸一下酒精,铜、银会光亮如初!原理?
1.正误判断(正确的打“√”,错误的打“×”)(1)乙醇是良好的有机溶剂,可以用来萃取溴水中的溴。( )(2)可用无水硫酸铜检验工业酒精中是否有水。( )(3)乙醇中的羟基不如水中的羟基活泼。( )(4)乙醇分子中含有六个氢原子,故1 ml乙醇与足量的钠反应可以生成3 ml的氢气。( )
相关课件
这是一份人教版 (2019)必修 第二册第三节 乙醇与乙酸获奖课件ppt,文件包含新人教版必修2化学73《乙醇和乙酸》第二课时课件pptx、73第三节乙醇和乙酸第二课时乙酸教案doc等2份课件配套教学资源,其中PPT共29页, 欢迎下载使用。
这是一份人教版 (2019)必修 第二册第三节 乙醇与乙酸完整版课件ppt,文件包含新人教版必修2化学73《乙醇和乙酸》第一课时课件pptx、73乙醇和乙酸第一课时乙醇教案doc等2份课件配套教学资源,其中PPT共30页, 欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第二册实验活动9 乙醇、乙酸的主要性质备课课件ppt,共21页。PPT课件主要包含了分子式,C2H4O2,结构简式,结构式,官能团,乙酸的结构,乙酸的物理性质,NaHCO3,澄清石灰水,探究乙酸的弱酸性等内容,欢迎下载使用。









