
实验活动5 常见金属的物理性质和化学性质(导学案)-2024-2025学年初中化学九年级下册人教版配套教案
展开年级的学生已初步具备了一定的观察问题、分析问题和解决问题的能力,对事物的认识正处于从感性到理性的转变时期,实验是激发他们学习兴趣的最好办法。因此,在实验中,可增强学生的主体意识,改进学生的学习方式,将学习的主动权交给学生,采用实验活动的方式,让学生充分发挥自己的潜能,去探究、交流和思考,从而完成对金属化学性质的认识从具体到抽象、从感性到理性的转变,使学生更直观地掌握金属的物理性质和化学性质。
备课笔记
备课笔记
知识回顾:
物质的物理性质是指不需要通过化学变化表现出来的性质。物理性质主要有:颜色、状态、气味、密度、硬度、熔点、沸点、导电性、挥发性、导热性等。物质的化学性质是指在化学变化中表现出来的性质,主要有:可燃性、还原性、氧化性等。
备课笔记
特别提醒:
用金属与酸反应和与金属化合物的溶液反应时,实验前,应将金属用砂纸打磨除去表面的物质,以免干扰实验。
备课笔记
规律总结:
活泼金属都是正二价时,相同质量完全反应时,产生的氢气质量的多少,跟金属的相对原子质量有关,相对原子质量越小,产生的氢气质量越多。
布置作业:完成本课时对应练习,并提醒学生预习下一节的内容。
备课笔记
课题
常见金属的物理性质和化学性质
课型
新授课
素养目标
1.通过观察、刻画、触摸等方式认识金属的物理性质。
2.初步掌握金属化学性质的实验操作。
3.初步学会运用实验自主探究的方法获得信息。
4.通过让学生设计实验方案去探究金属的导电性,金属的活动性顺序,培养学生的实验设计能力,进一步提高学生动手操作能力和科学探究能力。
5.通过实验探究,让学生参与到知识的形成过程中,从而获得成功的喜悦和对化学学习的兴趣。
6.进一步激发学生乐于探究的情感和发扬互助合作的团队精神。
教学重点
金属的化学性质。
教学难点
实验方案的设计。
教具准备
试管、试管夹、酒精灯、坩埚钳、电池、导线、小灯泡、火柴。
镁条、锌粒、铝片、铁片、铜片、黄铜片(或白铜片)、稀盐酸、稀硫酸、硫酸铜溶液、硝酸银溶液。
课前预习
1.金属的物理性质:大多数金属常温下呈固体(汞是液体),有金属光泽,具有良好的导热性、导电性和延展性。
2.合金比组成它的纯金属的硬度更大、熔点更低、抗腐蚀性更好。
3.在金属活动性顺序里,位于前面的金属能把位于后面的金属从它的化合物溶液中置换出来。
新课导入
同学们,之前我们学习了金属的物理性质和化学性质,可能你们觉得有点抽象,现在我们在实验室,我们可以去探究金属的物理性质和化学性质,从而感受化学实验的乐趣。
进行新课
一 金属的物理性质
活动1 观察金属的颜色和光泽
[布置任务]现在每个实验桌上有镁条、铝片、铁片、铜片,请同学们观察这些金属的颜色和光泽。
现象:
金属
颜色
光泽
镁条
银白色
有金属光泽
铝片
银白色
有金属光泽
铁片
银白色
有金属光泽
铜片
红色
有金属光泽
结论:金属一般都具有金属光泽,多数金属为银白色,铜为红色。
活动2 比较金属的硬度
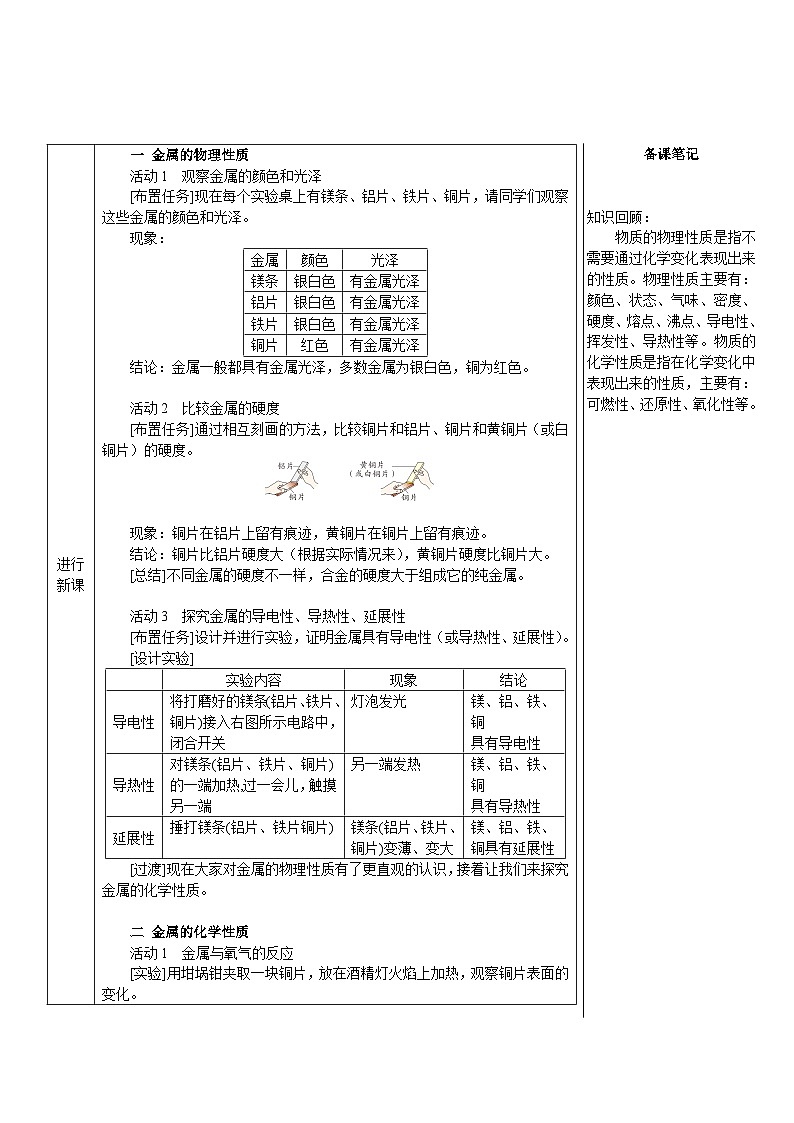
[布置任务]通过相互刻画的方法,比较铜片和铝片、铜片和黄铜片(或白铜片)的硬度。
现象:铜片在铝片上留有痕迹,黄铜片在铜片上留有痕迹。
结论:铜片比铝片硬度大(根据实际情况来),黄铜片硬度比铜片大。
[总结]不同金属的硬度不一样,合金的硬度大于组成它的纯金属。
活动3 探究金属的导电性、导热性、延展性
[布置任务]设计并进行实验,证明金属具有导电性(或导热性、延展性)。
[设计实验]
实验内容
现象
结论
导电性
将打磨好的镁条(铝片、铁片、铜片)接入右图所示电路中,闭合开关
灯泡发光
镁、铝、铁、铜
具有导电性
导热性
对镁条(铝片、铁片、铜片)的一端加热,过一会儿,触摸另一端
另一端发热
镁、铝、铁、铜
具有导热性
延展性
捶打镁条(铝片、铁片铜片)
镁条(铝片、铁片、铜片)变薄、变大
镁、铝、铁、铜具有延展性
[过渡]现在大家对金属的物理性质有了更直观的认识,接着让我们来探究金属的化学性质。
二 金属的化学性质
活动1 金属与氧气的反应
[实验]用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,观察铜片表面的变化。
进行新课
现象:红色的铜片逐渐变黑。
结论:铜与氧气在加热时发生反应,生成黑色的氧化铜,化学方程式为2Cu+O2 △ 2CuO。
活动2 金属与稀盐酸、稀硫酸的反应
[实验](1)向5支试管中分别放入少量镁条、铝片、锌粒、铁片、铜片,然后分别加入5mL稀盐酸(或稀硫酸),观察现象。
现象:盛镁条、铝片、锌粒、铁片的试管中均有气泡产生;盛铜片的试管无现象。
(2)用小试管收集反应产生的气体,验纯后点燃,并在火焰上方罩一冷而干燥的小烧杯。
现象:气体燃烧,发出淡蓝色火焰,烧杯内壁上有水珠生成。
结论:活泼金属镁、铝、铁、锌都能与稀盐酸(或稀硫酸)反应产生氢气;铜不能与稀盐酸(或稀硫酸)反应。
活动3 比较铁、铜、银的金属活动性强弱
[布置任务]设计并进行实验,比较铁、铜、银的金属活动性强弱。
[设计实验]
[总结]金属活动性:Fe>Cu>Ag。
教学板书
实验活动5 常见金属的物理性质和化学性质
金属的物理性质
活动1 观察金属的颜色和光泽。
活动2 比较金属的硬度
活动3 探究金属的导电性、导热性、延展性
金属的化学性质
活动1 金属与氧气的反应
活动2 金属与稀盐酸、稀硫酸的反应
活动3 比较铁、铜、银的金属活动性强弱
课堂小结
本节课旨在通过实验活动,进一步巩固对金属的物理性质和化学性质的认识。同时加深同学们对事物的外在表现和内在性质的认识。提高同学们动脑、动手、设计实验的能力。一些同学的基本的操作不够规范,说明基本实验能力还有待加强。
难题解答
[例1]在下面的物理性质中:①银白色金属;②延展性;③导热性;④导电性;⑤被磁铁吸引;其中铁、铜、铝三种金属都具有的是( )
A.①②③ B.②③④ C.③④⑤ D.①⑤
[解析]铁、铜、铝三种金属都具有良好的导电性、导热性、延展性。铜是紫红色,只有铁能被磁铁吸引。
[答案]B
[例2]以下是有关金属问题的研究,某实验小组在探究金属化学性质过程中的部分实验记录,请你根据记录回答下列问题。
(1)大小、形状都相同的金属与溶液质量、溶质质量分数都相同的稀盐酸反应的记录:
据金属活动性顺序和以上记录可知,能与稀盐酸反应的金属应具备的条件是 。
②根据金属活动性顺序,铝片应比锌片活泼,但记录显示铝与稀盐酸的反应速率比锌的 (填“快”或“慢”),你认为该记录中出现与金属活动性顺序相违背的现象的原因是 。
(2)实验小组同学认为,用下列两组试剂都可以完成铜与银的金属活动性强弱的比较:
A.铜片与AgNO3溶液; B.银片与Cu(NO3)2溶液。
请你选择要选用的试剂组并写出对应的实验现象或化学方程式。所选用的一组试剂是 (选填编号), 相应的实验现象或反应的化学方程式是 。
(3)把相同体积、相同质量分数的稀硫酸,分别滴到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中,生成H2的质量与反应时间的关系如上图所示。这三种金属的活动性顺序为 ;假如X、Y、Z都是+2价金属,则相对原子质量由大到小的顺序为 。
[解析](1)①能与酸反应的金属一定是在金属活动性顺序里排在氢元素前面的金属;②铝的活动性比锌的活动性强,但铝表面往往有一层致密的保护膜,所以刚开始反应速度较慢。(2)在验证铜与银的金属活动性强弱时,我们可选用铜与硝酸银溶液,铜能置换硝酸银溶液中的银,所以表面有银白色物质生成。(3)活动
难题解答
性不同的金属与酸反应时,活动性强的金属与酸反应,生成相同质量的H2所需的时间短,所以根据所用时间的长短可判断金属的活动性强弱。而相同质量的金属与酸反应产生的氢气较多,则金属的相对原子质量越小。
[答案](1)①在金属活动性顺序中排在氢元素的前面②慢铝表面有致密的氧化物薄膜(2)A铜片上附有一层银白色固体或Cu+2AgNO3=2Ag+Cu(NO3)2
(3)Y>X>Z Z>Y>X
教学反思
节课以学生自主实验为主,教师在旁指点辅导,要求学生规范地操作,难度不大,但注意事项多,同时要注意药品安全,教师应引导学生设计实验,再由学生操作,最后由学生总结实验探究收获和体会。
教学过程中老师的疑问:
教师点评和总结:
实验活动6 一定溶质质量分数的氯化钠溶液的配制-2024-2025学年初中化学九年级下册人教版配套教案: 这是一份实验活动6 一定溶质质量分数的氯化钠溶液的配制-2024-2025学年初中化学九年级下册人教版配套教案,共4页。
人教版(2024)九年级化学下册实验活动5 常见金属的物理性质和化学性质(导学案) 教案: 这是一份人教版(2024)九年级化学下册实验活动5 常见金属的物理性质和化学性质(导学案) 教案,共5页。教案主要包含了金属的物理性质,金属的化学性质等内容,欢迎下载使用。
人教版(2024)九年级化学下册跨学科实践活动7常见金属的物理性质和化学性质 教案: 这是一份人教版(2024)九年级化学下册跨学科实践活动7常见金属的物理性质和化学性质 教案,共6页。教案主要包含了认识垃圾分类等内容,欢迎下载使用。













