
备战2025年高考二轮复习化学(湖南版)选择题标准练3(Word版附解析)
展开学生用书P285
(选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1.(2024·贵州省六校联盟联考三)化学与生活、科学、技术等密切相关。下列说法正确的是( )
A.不插电的暖贴发热原理是化学能转化为电能
B.葡萄酒中添加适量二氧化硫的作用是漂白杀菌
C.免洗洗手液的有效成分中含有活性银离子,能使蛋白质变性
D.纤维是人们生活中的必需品。天然纤维、再生纤维和合成纤维统称为化学纤维
答案:C
解析:不插电的暖贴发热原理是化学能转化为热能,A错误;葡萄酒中添加适量二氧化硫的作用是抗氧化杀菌,B错误;银离子氧化性较强,能使蛋白质变性,C正确;天然纤维不属于化学纤维,再生纤维和合成纤维统称为化学纤维,D错误。
2.(2024·湖南师大附中三模)下列化学用语或图示表达正确的是( )
A.乙炔分子的空间填充模型:
B.BF4-的结构式:
C.基态铬原子的价层电子轨道表示式:
D.HCl中σ键的形成过程:
答案:D
解析:乙炔分子的空间填充模型为,球棍模型为,故A错误;基态B原子的价层电子排布式为2s22p1,与F形成的三个键为共价键,B提供空轨道,氟离子提供孤电子对,形成配位键,表示为,故B错误;核电荷数为24的基态Cr原子的价层电子轨道表示式:,故C错误;HCl中σ键为s-p σ键,头碰头进行重叠,形成过程:,故D正确。
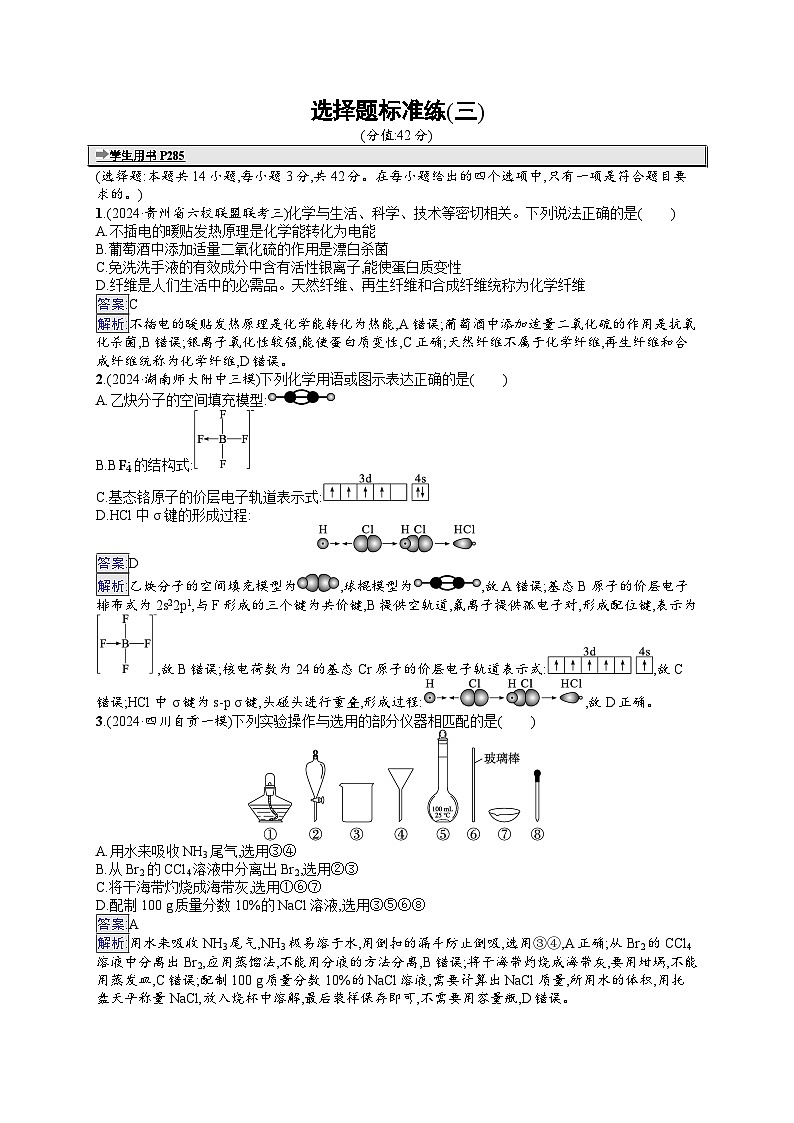
3.(2024·四川自贡一模)下列实验操作与选用的部分仪器相匹配的是( )
A.用水来吸收NH3尾气,选用③④
B.从Br2的CCl4溶液中分离出Br2,选用②③
C.将干海带灼烧成海带灰,选用①⑥⑦
D.配制100 g质量分数10%的NaCl溶液,选用③⑤⑥⑧
答案:A
解析:用水来吸收NH3尾气,NH3极易溶于水,用倒扣的漏斗防止倒吸,选用③④,A正确;从Br2的CCl4溶液中分离出Br2,应用蒸馏法,不能用分液的方法分离,B错误;将干海带灼烧成海带灰,要用坩埚,不能用蒸发皿,C错误;配制100 g质量分数10%的NaCl溶液,需要计算出NaCl质量,所用水的体积,用托盘天平称量NaCl,放入烧杯中溶解,最后装样保存即可,不需要用容量瓶,D错误。
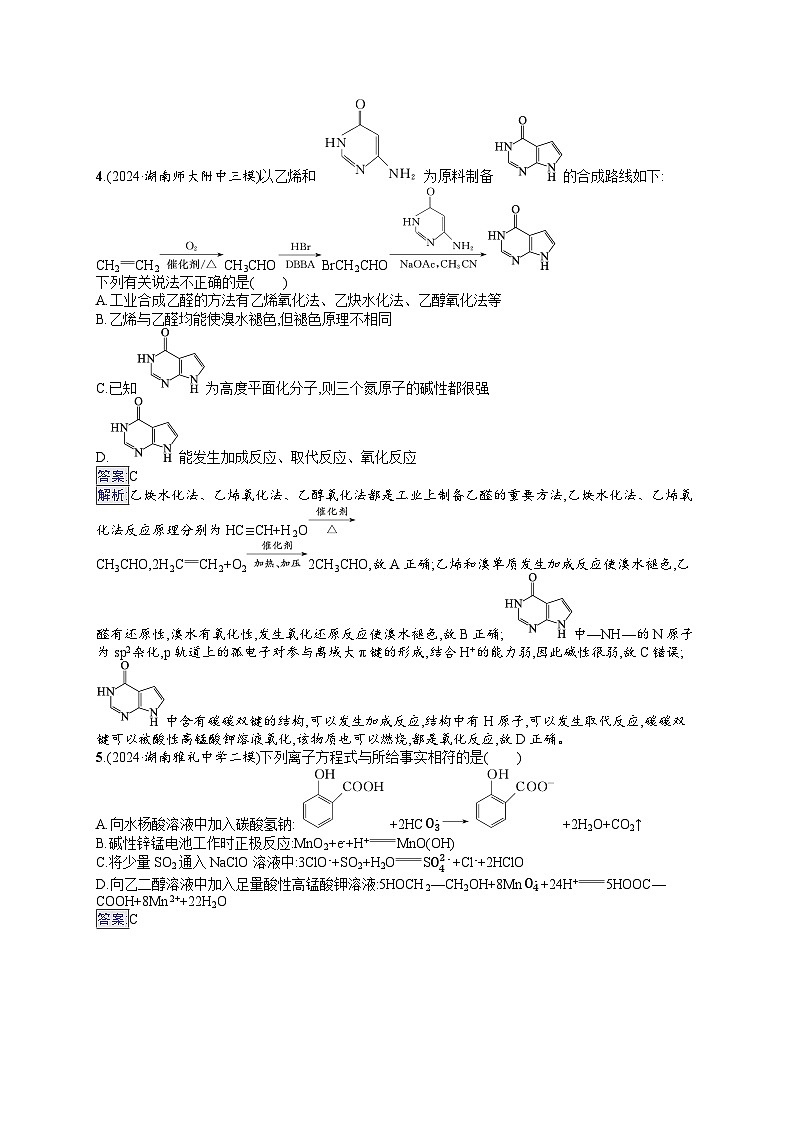
4.(2024·湖南师大附中三模)以乙烯和为原料制备的合成路线如下:
CH2CH2CH3CHOBrCH2CHO
下列有关说法不正确的是( )
A.工业合成乙醛的方法有乙烯氧化法、乙炔水化法、乙醇氧化法等
B.乙烯与乙醛均能使溴水褪色,但褪色原理不相同
C.已知为高度平面化分子,则三个氮原子的碱性都很强
D.能发生加成反应、取代反应、氧化反应
答案:C
解析:乙炔水化法、乙烯氧化法、乙醇氧化法都是工业上制备乙醛的重要方法,乙炔水化法、乙烯氧化法反应原理分别为HC≡CH+H2O
CH3CHO,2H2CCH2+O22CH3CHO,故A正确;乙烯和溴单质发生加成反应使溴水褪色,乙醛有还原性,溴水有氧化性,发生氧化还原反应使溴水褪色,故B正确;中—NH—的N原子为sp2杂化,p轨道上的孤电子对参与离域大π键的形成,结合H+的能力弱,因此碱性很弱,故C错误;中含有碳碳双键的结构,可以发生加成反应,结构中有H原子,可以发生取代反应,碳碳双键可以被酸性高锰酸钾溶液氧化,该物质也可以燃烧,都是氧化反应,故D正确。
5.(2024·湖南雅礼中学二模)下列离子方程式与所给事实相符的是( )
A.向水杨酸溶液中加入碳酸氢钠:+2HCO3-+2H2O+CO2↑
B.碱性锌锰电池工作时正极反应:MnO2+e-+H+MnO(OH)
C.将少量SO2通入NaClO溶液中:3ClO-+SO2+H2OSO42-+Cl-+2HClO
D.向乙二醇溶液中加入足量酸性高锰酸钾溶液:5HOCH2—CH2OH+8MnO4-+24H+5HOOC—COOH+8Mn2++22H2O
答案:C
解析:酚羟基酸性小于碳酸,不会和碳酸氢钠反应生成二氧化碳,离子方程式为+HCO3-+H2O+CO2↑,A错误;碱性锌锰电池中二氧化锰作正极,正极上得电子发生还原反应,正极反应式为MnO2+e-+H2OMnO(OH)+OH-,B错误;少量二氧化硫通入次氯酸钠溶液中,发生氧化还原反应生成硫酸根离子和氯离子,同时过量的次氯酸根离子和氢离子反应生成弱酸次氯酸,离子方程式为3ClO-+SO2+H2OSO42-+Cl-+2HClO,C正确;乙二醇溶液与足量酸性高锰酸钾溶液反应生成硫酸钾、硫酸锰、二氧化碳和水,反应的离子方程式为+2MnO4-+6H+2Mn2++2CO2↑+6H2O,D错误。
6.(2024·安徽安庆二模)根据下列实验事实能得出相应结论的是( )
答案:B
解析:A项,淀粉溶液中滴加稀硫酸,水浴加热后,没有加NaOH中和硫酸,不能检验葡萄糖,则不能说明淀粉没有发生水解;B项,CuCl2溶液中存在[Cu(H2O)4]2+(蓝色)+4Cl-[CuCl4]2-(黄色)+4H2O ΔH>0,故将试管中的CuCl2溶液加热,再冷却降温,观察溶液颜色的变化能够探究温度对平衡移动的影响;C项,一般剩余的药品不能放回原瓶,防止试剂污染,则剩余的Na2SO4应放在指定的仪器中;D项,硝酸易挥发,应除掉硝酸后再通入硅酸钠溶液,否则无法比较H2CO3和H2SiO3的酸性强弱,即无法得出C的非金属性强于Si;故答案为B。
7.(2024·湖南高考模拟仿真三)下列事实不能通过比较电负性进行解释的是( )
A.CH4比SiH4稳定
B.H2O的键角大于H2S的键角
C.[Fe(CN)6]3-中与Fe3+形成配位键的是碳原子
D.CF3COOH酸性强于CH3COOH
答案:A
解析:CH4比SiH4稳定,是因为H—C比Si—H的键能大,不能通过比较电负性进行解释,A符合题意;H2O的键角大于H2S的键角,是因为S的电负性小于O的电负性,H2O中O周围电子云密度大,成键电子对之间的排斥力大,B不符合题意;CN-中C、N都含有孤电子对,C的电负性较小,更容易提供孤电子对形成配位键,C不符合题意;F的电负性大,—CF3是吸电子基,导致羧基中的羟基极性增强,容易电离出H+,D不符合题意。
8.(2024·山东滨州二模)SiCl4与N-甲基咪唑(,其中含五元平面环)反应可以得到M2+,其结构如图。
下列说法正确的是( )
A.M2+中碳原子和氮原子的杂化方式均有sp2、sp3
B.SiCl4比CCl4易水解的因素包括Si有更多的价层轨道
C.M2+中最多29个原子共面
D.N-甲基咪唑的碱性弱于咪唑
答案:B
解析:由中含五元平面环可知,氮原子只有sp2杂化,A错误;Si有更多的价层轨道能容纳孤电子对,可导致SiCl4比CCl4易水解,B正确;由中含五元平面环可知该结构中最多10个原子共面,又中最多4个和硅共面,即M2+中最多41个原子共面,C错误;甲基是推电子基团,氮原子的电子云密度大于,故碱性更强,D错误。
9.(2024·湖南株洲一模)稀土是一种重要的战略资源,我国是稀土储量最大的国家。铈(Ce)是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为CeCO3F)形式存在。工业上利用氟碳铈矿制取CeCl3的一种工艺流程如图:
下列说法错误的是( )
A.焙烧过程中氧化剂与还原剂的物质的量之比为1∶4
B.通过操作Ⅱ(包含酸溶、蒸发结晶)即可得到纯净的CeCl3·6H2O
C.酸浸过程中用稀硫酸和双氧水替代盐酸可体现环境友好
D.Ce(BF4)3中阴离子的空间结构为正四面体
答案:B
解析:焙烧后Ce元素以CeO2、CeF4形式存在,Ce均表现为+4价,CeCO3F中Ce表现+3价,因此焙烧CeCO3F的过程中Ce的化合价升高,被氧化;CeCO3F为还原剂,氧气为氧化剂,则n(CeCO3F)×1=n(O2)×4,n(O2)∶n(CeCO3F)=1∶4,A正确;通过操作Ⅱ(包含酸溶、蒸发浓缩、冷却结晶、过滤、洗涤、干燥)即可得到纯净的CeCl3·6H2O,B错误;因用盐酸可能会生成污染性气体氯气,所以酸浸过程中用稀硫酸和双氧水替代盐酸可体现环境友好,C正确;Ce(BF4)3中阴离子BF4-的中心原子价层电子对数为4,且不含孤电子对,所以其空间结构为正四面体,D正确。
10.(2024·江西景德镇第三次质检)由于钠资源储量丰富,便于开采,价格便宜,钠离子电池有望成为下一代大规模储能电池。我国化学家最近研制的一种钠离子电池如图所示。下列说法正确的是( )
A.膜是阴离子交换膜
B.充电时Na+向石墨电极移动
C.放电时正极的电极反应:NaV2(PO4)2O2F+2e-+2Na+Na3V2(PO4)2O2F
D.有机溶剂可选择乙醇
答案:C
解析:由图知,金属钠为负极,电极反应式为Na-e-Na+,NaV2(PO4)2O2F和Na3V2(PO4)2O2F掺杂石墨极为正极,电极反应式为NaV2(PO4)2O2F+2e-+2Na+Na3V2(PO4)2O2F。Na+通过膜由负极进入正极,膜是阳离子交换膜,A错误;充电时Na+向金属钠电极移动,B错误;由分析可知C正确;乙醇能与钠反应,故有机溶剂不能选择乙醇,D错误。
11.(2024·江西南昌一模)香花石是我国地质学家发现的新矿物,其化学式为N3(YMZ4)3·2XW。已知X、Y、Z、W、M、N为原子序数依次增大的前20号元素;其中X、Y、N为金属元素,且Y与N同主族;Z原子的s能级电子总数等于p能级的电子总数,W原子核外有1个未成对电子,M的最外层电子数是最内层的2倍。下列说法正确的是( )
A.原子半径:M>W>Z
B.第一电离能:N>Y
C.电负性:X>Y>W
D.简单氢化物的沸点:Z>W
答案:D
解析:已知X、Y、Z、W、M、N为原子序数依次增大的前20号元素;Z原子的s能级电子总数等于p能级的电子总数,则电子排布式为1s22s22p4,为O元素;W原子核外有1个未成对电子且不是金属元素,为F元素;M的最外层电子数是最内层的2倍,则M为Si元素;其中X、Y、N为金属元素,且Y与N同主族,X为Li、Y为Be,故N为Ca。原子半径:M(Si)>Z(O)>W(F),A错误;第一电离能:Y(Be)>N(Ca),B错误;电负性:W(F)>Y(Be)>X(Li),C错误;H2O、HF中存在氢键,水分子间氢键个数多于HF,所以简单氢化物的沸点:H2O>HF,D正确。
12.(2024·湖南雅礼中学三模)CO2催化加氢制甲醇,并进一步生产低碳烯烃,可一定程度上减少我国对原油进口的依赖,对促进国家能源安全具有重大现实意义。CO2催化加氢制甲醇的反应历程如图所示,H2首先在“—O—Ga—O—Zn—”表面解离成2个H*,随后参与到CO2的转化过程。下列说法正确的是( )
A.“—O—Ga—O—Zn—”能改变总反应的焓变
B.H2O是反应历程的中间产物之一
C.反应历程中存在非极性键的断裂和形成
D.理论上反应历程消耗的H*与生成的甲醇的物质的量之比为6∶1
答案:D
解析:催化剂能降低反应的活化能,提高反应速率,但不能改变总反应的焓变,A错误;根据图中信息可知,生成的H2O不再参与后面流程,因此是反应历程的最终产物之一,B错误;该反应的反应物为CO2和H2,产物为CH3OH和H2O,只存在非极性键的断裂,没有非极性键的形成,C错误;由得失电子守恒可得3H2~CH3OH~6H*,所以产生1 ml CH3OH消耗6 ml H*,即理论上反应历程中消耗的H*与生成的甲醇的物质的量之比为6∶1,D正确。
13.(2024·黑龙江哈尔滨三校联考二模)氟化钾镁是一种具有优良光学性能的材料,主要应用于激光领域,其立方晶胞结构如图。NA表示阿伏加德罗常数的值。下列说法错误的是( )
A.K+的配位数为12
B.每个Mg2+位于距其最近且等距的F-构成的正四面体空隙中
C.若Mg2+位于晶胞的体心,则F-位于晶胞的面心
D.若晶胞参数为a nm,则晶体的密度是120×1021a3NA g·cm-3
答案:B
解析:由图可知,与K+等距且最近的F-位于棱心,共12个,即K+的配位数为12,A正确;每个Mg2+位于距其最近且等距的F-构成的正八面体体心中,B错误;若Mg2+位于晶胞的体心,则K+位于晶胞的顶角处,F-位于面心,C正确;由均摊法可知,1个晶胞中含有Mg2+的数目为8×18=1,F-的数目为12×14=3,K+的数目为1,晶体的密度为1×24 g·ml-1+3×19 g·ml-1+1×39 g·ml-1NAml-1×(a×10-7cm)3=120×1021a3NA g·cm-3,D正确。
14.(2024·江苏南京二模)利用管状透氧膜反应器实现乙醇-水重整制氢,具有无需额外热源、氧气可协助消除积碳等优点。其主要反应为:
反应Ⅰ:C2H5OH(g)+H2O(g)2CO(g)+4H2(g) ΔH1=+256 kJ·ml-1
反应Ⅱ:2C2H5OH(g)+3O2(g)4CO2(g)+6H2(g) ΔH2=-1 107 kJ·ml-1
反应Ⅲ:CO(g)+H2O(g)CO2(g)+H2(g) ΔH3=-41 kJ·ml-1
反应Ⅳ:2H2(g)+O2(g)2H2O(g) ΔH4
一定温度下,将一定比例的C2H5OH、H2O、Ar气体通过装有催化剂的管状透氧膜反应器。经计算机仿真模拟,控制n投料(C2H5OH)=1 ml,平衡时氢醇比[n生成(H2)n投料(C2H5OH)]随水醇比[n投料(H2O)n投料(C2H5OH)]、膜管长度的变化如图所示。若仅考虑上述反应,下列说法正确的是( )
A.ΔH4=13(2ΔH1-ΔH2+4ΔH3)
B.水醇比为0时,管长度超过10 cm后氢醇比下降的原因可能为O2氧化H2
C.水醇比为1、管长度为2 cm,若C2H5OH、O2转化率为100%且n生成(CO)n生成(CO2)=9,则管状透氧膜透过氧气0.1 ml
D.实际生产中,水醇比越大、管长度越短,氢气产率越高
答案:B
解析:根据盖斯定律,ΔH4=13(ΔH2-2ΔH1-4ΔH3),A错误;水醇比为0时,发生反应Ⅱ:2C2H5OH(g)+3O2(g)4CO2(g)+6H2(g),管状透氧膜长度越长,与氧气接触越多,氢醇比下降的原因可能为O2氧化H2,B正确;n投料(C2H5OH)=1 ml,水醇比为1,n投料(H2O)=1 ml,管长度为2 cm,由图可知,平衡时氢醇比[n生成(H2)n投料(C2H5OH)]=3.6,n生成(H2)=3.6 ml,根据H守恒,平衡时H2O为6+2-7.22 ml=0.4 ml,n生成(CO)n生成(CO2)=9,根据C守恒,n生成(CO)=1.8 ml、n生成(CO2)=0.2 ml,根据O守恒,则管状透氧膜透过氧气0.3 ml,C错误;由题图可知,D错误。选项
实验事实
结论
A
向淀粉溶液中滴加稀硫酸,水浴加热,再加入新制的Cu(OH)2,无砖红色沉淀
淀粉未发生水解
B
将试管中的CuCl2溶液加热,再冷却降温,观察实验现象
探究温度对平衡移动的影响
C
将实验剩余的Na2SO4固体放回原试剂瓶
可以节约试剂,不浪费资源
D
将硝酸溶液与CaCO3混合后产生的气体直接通入硅酸钠溶液后,溶液变浑浊
非金属性:N>C>Si
备战2025年高考二轮复习化学(湖南版)选择题标准练1(Word版附解析): 这是一份备战2025年高考二轮复习化学(湖南版)选择题标准练1(Word版附解析),共6页。试卷主要包含了下列描述对应方程式错误的是等内容,欢迎下载使用。
备战2025年高考二轮复习化学(湖南版)选择题标准练2(Word版附解析): 这是一份备战2025年高考二轮复习化学(湖南版)选择题标准练2(Word版附解析),共6页。试卷主要包含了化学与生活、科技相关,设NA为阿伏加德罗常数的值,下列化学用语不正确的是,某抗失眠药物的结构简式如图所示等内容,欢迎下载使用。
备战2025年高考二轮复习化学(湖南版)选择题标准练5(Word版附解析): 这是一份备战2025年高考二轮复习化学(湖南版)选择题标准练5(Word版附解析),共6页。试卷主要包含了下列化学用语或图示表达正确的是,某反应体系只有六种粒子,对下列事实的解释错误的是等内容,欢迎下载使用。












