
备战2025年高考二轮复习化学(湖南版)大单元选择题突破练6 B组(Word版附解析)
展开(选择题每小题3分)
1.(2024·黑龙江哈尔滨三校联考二模)下列有关物质的工业制备反应错误的是( )
A.侯氏制碱:NaCl+H2O+NH3+CO2NaHCO3↓+NH4Cl
B.工业合成氨:N2+3H22NH3
C.氯碱工业:2NaCl+2H2O2NaOH+H2↑+Cl2↑
D.冶炼金属铝:2AlCl32Al+3Cl2↑
答案:D
解析:侯氏制碱法是向饱和氯化钠溶液中通入氨气、二氧化碳气体生成碳酸氢钠固体,化学方程式为NaCl+H2O+NH3+CO2NaHCO3↓+NH4Cl,A正确;工业合成氨反应的化学方程式为N2+3H22NH3,B正确;氯碱工业是电解饱和食盐水,反应的化学方程式为2NaCl+2H2O2NaOH+H2↑+Cl2↑,C正确;三氯化铝是共价化合物,熔融态不能电离出自由移动的离子,D错误。
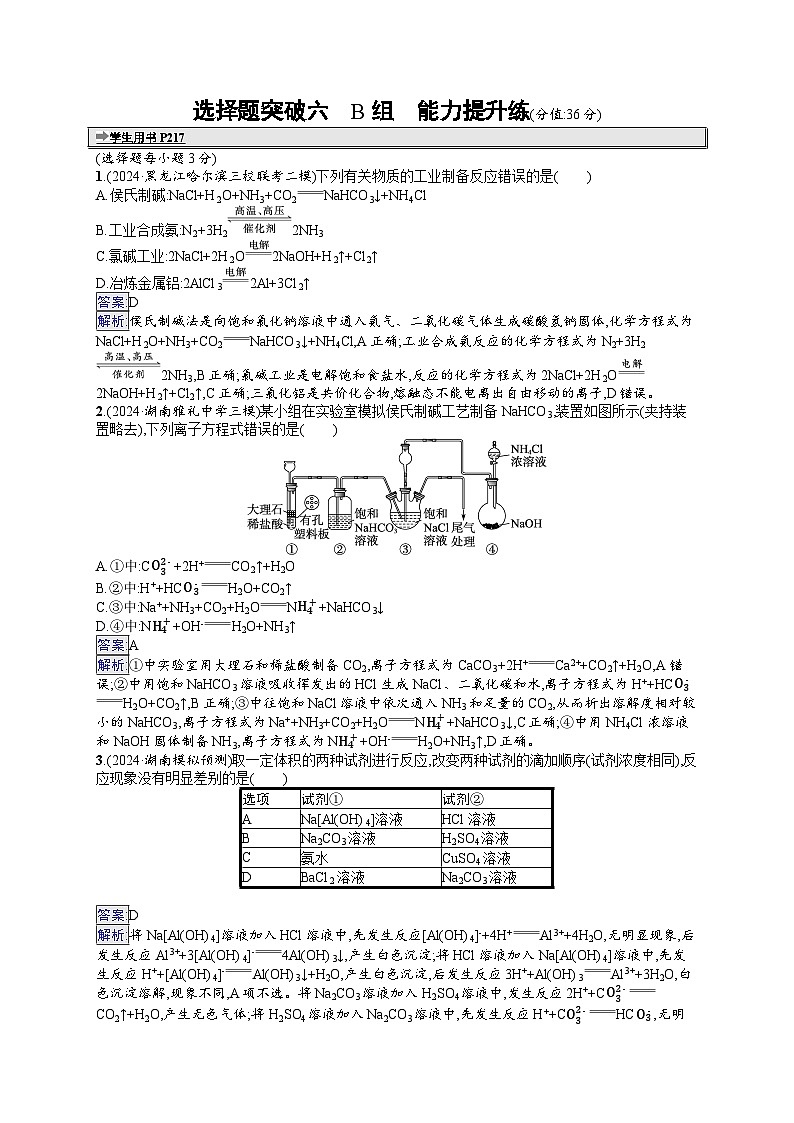
2.(2024·湖南雅礼中学三模)某小组在实验室模拟侯氏制碱工艺制备NaHCO3,装置如图所示(夹持装置略去),下列离子方程式错误的是( )
A.①中:CO32-+2H+CO2↑+H2O
B.②中:H++HCO3-H2O+CO2↑
C.③中:Na++NH3+CO2+H2ONH4++NaHCO3↓
D.④中:NH4++OH-H2O+NH3↑
答案:A
解析:①中实验室用大理石和稀盐酸制备CO2,离子方程式为CaCO3+2H+Ca2++CO2↑+H2O,A错误;②中用饱和NaHCO3溶液吸收挥发出的HCl生成NaCl、二氧化碳和水,离子方程式为H++HCO3-H2O+CO2↑,B正确;③中往饱和NaCl溶液中依次通入NH3和足量的CO2,从而析出溶解度相对较小的NaHCO3,离子方程式为Na++NH3+CO2+H2ONH4++NaHCO3↓,C正确;④中用NH4Cl浓溶液和NaOH固体制备NH3,离子方程式为NH4++OH-H2O+NH3↑,D正确。
3.(2024·湖南模拟预测)取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度相同),反应现象没有明显差别的是( )
答案:D
解析:将Na[Al(OH)4]溶液加入HCl溶液中,先发生反应[Al(OH)4]-+4H+Al3++4H2O,无明显现象,后发生反应Al3++3[Al(OH)4]-4Al(OH)3↓,产生白色沉淀;将HCl溶液加入Na[Al(OH)4]溶液中,先发生反应H++[Al(OH)4]-Al(OH)3↓+H2O,产生白色沉淀,后发生反应3H++Al(OH)3Al3++3H2O,白色沉淀溶解,现象不同,A项不选。将Na2CO3溶液加入H2SO4溶液中,发生反应2H++CO32-CO2↑+H2O,产生无色气体;将H2SO4溶液加入Na2CO3溶液中,先发生反应H++CO32-HCO3-,无明显现象,后发生反应H++HCO3-CO2↑+H2O,产生无色气体,现象不同,B项不选。将氨水加入CuSO4溶液中,先发生反应2NH3·H2O+Cu2+Cu(OH)2↓+2NH4+,生成蓝色沉淀,后发生反应Cu(OH)2+4NH3·H2O[Cu(NH3)4]2++2OH-+4H2O,蓝色沉淀溶解形成深蓝色溶液;将CuSO4溶液加入氨水中,发生反应Cu2++4NH3·H2O[Cu(NH3)4]2++4H2O,溶液变为深蓝色,现象不同,C项不选。无论如何滴加,均产生白色沉淀,现象相同,D项选。
4.(2024·湖南二模)证据推理与模型认知是中学化学的学科核心素养之一,下列类推正确的是( )
A.甲烷是正四面体结构,其键角为109°28';白磷也是正四面体结构,其键角也是109°28'
B.CO2和Na2O2反应生成Na2CO3和O2,推测SO2和Na2O2反应生成Na2SO3和O2
C.根据对角线规则,元素Li和Mg的有些性质相似,推测元素Be和Al的有些性质也相似
D.金属钠能和空气中的氧气、水蒸气反应,因此保存在煤油中,推测金属锂也应保存在煤油中
答案:C
解析:白磷的正四面体结构如图所示,其P—P—P的夹角为60°,故A错误;Na2O2有强氧化性,与具有还原性的SO2直接生成Na2SO4,无O2生成,故B错误;元素周期表中位于对角线位置的元素性质相似,Li和Mg、Be和Al位于元素周期表对角线位置,性质相似,故C正确;金属锂的密度比煤油小,应保存在石蜡中,故D错误。
5.(2024·湖南雅礼中学一模)部分含氮物质的分类与相应氮元素化合价关系如图所示。下列说法不正确的是( )
A.谚语“雷雨发庄稼”中存在转化关系:b→c→d→e
B.常温下,a和e的水溶液等物质的量反应后溶液的pH<7
C.e的浓溶液比浓磷酸易挥发,可能是因为e存在分子内氢键
D.一定条件下,a与CuO反应不能得到b
答案:D
解析:由图可知,a、b、c、d、e均为含氮物质,故a为NH3、b为N2、c为NO、d为NO2或N2O4、e为硝酸,据此解答。
谚语“雷雨发庄稼”是氮气转化为一氧化氮,一氧化氮转化为二氧化氮,二氧化氮溶于水转化为硝酸,即其中存在转化关系:b→c→d→e,故A正确;常温下,a和e的水溶液等物质的量反应后得到硝酸铵,铵根水解,溶液显酸性,即pH<7,故B正确;硝酸的浓溶液比浓磷酸易挥发,可能是因为硝酸存在分子内氢键,故C正确;氨气具有还原性,一定条件下,氨气与CuO反应生成氮气、水和铜,故D错误。
6.(2024·湖南三模)微生物介导的碳氮硫循环耦合如图所示。下列说法错误的是( )
A.S2-在富氧条件下最终的产物为SO32-
B.S2-可作为电子供体进行NO3-还原
C.N2可通过生物固氮作用做氮肥
D.溶液中可能存在:NH4++NO2-N2↑+2H2O
答案:A
解析:SO32-在空气中不稳定,易被氧气氧化为SO42-,A项错误;由循环图可知,S2-可将NO3-还原为N2,B项正确;N2通过豆科植物根瘤菌生物固氮转化为化合物,做氮肥,C项正确;一定条件下,NH4+和NO2-可发生归中反应:NH4++NO2-N2↑+2H2O,D项正确。
7.(2024·广东肇庆二模)某化学兴趣小组为探究蔗糖与浓硫酸的反应设计了如图所示实验装置。倾斜Y形试管使反应发生,下列说法正确的是( )
A.装置Ⅱ中品红溶液褪色,证明SO2具有氧化性
B.装置Ⅲ中产生白色沉淀,其主要成分为CaCO3和CaSO3
C.装置Ⅳ中无明显现象
D.装置不变,仅将装置Ⅰ中的蔗糖换成木炭,也能出现相同的现象
答案:C
解析:蔗糖与浓硫酸反应可生成CO2和SO2,SO2具有漂白性,能使品红溶液褪色,A错误;漂白粉的主要成分是Ca(ClO)2,Ca(ClO)2具有氧化性。通入CO2和SO2后反应生成CaCO3和CaSO4沉淀,B错误;CO2和SO2均不能与BaCl2溶液反应,故装置Ⅳ无明显现象,C正确;木炭与浓硫酸反应需要加热,仅将装置Ⅰ中的蔗糖换成木炭,不能出现相同的现象,D错误。
8.(2024·广东广州天河区综合测试)部分含铜物质的分类与相应化合价的关系如图所示。下列推断不合理的是( )
A.若bc+a,则b既有氧化性又有还原性
B.在加热条件下,c能将乙醇氧化为乙醛
C.a在潮湿的空气中久置会转化为c
D.新制的d可用于检验葡萄糖中的醛基
答案:C
解析:根据题意可知,a为Cu、b为Cu2O、c为CuO、d为Cu(OH)2、e为+2价的铜盐。若Cu2OCuO+Cu,则说明Cu2O既有氧化性又有还原性,A正确;c为CuO,在加热条件下,CuO能将乙醇氧化为乙醛,B正确;铜在潮湿的空气中久置会转化为碱式碳酸铜,而不是转化为氧化铜,C错误;d为Cu(OH)2,新制的Cu(OH)2可用于检验葡萄糖中的醛基,D正确。
9.(2024·湖南株洲质检)稀土是一种重要的战略资源,我国是稀土储量最大的国家。铈(Ce)是一种典型的稀土元素,其在自然界中主要以氟碳铈矿(主要成分为CeCO3F)形式存在。工业上利用氟碳铈矿制取CeCl3的一种工艺流程如图:
下列说法错误的是( )
A.“焙烧”过程中氧化剂与还原剂的物质的量之比为1∶4
B.通过操作Ⅱ(包含酸溶、蒸发结晶)即可得到纯净的CeCl3·6H2O
C.“酸浸”过程中用稀硫酸和双氧水替代盐酸可体现环境友好
D.Ce(BF4)3中阴离子的空间结构为正四面体
答案:B
解析:“焙烧”后Ce元素以CeO2、CeF4的形式存在,Ce均表现为+4价,CeCO3F中Ce表现为+3价,因此“焙烧”CeCO3F时Ce元素的化合价升高,被氧化,则CeCO3F为还原剂,氧气为氧化剂,因此有n(CeCO3F)×1=n(O2)×4,n(O2)∶n(CeCO3F)=1∶4,A正确;通过操作Ⅱ(包含酸溶、蒸发浓缩、冷却结晶、过滤、洗涤、干燥)即可得到纯净的CeCl3·6H2O,B错误;因用盐酸可能会生成污染性气体氯气,所以“酸浸”过程中用稀硫酸和双氧水替代盐酸可体现环境友好,C正确;Ce(BF4)3中阴离子BF4-的中心原子价层电子对数为4,且不含孤电子对,所以其空间结构为正四面体,D正确。
10.(2024·广东广州冲刺训练二)硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS不溶于水)。下列说法不正确的是( )
A.过程①中,生成CuS的反应为S2-+Cu2+CuS↓
B.过程②中,S是氧化产物
C.转化过程中,存在极性共价键的断裂和生成
D.回收S的总反应为2H2S+O22H2O+2S↓
答案:A
解析:过程①中硫化氢和铜离子发生复分解反应生成CuS,硫化氢为弱酸不能拆,反应的离子方程式为H2S+Cu2+CuS↓+2H+,A错误;过程②中硫元素化合价升高被氧化得到氧化产物S,B正确;转化过程中氧气转化为水、硫化氢转化为硫化铜,存在极性共价键的断裂和极性共价键的生成,C正确;总反应为硫化氢和氧气在催化剂作用下生成水和硫单质:2H2S+O22H2O+2S↓,D正确。
11.(2024·广东江门等5地一模)部分含S和Cl的物质类别与相应化合价的关系如图所示。下列说法正确的是( )
A.a和e都是强酸
B.向h的溶液中通入c,溶液的酸性增强
C.b或f与金属Cu反应的产物中Cu的化合价均为+2价
D.c和g都具有漂白性,二者使品红溶液褪色的原理相同
答案:B
解析:根据含S和Cl的物质类别与相应化合价的关系可知,a是H2S、b是S、c是SO2、d是H2SO4、e是HCl、f是Cl2、g是ClO2、h是HClO。a是H2S,属于弱酸,e是HCl,属于强酸,A错误;h是HClO,属于弱酸,c是SO2,向HClO的溶液中通入SO2,发生反应:SO2+HClO+H2OH2SO4+HCl,即生成两种强酸,则溶液酸性增强,B正确;b是S、f是Cl2,两者与金属Cu反应的产物分别为Cu2S、CuCl2,产物中Cu的化合价分别为+1价、+2价,C错误;c是SO2、g是ClO2,SO2具有漂白性,是因为它能与某些有色物质生成不稳定的无色物质,ClO2具有漂白性,是因为ClO2具有氧化性,二者使品红溶液褪色的原理不相同,D错误。
12.(2024·湖南雅礼中学一模)白硼钙石的主要成分是Ca4B10O19·7H2O(含有少量Fe2O3、FeO、CaCO3和SiO2等杂质),利用白硼钙石制取强还原剂NaBH4的工艺流程如下:
已知:H3BO3微溶于水,易溶于乙醇;偏硼酸钠(NaBO2)易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定。下列说法错误的是( )
A.“滤渣1”的主要成分是SiO2
B.“操作X”涉及蒸发浓缩、降温结晶
C.“酸浸”采用高温条件有利于提高反应速率
D.“反应Y”的化学方程式是NaBO2+2MgH22MgO+NaBH4
答案:C
解析:由题干流程图可知,将白硼钙石粉碎后加入浓硝酸,Ca转化为Ca(NO3)2、Fe转化为Fe(NO3)3、B转化为H3BO3,SiO2不溶于硝酸,过滤得到滤液1,主要含有Ca(NO3)2、Fe(NO3)3,滤渣主要含有SiO2和H3BO3,向滤渣中加入乙醇进行醇浸过滤得到滤渣1,主要成分为SiO2,滤液为含有H3BO3的酒精溶液,向滤液中加入NaOH溶液进行水浴加热,将H3BO3转化为NaBO2,将乙醇蒸馏出来后,对滤液进行蒸发浓缩、降温结晶,过滤干燥,获得纯净的NaBO2固体,将固体NaBO2和MgH2混合反应生成NaBH4和耐火材料即MgO,据此分析解题。
由分析可知,“滤渣1”的主要成分是SiO2,A正确;由题干信息知,偏硼酸钠(NaBO2)易溶于水,溶解度随温度升高而增大,难溶于乙醇,碱性条件下稳定,故“操作X”涉及蒸发浓缩、降温结晶,B正确;“酸浸”采用高温条件会导致浓硝酸分解,反应速率减慢,C错误;由分析可知,耐火材料为MgO,故“反应Y”的化学方程式是NaBO2+2MgH22MgO+NaBH4,D正确。选项
试剂①
试剂②
A
Na[Al(OH)4]溶液
HCl溶液
B
Na2CO3溶液
H2SO4溶液
C
氨水
CuSO4溶液
D
BaCl2溶液
Na2CO3溶液
备战2025年高考二轮复习化学(湖南版)大单元选择题突破练3 B组(Word版附解析): 这是一份备战2025年高考二轮复习化学(湖南版)大单元选择题突破练3 B组(Word版附解析),共4页。试卷主要包含了下列离子方程式书写正确的是,下列离子方程式书写错误的是等内容,欢迎下载使用。
备战2025年高考二轮复习化学(湖南版)大单元选择题突破练6 A组(Word版附解析): 这是一份备战2025年高考二轮复习化学(湖南版)大单元选择题突破练6 A组(Word版附解析),共5页。试卷主要包含了4%,278×19等内容,欢迎下载使用。
备战2025年高考二轮复习化学(湖南版)大单元选择题突破练9 B组(Word版附解析): 这是一份备战2025年高考二轮复习化学(湖南版)大单元选择题突破练9 B组(Word版附解析),共5页。试卷主要包含了65 g Zn,理论上转移0等内容,欢迎下载使用。












