

2024-2025学年浙江省浙东北联盟高二(上)期中联考化学试卷(解析版)
展开
这是一份2024-2025学年浙江省浙东北联盟高二(上)期中联考化学试卷(解析版),共19页。试卷主要包含了考试结束后,只需上交答题纸等内容,欢迎下载使用。
1.本卷共6页满分100分,考试时间90分钟。
2.答题前,在答题卷指定区域填写班级、姓名、考场号、座位号及准考证号并填涂相应数字。
3.所有答案必须写在答题纸上,写在试卷上无效。
4.考试结束后,只需上交答题纸。
可能用到的相对原子质量:H-1 C-12 O-16 S-32 Fe-56
选择题部分
一、选择题(每小题只有1个选项符合题目要求。每小题3分,共48分)
1. 影响化学反应速率的主要因素
A. 浓度B. 温度
C. 催化剂D. 反应物的组成、结构和性质
【答案】D
【解析】影响化学反应速率的主要因素是内因,即是反应物的组成、结构和性质。
答案选D。
2. 干冰升华过程中,其焓变和熵变正确的是
A. ,B. ,
C. ,D. ,
【答案】A
【解析】干冰升华过程中吸热,气体分子数增多,结合吸放热与ΔH的关系、气体体积的变化与熵变的关系分析解答。
干冰升华过程中,物质由固态变为气态,体系的混乱度增大,属于熵增的过程,ΔS>0;干冰升华过程中,物质由固态变为气态,为吸热过程,ΔH>0,故A正确;
故答案选A。
3. 实验设计的科学性反映了实验者的科学素养。下列有关测定中和反应反应热的实验,说法正确的是
A. 用温度计测量酸溶液的温度后立即测量碱溶液的温度
B. 为了使反应充分,可以向酸(碱)中分次加入碱(酸)
C. 用铜丝代替玻璃搅拌器,会使中和反应放热测定值偏小
D. 测定中和反应反应热时可用稀醋酸和NaOH稀溶液
【答案】C
【解析】用温度计测量酸溶液的温度,用水冲洗温度计后再测量碱溶液的温度,故A错误;向酸(碱)中分次加入碱(酸),热量损失较多,不能分次加入碱(酸),故B错误;用铜丝代替玻璃搅拌器,会使热量损失较多,使中和反应放热测定值偏小,故C正确;醋酸电离吸热,测定中和反应反应热时不能用稀醋酸和NaOH稀溶液反应,故D错误;
选C。
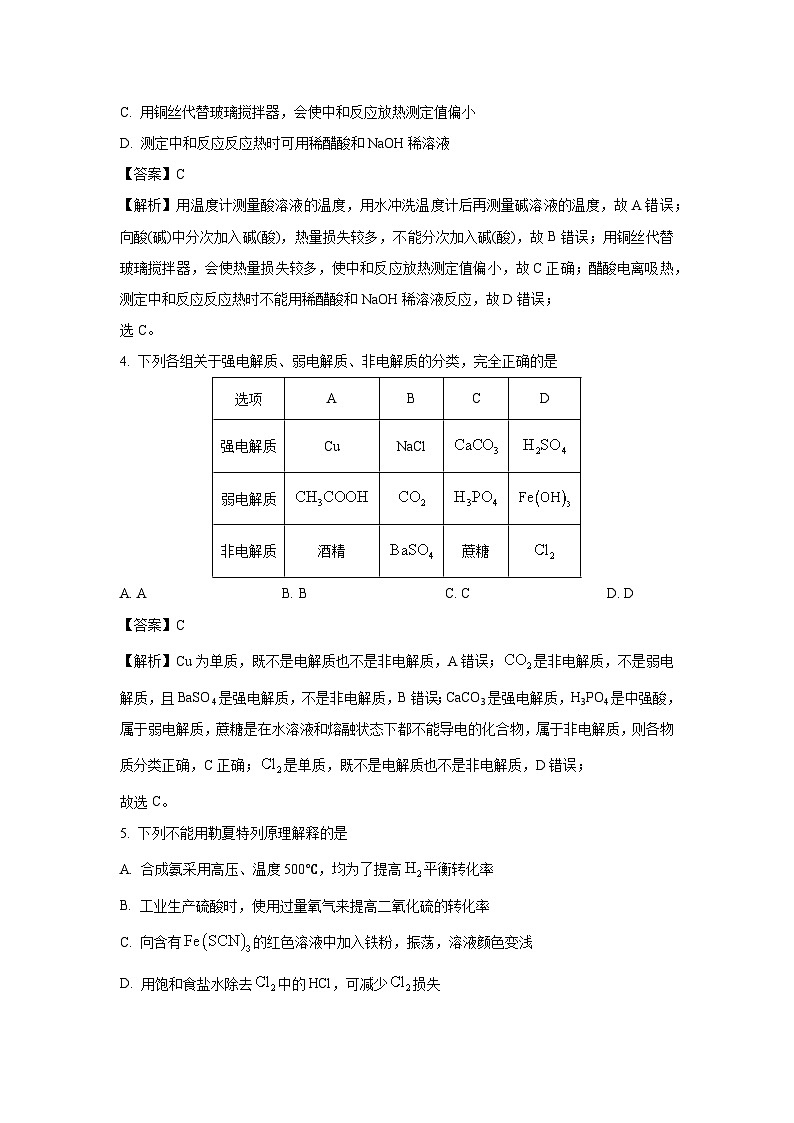
4. 下列各组关于强电解质、弱电解质、非电解质的分类,完全正确的是
A. AB. BC. CD. D
【答案】C
【解析】Cu为单质,既不是电解质也不是非电解质,A错误;是非电解质,不是弱电解质,且BaSO4是强电解质,不是非电解质,B错误;CaCO3是强电解质,H3PO4是中强酸,属于弱电解质,蔗糖是在水溶液和熔融状态下都不能导电的化合物,属于非电解质,则各物质分类正确,C正确;是单质,既不是电解质也不是非电解质,D错误;
故选C。
5. 下列不能用勒夏特列原理解释的是
A. 合成氨采用高压、温度500℃,均为了提高平衡转化率
B. 工业生产硫酸时,使用过量氧气来提高二氧化硫的转化率
C. 向含有的红色溶液中加入铁粉,振荡,溶液颜色变浅
D. 用饱和食盐水除去中的HCl,可减少损失
【答案】A
【解析】合成氨反应为放热反应,升高温度,不利于提高氢气平衡转化率,工业采用500℃条件是为提高催化剂活性,加快反应速率,不能用勒夏特列原理解释,故A符合题意;工业生产硫酸时,使用过量氧气,有利于平衡正向移动,可用勒夏特列原理解释,故B不符合题意;Fe3++3SCN-Fe(SCN)3,Fe+2Fe3+═3Fe2+,铁粉使铁离子与硫氰酸根离子反应的平衡逆向移动,可用勒夏特列原理解释,故C不符合题意;饱和食盐水中存在平衡Cl2+H2OHCl+HClO,增大溶液中氯离子浓度,平衡逆向移动,减小氯气的溶解度,故用排饱和食盐水法除去Cl2中的HCl可用勒夏特列原理来解释,故D不符合题意;
故选:A。
6. 在恒温条件,体积为VL的密闭容器中,充入一定量混合气体发生反应:,达到平衡时,测得A的浓度为1ml·L-1;将容器的体积缩小为0.5VL,再次达到平衡时,测得A的浓度为1.8ml·L-1,下列有关判断正确的是
A. B. 平衡向逆反应方向移动
C. B的浓度比第1次平衡时大D. C的体积分数比第1次平衡时低
【答案】C
【解析】在恒温条件,体积为VL密闭容器中,充入一定量混合气体发生反应:,达到平衡时,测得A的浓度为1ml•L-1,将容器的体积缩小为0.5VL,假设平衡不移动,A的浓度变为2ml•L-1,再次达到平衡时,测得A的浓度为1.8ml•L-1,说明加压平衡正向移动,故x+y>z,据此作答。
由分析可知,x+y>z,故A错误;由分析可知,平衡正向移动,故B错误;平衡正向移动,B的物质的量减小,但容器体积减小程度更大,故B的浓度比第1次平衡时大,故C正确;平衡正向移动,C的体积分数增大,故D错误;
故选:C。
7. 在一恒温恒容容器中,表明反应已达到平衡状态的是
A. 单位时间内生成amlA,同时生成2amlB
B. B、C、D的浓度之比为2∶1∶1
C. 混合气体的密度不再改变
D. 混合气体的压强不再改变
【答案】C
【解析】单位时间内生成aml A,同时生成2aml B,均为逆反应速率,无法判断反应是否达到平衡,故A错误;B、C、D的浓度之比为2:1:1,不知道浓度是否还会变化,无法判断反应是否达到平衡,故B错误;A是固体,容器容积不变,混合气体的密度是变量,当其不再改变时,说明反应达到平衡状态,故C正确;反应前后气体分子数不变,故恒温恒容容器中,混合气体的压强始终不变,无法判断反应是否达到平衡,故D错误;
答案选C。
8. 下列滴定反应中,指示剂使用不正确的是
A. 用强碱标准溶液滴定弱酸溶液,酚酞作指示剂
B. 用标准溶液滴定KI溶液,KSCN作指示剂
C. 用溶液滴定KI溶液,淀粉作指示剂
D. 用酸性标准溶液滴定溶液,无需指示剂
【答案】C
【解析】用强碱标准溶液滴定弱酸溶液,滴定终点溶液显碱性,用酚酞作指示剂,故A正确;Fe3+遇KSCN溶液显红色,用标准溶液滴定KI溶液,用KSCN作指示剂,故B正确;用溶液滴定KI溶液,若用淀粉作指示剂,反应开始溶液就变蓝色,淀粉不能指示滴定终点,故C错误;溶液显紫色,用酸性标准溶液滴定溶液,滴定终点溶液变为浅紫色,无需指示剂,故D正确;
选C。
9. 设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 0.1mlKI与0.1ml在溶液中反应转移的电子数为
B. 1L0.1ml⋅L-1溶液中含有的氧原子数为
C. 25℃时,的醋酸溶液1L,溶液中含的数目小于
D. 30gHCHO与混合物中含C原子数为
【答案】D
【解析】KI与的反应是可逆反应,0.1mlKI与0.1ml在溶液中反应转移的电子数小于,故A错误;溶液中水也含有氧原子,故1L0.1ml⋅L-1溶液中含有的氧原子数大于,故B错误;pH=3的醋酸溶液中氢离子浓度为0.001ml/L,故1L溶液中氢离子的物质的量为n=cV=0.001ml/L×1L=0.001ml,个数为0.001NA,故C错误;HCHO和CH3COOH最简式均为CH2O,30gHCHO和CH3COOH混合物中含C原子数为×1×NA/ml=NA,故D正确;
答案选D。
10. 下列说法中,正确的是
A. 用焓判据和熵判据可解释与盐酸反应在低温下能自发进行
B. 放热过程()或熵增过程()一定是自发的
C. 1ml在不同状态时的熵值:
D. 自发反应: 可用焓判据来解释
【答案】D
【解析】与盐酸反应是吸热反应,用焓判据不能解释其在低温下能自发进行,故A错误;反应自发进行的条件是△H-T△S<0,反应能否自发进行与焓变、熵变和反应温度有关,放热过程(△H0,上述反应中属于吸热反应的是①;
CO的燃烧热是1mlCO燃烧生成二氧化碳放出的热量。根据盖斯定律③-②得表示CO燃烧热的热化学方程式 kJ⋅ml-1。
18. 某小组学生设计了如下实验探究影响化学反应速率因素的实验:
Ⅰ.甲同学利用如图所示装置测定化学反应速率。
(1)圆底烧瓶中发生反应的的离子方程式为___________。
(2)通过测定量气筒中收集到的气体体积计算该反应的速率,结果发现测定值比实际值偏小,其原因可能是___________。
Ⅱ.乙同学利用反应产生沉淀的快慢探究该化学反应速率的影响因素,数据如下表所示:
(3)实验①中,V=___________。
(4)实验②、③的目的是___________。
【答案】(1)
(2)产生的气体部分溶于水,使收集到的比理论值少,导致测定值比实际值小
(3)8 (4)其他条件相同时,探究温度对化学反应速率的影响
【解析】Ⅰ.圆底烧瓶内稀硫酸与硫代硫酸钠反应生成硫酸钠、单质硫、二氧化硫和水,用量气筒测量生成的二氧化硫的体积,由于二氧化硫在水中溶解度较大,故测得的二氧化硫体积会偏小;
Ⅱ.实验利用反应产生沉淀的快慢探究该化学反应速率的影响因素,根据控制变量法,实验①和②探究的是硫酸浓度的影响,实验②和③探究的是温度的影响,在溶液中进行的实验需要使溶液的总体积保持相等,由此计算V的值;
【小问1详解】
稀硫酸与硫代硫酸钠反应生成硫酸钠、单质硫、二氧化硫和水,离子方程式;
【小问2详解】
由分析可知,由于二氧化硫在水中溶解度较大,使收集到的比理论值少,导致测定值比实际值小;
【小问3详解】
在溶液中进行的实验需要使溶液的总体积保持相等,由实验②和③可知,溶液的总体积为10mL,故实验①中加入的水的体积V=8mL;
【小问4详解】
由分析可知,实验②、③的目的是其他条件相同时,探究温度对化学反应速率的影响。
19. 根据电离平衡常数(用表示)的大小可以判断弱电解质的相对强弱。25℃时有关物质的电离平衡常数如下表所示:
(1)25℃,相同浓度的HCOOH和HClO溶液中,导电能力:HCOOH___________HClO,___________(填“>”、“ ②.=
(2)①②④③或“①>②>④>③”或写成“③③”或写成“③
相关试卷
这是一份2024-2025学年浙江省宁波市三锋教研联盟高一(上)11月期中联考化学试卷(解析版),共20页。试卷主要包含了考试结束后,只需上交答题纸,5 Ba-137, 下列属于非氧化还原反应的是等内容,欢迎下载使用。
这是一份2024-2025学年浙江省浙东北联盟高一(上)期中化学试卷(解析版),共23页。试卷主要包含了考试结束后,只需上交答题纸, 下列说法正确的是, 下列试剂的保存方法不正确的是, 下列实验现象的描述正确的是等内容,欢迎下载使用。
这是一份2024-2025学年浙江省宁波五校联盟高一(上)期中联考化学试卷(解析版),共24页。试卷主要包含了考试结束后,只需上交答题纸,可能用到的相对原子质量, 下列说法不正确的是等内容,欢迎下载使用。










