









初中人教版(2024)课题2 金属的化学性质优秀课件ppt
展开
这是一份初中人教版(2024)课题2 金属的化学性质优秀课件ppt,文件包含82金属的化学性质第2课时pptx、82金属的化学性质第2课时分层练习原卷版docx、82金属的化学性质第2课时分层练习解析版docx等3份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
探究金属铝、铜、银的金属活动性强弱。
初步认识常见金属与金属化合物溶液的置换反应。
学习并应用金属活动性顺序。
learning bjectives
金属活动性顺序的应用。
通过实验探究等活动认识金属活动性顺序。
Key pints and difficulties
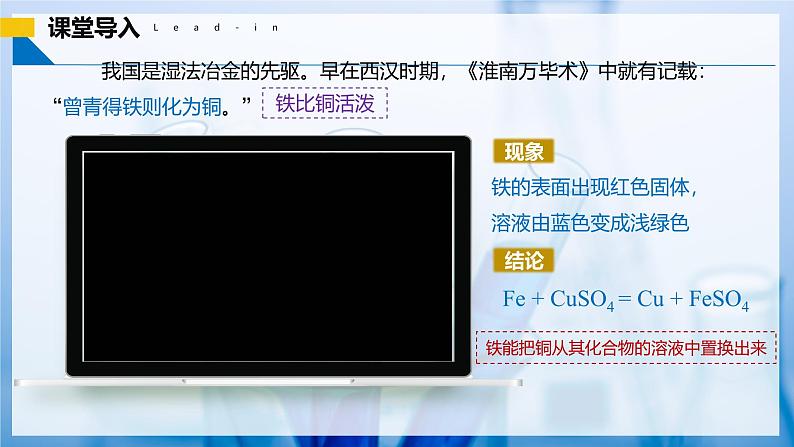
铁的表面出现红色固体,溶液由蓝色变成浅绿色
Fe + CuSO4 = Cu + FeSO4
我国是湿法冶金的先驱。早在西汉时期,《淮南万毕术》中就有记载:“曾青得铁则化为铜。”
铁能把铜从其化合物的溶液中置换出来
【问题】如何设计实验,探究铝、铜、银的金属活动性顺序?【实验】
New Presentatin
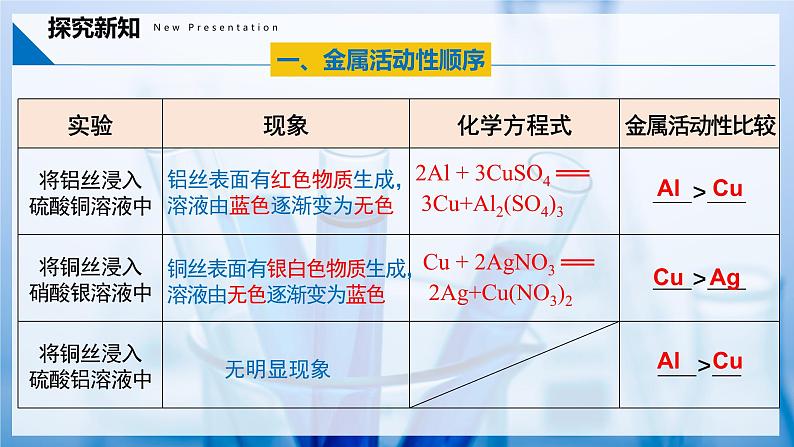
(1)将一根用砂纸打磨过的铝丝浸入硫酸铜溶液中(2)将一根洁净的铜丝浸入硝酸银溶液中(3)将一根洁净的铜丝浸入硫酸铝溶液中
(1) (2) (3)
铝丝表面有红色物质生成,溶液由蓝色逐渐变为无色
铜丝表面有银白色物质生成,溶液由无色逐渐变为蓝色
2Al + 3CuSO4 ══ 3Cu+Al2(SO4)3
Cu + 2AgNO3 ══ 2Ag+Cu(NO3)2
Cu Ag
Al Cu
【分析与结论】1.上述能发生的反应所属的基本反应类型是___________。2.通过上述实验,你能得出铝、铜、银的金属活动性顺序吗?
二、金属活动性顺序的应用
1.判断金属与酸或与其他金属化合物溶液能否反应:
(1)铜与稀盐酸:______________________________________。(2)铜与硫酸亚铁溶液:________________________________。(3)铝与硝酸银溶液:__________________________________。(4)锌与硫酸铜溶液:__________________________________。
Al + 3AgNO3 === Al(NO3)3 + 3Ag
Zn + CuSO4 === ZnSO4 + Cu
2.设计实验比较三种金属活动性的试剂选择:
①先排出金属活动性顺序;②选取两边的金属和中间金属的化合物溶液,即“两金夹一液”;(或选取中间的金属和两边金属的化合物溶液,即“两液夹一金”)。
例:比较Fe、Cu、Ag三种金属的活动性强弱选用试剂为:
① Fe、CuSO4溶液、Ag
② FeSO4溶液、Cu、AgNO3溶液
例:判断下列设计的验证镁、锌、铜的金属活动性顺序的方案是否可行.
Exchange and discuss
3.分析金属与金属化合物溶液反应后滤液、滤渣的成分:
例:向CuSO4溶液中加入一定量的铁粉,充分反应后过滤。(1)反应的化学方程式为____________________________。(2)请根据下表列出的情况,填写滤渣和滤液的成分。(3)如果向滤渣中加入稀盐酸,有气泡产生,则滤渣的成分是____________。
Fe + CuSO4 === FeSO4 +Cu
FeSO4、CuSO4
一种金属与多种金属化合物溶液同时接触且都能发生反应
例:将一定量的Fe粉放入 Cu(NO3)2和 AgNO3的混合溶液中,充分反应后过滤
滤渣中一定含有: ,可能有 。
滤液中一定含有: ,可能有 。
Cu(NO3)2、AgNO3
活动性最弱的金属先被置换出来
例:将一定量的Fe粉、Cu粉铁丝放入 AgNO3溶液中,充分反应后过滤
活动性强的金属先发生反应
多种金属与一种金属化合物溶液同时接触且都能发生反应
Knwledge summary
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属的位置越靠前,它的活动性就越强
位于氢前面的金属能置换出稀HCl、稀H2SO4的氢
位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来
判断金属与酸或与其他金属化合物溶液能否反应
设计实验比较三种金属活动性的试剂选择
分析金属与金属化合物溶液反应后滤液、滤渣的成分
1.根据金属活动性顺序判断,下列各组物质不能发生化学反应的是( ) A.Hg与AgNO3溶液 B.Cu与Mg(NO3)2溶液 C.Zn与FeSO4溶液 D.Al与稀盐酸
2.现有锌、铜、银三种金属,为测定其活动性顺序,可选择的一种试剂是( ) A.稀硫酸 B.硫酸锌溶液 C.硫酸铜溶液 D.硝酸银溶液
3.将等质量的X、Y、Z三种金属分别加入到足量等浓度的稀盐酸中,只有X表面有气泡产生;再把金属Z加入到YNO3溶液中,观察到有固体析出。据此判断三种金属的活动性顺序为( ) A.Z>X>Y B.X>Z>Y C.X>Y>Z D.Y>Z>X
4.如图,将洁净的铝丝放入硝酸铜溶液中,一段时间后溶液蓝色变浅,铝丝表面生长出红色“树枝”,下列说法错误的是( ) A.红色“树枝”成分是铜 B.溶液颜色变浅是由于部分Cu2+转化为Cu C.所得溶液中的金属离子只有Al3+ D.该反应可得出铝的金属活动性比铜强
相关课件
这是一份初中化学人教版(2024)九年级下册(2024)课题2 金属的化学性质获奖课件ppt,文件包含82金属的化学性质第1课时pptx、82金属的化学性质第1课时分层练习解析版docx、82金属的化学性质第1课时分层练习原卷版docx等3份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
这是一份初中人教版(2024)课题2 金属的化学性质课文ppt课件,文件包含第2课时金属活动性顺序pptx、金属活动性mp4、金属置换反应mp4、钠与硫酸铜mp4、铁丝与硫酸铜反应mp4等5份课件配套教学资源,其中PPT共29页, 欢迎下载使用。
这是一份初中化学第八单元 金属和金属材料课题 2 金属的化学性质优质教学课件ppt,共17页。PPT课件主要包含了想想议议,铜+硫酸亚铁,不能能,铝>铜>银,铝丝上附着黑色固体,金属活动性顺序,不反应,Cu-Zn,放入硝酸银溶液中等内容,欢迎下载使用。










