





人教版(2024)九年级上册(2024)课题1 质量守恒定律教案配套ppt课件
展开
这是一份人教版(2024)九年级上册(2024)课题1 质量守恒定律教案配套ppt课件,共28页。PPT课件主要包含了学习目标,木炭烤肉,问题1,问题2,问题3,质量守恒定律,狄仁杰的迷惑等内容,欢迎下载使用。
1.通过实验探究认识质量守恒定律,能说明常见化学反应中的质量关系。2.理解质量守恒定律的微观本质,能用微粒的观点对质量守恒定律作出解释。
1756年,将锡放在密闭的容器里煅烧,生成白色的氧化锡,但容器和容器里的物质总质量在煅烧前后并没有发生变化。
1774年,将45.0份质量的氧化汞加热分解,恰好得到41.5份质量的汞和3.5份质量的氧气,反应前后各物质的质量总和没有改变。
化学反应前后物质的质量关系
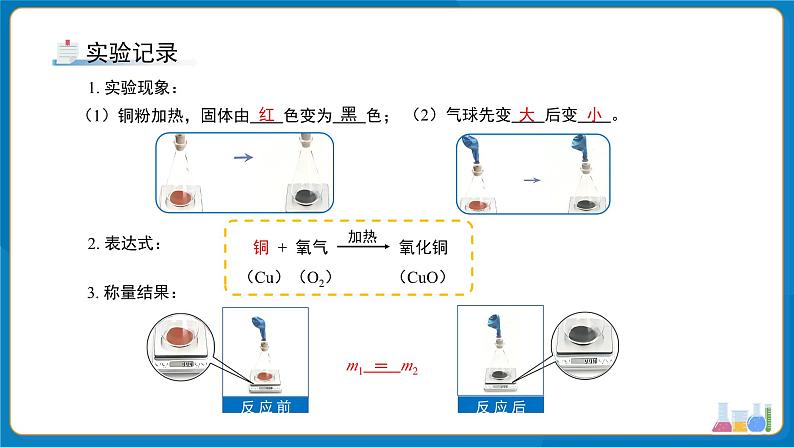
方案一 将铜粉平铺于锥形瓶的底部,把上端系有小气球的玻璃导管插入单孔橡胶塞,用橡胶塞塞紧锥形瓶口。将装置放在天平上称量,记录所称的质量m1。再将锥形瓶置于陶土网上,用酒精灯加热,观察实验现象。反应一段时间后停止加热,待装置冷却后再次称量,记录所称的质量m2。
(2)气球先变 后变 。
(1)铜粉加热,固体由 色变为 色;
玻璃管 小气球
玻璃管 小气球
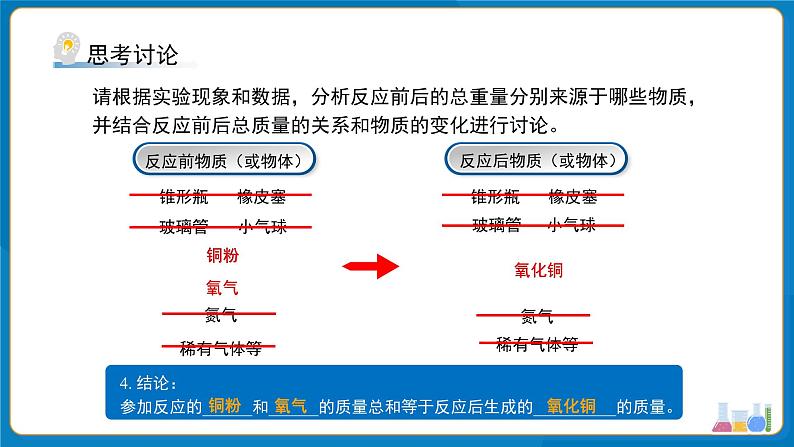
请根据实验现象和数据,分析反应前后的总重量分别来源于哪些物质,并结合反应前后总质量的关系和物质的变化进行讨论。
密闭装置;平衡气压,防止橡胶塞被顶开。
可能出现反应前后天平不平衡,各物质质量总和不相等。
燃烧放热,气球体积膨胀,存在向上的浮力。
铜粉加热装置中“橡胶塞+小气球”装置的作用是什么?
如果没有“橡胶塞+小气球”装置,实验可能出现哪些结果?
待装置冷却后再次称量的原因是什么?
请思考以下问题,在铜粉加热前后质量的测定中,
干燥的固体试剂应放在纸上或容器(如小烧杯、表面皿)中称量;
易潮解的试剂应放在容器中称量。
方案二 在锥形瓶中加入用砂纸打磨干净的铁丝,再小心地放入盛有硫酸铜溶液的小试管,塞好橡胶塞。将装置放在天平上称量,记录所称的质量m1。取下锥形瓶并将其倾斜,使小试管中的硫酸铜溶液流入锥形瓶,观察实验现象。反应一段时间后再次称量,记录所称的质量m2。
(2)铁丝表面有 色物质生成。
(1)溶液由 色变为 色;
铁 + 硫酸铜 → 铜 + 硫酸亚铁 (Fe) (CuSO4) (Cu) (FeSO4)
分析这两个方案的实验现象和实验数据,你能得到什么结论?
参加化学反应的各物质的质量总和
反应后生成的各物质的质量总和
是不是所有的化学反应都遵循这一规律呢?有没有例外呢?
m前________m后
有大量 产生。
反应生成的气体逸散到了空气中。
反应前后测定的结果为什么不一样?
该反应是否遵守质量守恒定律?
镁条燃烧发出__________,生成________,放出____。
镁燃烧后质量增加的原因是什么呢?
若镁燃烧后质量减少了,请分析其原因是什么?
逸散到空气中的氧化镁白烟的质量大于参加反应的氧气质量。
如果用有气体参加或生成的反应验证质量守恒定律要在密闭体系中进行。
质量守恒定律揭示的是“质量”方面的守恒关系,不能任意扩展到其他物理量;
物理变化不适用此定律;
质量守恒定律的适用对象只能是化学变化;
如:体积或分子个数的守恒这就是错误的。
化学反应中,各反应物之间要按一定的质量比相互作用,因此参加反应的各物的质量总和不是任意比例的反应物质量的简单加和。
以氢气在氧气中燃烧生成水为例,分析化学反应前后元素、分子、原子的种类、数目和质量的变化情况,从微观和宏观两个视角说明化学反应为什么遵守质量守恒定律。
反应物和生成物的总质量
在科学家对物质的组成和结构有了更深入的认识后,人们从微观本质上揭示了化学反应前后质量守恒的原因。化学反应的过程,就是参加反应的各物质(反应物)的原子重新组合生成新物质(生成物)的过程。化学反应前后,原子的种类和数目不变,原子的质量也没有改变,因此参加反应的各物质的质量总和一定等于生成的各物质的质量总和。
为什么铁刀放置较长时间后质量会增加呢?
为什么蜡烛燃烧后质量会减轻呢?
燃烧时产生CO2气体和水蒸气等。
1.在化学变化中,下列说法正确的是( )①原子的种类、元素的种类、分子的种类均不变②原子的数目、分子的数目均不变③原子的质量、元素的质量、物质的总质量均不变④原子核的种类、数量、质量均不变A.①② B.①③ C.③④ D.②④
在化学变化中,五个“不变”:从宏观上看,物质总质量、元素种类不变;从微观上看,原子种类、原子数目、原子质量一定不会变化;两个“一定变”:从宏观上看,物质的种类一定变;从微观上看,分子的种类一定变;一个“可能变”:分子的数目可能变;所以③④说法正确, ①②说法错误。
2.某物质在纯氧中燃烧后生成二氧化碳和水,则该物质的组成为( )A.可能是化合物,也可能是单质 B.一定含有碳、氢、氧三种元素C.一定含有碳、氢元素,可能含有氧元素D.无法确定
3.现将20 g A和足量B在一定条件下充分反应,生成16 g C和11 g D,则参加反应的A和B的质量比是( )A.20:11 B.20:7 C.5:4 D.16:11
根据质量守恒定律,参与反应的B的质量为16 g+11 g-20 g=7 g
4.下列关于质量守恒定律的说法正确的是( )A.参加反应的氢气和氧气的体积,一定等于生成的水的体积 B.100 g冰融化得到100 g水,符合质量守恒定律C.高锰酸钾加热后固体质量减少,说明这一反应不符合质量守 恒定律D.镁条燃烧后,生成物质量比镁条的质量大,该反应符合质量 守恒定律
质量守恒定律揭示的是“质量”方面的守恒关系,不能任意扩展到其他物理量。
相关课件
这是一份初中化学人教版九年级上册课题 1 质量守恒定律说课课件ppt,共18页。PPT课件主要包含了学习目标,提出问题,设计实验,实验原理,方案一,实验步骤,方案二,浅绿色,大量白烟,化学变化的实质是等内容,欢迎下载使用。
这是一份初中化学人教版九年级上册课题 1 质量守恒定律课前预习ppt课件,共14页。PPT课件主要包含了学习目标,P96,练一练等内容,欢迎下载使用。
这是一份初中化学人教版九年级上册课题 1 质量守恒定律课文配套课件ppt,共39页。PPT课件主要包含了你猜得着吗,情景引入,实验探究1,实验探究2,产生的现象为,得出结论,P94,练一练,盐酸与碳酸钠反应,实验探究3P94等内容,欢迎下载使用。









