





2025版高考化学全程一轮复习第46讲化学反应速率化学平衡的常规图像课件
展开
这是一份2025版高考化学全程一轮复习第46讲化学反应速率化学平衡的常规图像课件,共52页。PPT课件主要包含了类型一,类型二,类型三,增大反应物的浓度,增大生成物的浓度,使用催化剂,答案B,ACDF,答案D,答案C等内容,欢迎下载使用。
1. 系统掌握速率、平衡图像的分析方法。2.加深对勒夏特列原理的理解。
类型一 瞬时速率—时间图像1.“渐变”类速率—时间图像
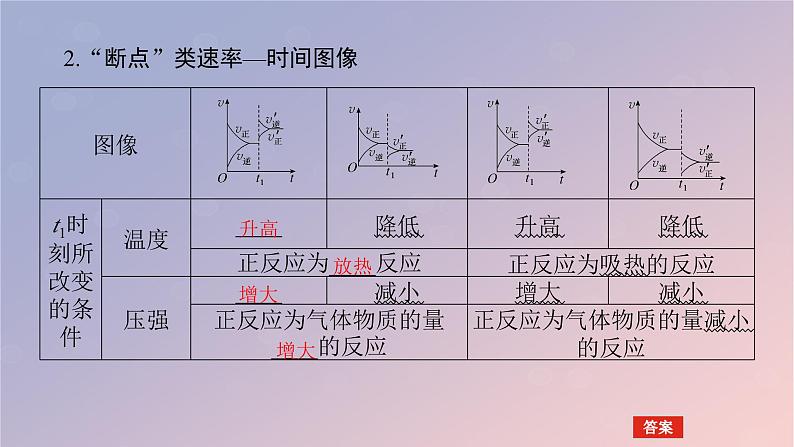
2.“断点”类速率—时间图像
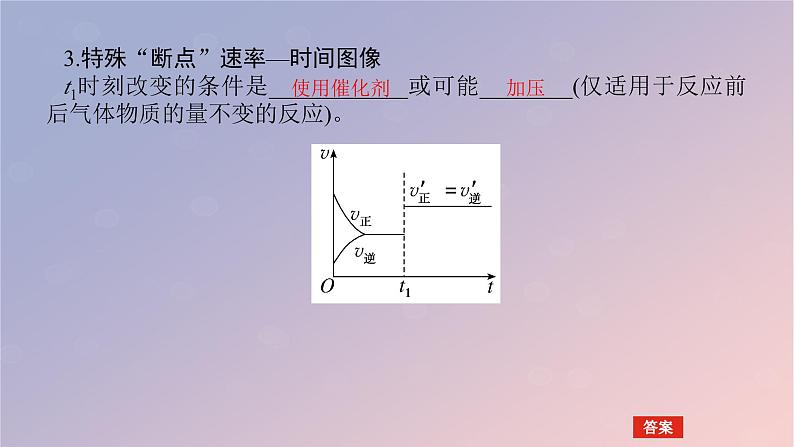
3.特殊“断点”速率—时间图像t1时刻改变的条件是____________或可能________(仅适用于反应前后气体物质的量不变的反应)。
4.反应进程类速率—时间图像Zn与足量盐酸的反应,化学反应速率随时间的变化出现如图所示情况。(1)AB段(v增大)反应放热,溶液温度逐渐升高,v增大;(2)BC段(v减小)溶液中c(H+)逐渐减小,v减小。
【教考衔接】例 [2021·湖南卷,11改编]已知:A(g)+2B(g)⇌3C(g) ΔH<0,向一恒温恒容的密闭容器中充入1 ml A和3 ml B发生反应,t1时达到平衡状态I,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是________。a.容器内压强不变,表明反应达到平衡b.t2时改变的条件:向容器中加入Cc.平衡时A的体积分数φ:φ(Ⅱ)>φ(Ⅰ)d.平衡常数K:K(Ⅱ)<K(Ⅰ)
解析:容器内发生的反应为A(g)+2B(g)⇌3C(g),该反应是气体分子数不变的可逆反应,所以在恒温恒容条件下,气体的压强始终保持不变,则容器内压强不变,不能说明反应达到平衡状态,a错误;根据图像变化曲线可知,t2~t3过程中,t2时v′正瞬间不变,平衡过程中不断增大,则说明反应向逆反应方向移动,且不是“突变”图像,属于“渐变”过程,所以排除温度与催化剂等影响因素,改变的条件为:向容器中加入C,b正确;最初加入体系中的A和B的物质的量的比值为1∶3,当向体系中加入C时,平衡逆向移动,最终A和B各自物质的量增加的比例为1∶2,因此平衡时A的体积分数φ(Ⅱ)>φ(Ⅰ),c正确;平衡常数K与温度有关,因该反应在恒温条件下进行,所以K保持不变,d错误。
【对点演练】1.可逆反应2SO2(g)+O2(g)⇌2SO3(g)在一定条件下达到平衡状态。在t1时刻改变某一条件,化学反应速率与反应时间的关系如图所示。下列说法正确的是( )A.维持温度、反应体系容积不变,t1时充入SO3(g)B.维持温度、压强不变,t1时充入SO3(g)C.维持反应体系容积不变,t1时升高反应体系温度D.维持温度、反应体系容积不变,t1时充入一定量Ar
解析:维持温度、反应体系容积不变,t1时充入SO3(g),此时逆反应速率增大,正反应速率不变,故A错误;维持温度、压强不变,t1时充入SO3(g),此时逆反应速率增大,而且反应体系容积增大导致正反应速率减小,故B正确;维持反应体系容积不变,t1时升高反应体系温度,正、逆反应速率都增大,故C错误;维持温度、反应体系容积不变,t1时充入一定量Ar,反应物和生成物浓度都不变,正、逆反应速率都不变,故D错误。
2.在一密闭容器中发生反应N2(g)+3H2(g)⇌2NH3(g) ΔH0],c(N2O4)随t(时间)变化曲线如图,画出0~t2时段,c(NO2)随t变化曲线。保持其他条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线。
类型三 恒压(或恒温)线此类图像的纵坐标为某物质的平衡浓度或转化率,横坐标为温度或压强,解答此类问题,要关注曲线的变化趋势,有多个变量时,注意控制变量,即“定一议二”。反应:aA(g)+bB(g)⇌cC(g)+dD(g) ΔH
合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分数越大
解析:①合成氨的反应中,压强越大越有利于氨的合成,因此,压强越大平衡时氨的摩尔分数越大。由图中信息可知,在相同温度下,反应达平衡时氨的摩尔分数p1<p2<p3,因此,图中压强由小到大的顺序为p1<p2<p3,判断的依据是:合成氨的反应为气体分子数减少的反应,压强越大平衡时氨的摩尔分数越大。②对比图3和图4中的信息可知,在相同温度和相同压强下,图4中平衡时氨的摩尔分数较小。在恒压下充入惰性气体Ar,反应混合物中各组分的浓度减小,各组分的分压也减小,化学平衡要朝气体分子数增大的方向移动,因此,充入惰性气体Ar不利于合成氨,进料组成中含有惰性气体Ar的图是图4。
【对点演练】1.如图是温度和压强对反应X+Y⇌2Z影响的示意图。图中横坐标表示温度,纵坐标表示平衡时混合气体中Z的体积分数。下列叙述正确的是( )A.上述可逆反应的正反应为放热反应B.X、Y、Z均为气态C.X和Y中最多只有一种为气态,Z为气态D.上述反应的逆反应的ΔH>0
解析:由图像可知,随温度升高Z的体积分数增大,正反应为吸热反应,逆反应为放热反应,故A、D错误;相同温度下,压强越大,Z的体积分数越小,说明增大压强平衡左移,则Z为气态,X、Y中最多只有一种气态物质,故B错误、C正确。
2.反应N2O4(g)⇌2NO2(g) ΔH=+57 kJ·ml-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )A.A、C两点的化学平衡常数:KA>KCB.A、C两点气体的颜色:A深,C浅C.由状态B到状态A,可以用加热的方法D.A、C两点气体的平均相对分子质量:A>C
解析:A、C两点对应的温度相同,平衡常数只受温度的影响,KA=KC,A错误;A点到C点,压强增大,NO2(g)的浓度增大,虽然平衡逆向移动,最终二氧化氮的浓度比原浓度大,即C点气体颜色比A点深,B错误; A点到B点,NO2的体积分数减小,说明相同压强下,T2到T1,平衡逆向移动,T2>T1,即由状态B到状态A,可以用加热的方法,C正确;A点到C点,压强增大,平衡逆向移动,该反应的逆反应为气体相对分子质量增大的反应,即A点气体的平均相对分子质量小于C点气体的平均相对分子质量,D错误。
3.向体积均为1 L的两恒容容器中分别充入2 ml X和1 ml Y发生反应:2X(g)+Y(g)⇌Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法正确的是( )A.ΔH>0B.气体的总物质的量:na
相关课件
这是一份新高考化学一轮复习讲义课件第7章 第44讲 化学反应速率、平衡的常规图像(含解析),共60页。PPT课件主要包含了复习目标,常规图像题的解题步骤,ACDF,n1-n3,n2-n3,Kb>Kc>Kd,真题演练明确考向,p1>p2>p3,课时精练,曲线a等内容,欢迎下载使用。
这是一份2025届高中化学全程复习构想课件全套46化学反应速率、化学平衡的常规图像,共53页。PPT课件主要包含了类型一,类型二,类型三,增大反应物的浓度,增大生成物的浓度,使用催化剂,答案B,ACDF,答案D,答案C等内容,欢迎下载使用。
这是一份课件 高考化学一轮复习第八单元 化学反应速率与化学平衡 第31讲 化学反应速率与平衡图像分析,共60页。PPT课件主要包含了夯实必备知识,对点自测,提升关键能力,经典真题·明考向,备用习题,作业手册,CH3OH,p1p2p3等内容,欢迎下载使用。








