

广东省建文教育集团两学部2024-2025学年高三上学期1月第一次模拟考试化学试题
展开
这是一份广东省建文教育集团两学部2024-2025学年高三上学期1月第一次模拟考试化学试题,共9页。试卷主要包含了未知,单选题,解答题等内容,欢迎下载使用。
一、未知
1.下列说法正确的是
A.仅用酸性高锰酸钾溶液可以鉴别苯、苯乙烯、环己烷
B.糖类、蛋白质、油脂都可以发生水解
C.以苯甲醇为原料可以制得苯甲酸
D.分子式为的有机物一定能和钠反应产生H2
二、单选题
2.下列属于盐的是
A.Na2CO3B.MgOC.NaOHD.CH4
三、未知
3.下列说法不正确的是
A.铁锈的形成一定发生了氧化还原反应B.复分解反应都不是氧化还原反应
C.燃烧都是放热反应,也都是氧化还原反应D.分解反应都是氧化还原反应
4.下列表示物质结构的化学用语或模型图正确的是
A.CO2的比例模型:
B.的电子式为:
C.的结构式:
D.的原子结构示意图:
四、单选题
5.下列实验不能获得成功的是
①将水和溴乙烷混合加热制乙醇
②将乙醇与浓硫酸共热至140℃来制取乙烯
③用电石和水制取乙炔
④苯、浓溴水和铁粉混合,反应后可制得溴苯
⑤将乙醇和3 ml•L -1的硫酸按体积比1:3混和共热至170 ℃制乙烯
A.只有②④⑤B.只有①②④C.只有②④D.只有①②④⑤
6.由CO2合成环状碳酸酯的一种反应机理如图所示。
下列说法不正确的是
A.转化过程中涉及极性键的断裂与形成
B.根据杂化轨道理论,上述转化过程中的含碳化合物碳原子的杂化方式为sp2和sp3
C.化合物1的阳离子体积大,所含离子键较弱,其常温下可能为液态
D.可按照该反应机理与CO2反应生成
7.下列说法正确的是( )
A.HCl和NaOH反应的中和热△H=-57.3 kJ/ml,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3) kJ/ml
B.需要加热才能发生的反应一定是吸热反应
C.0.1ml氮气和0.3ml氢气,在密闭容器中充分反应生成氨气,转移的电子数为0.6NA
D.电热水器用镁棒防止内胆腐蚀,原理是牺牲阳极的阴极保护法
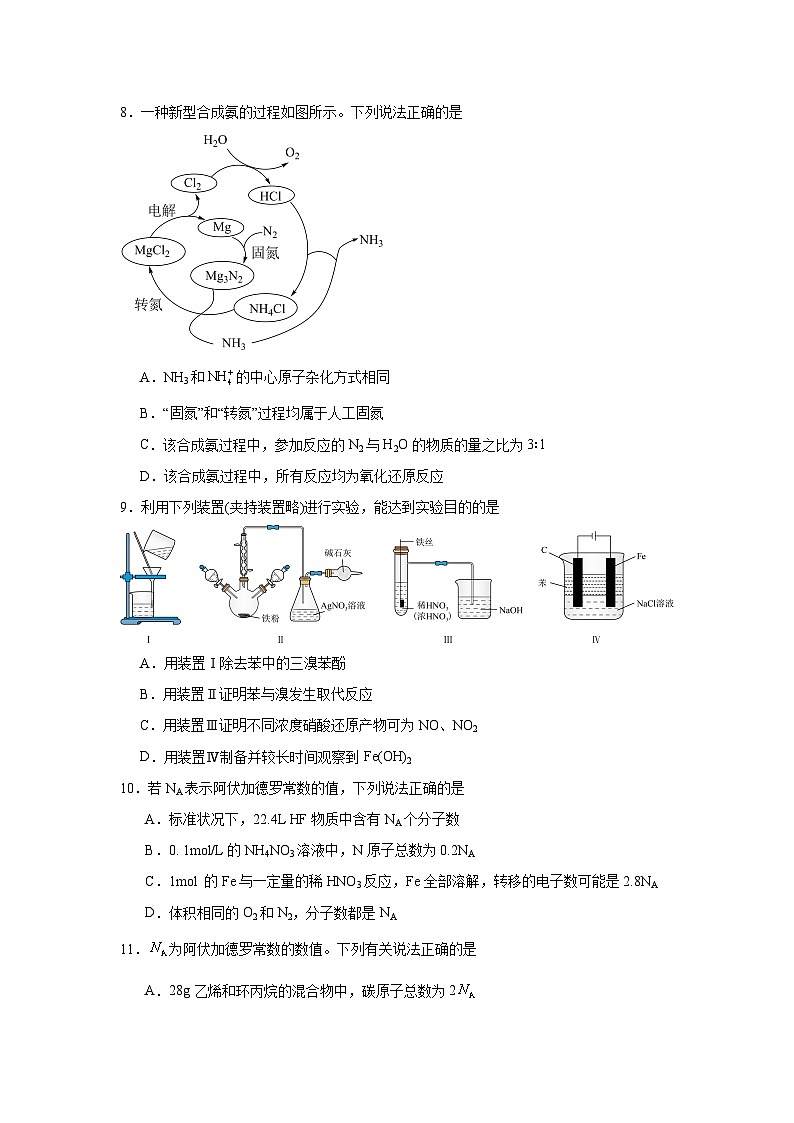
8.一种新型合成氨的过程如图所示。下列说法正确的是
A.NH3和的中心原子杂化方式相同
B.“固氮”和“转氮”过程均属于人工固氮
C.该合成氨过程中,参加反应的N2与H2O的物质的量之比为3∶1
D.该合成氨过程中,所有反应均为氧化还原反应
9.利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A.用装置Ⅰ除去苯中的三溴苯酚
B.用装置Ⅱ证明苯与溴发生取代反应
C.用装置Ⅲ证明不同浓度硝酸还原产物可为NO、NO2
D.用装置Ⅳ制备并较长时间观察到Fe(OH)2
10.若NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下,22.4L HF物质中含有NA个分子数
B.0. 1ml/L的NH4NO3溶液中,N原子总数为0.2NA
C.1ml 的Fe与一定量的稀HNO3反应,Fe全部溶解,转移的电子数可能是2.8NA
D.体积相同的O2和N2,分子数都是NA
11.为阿伏加德罗常数的数值。下列有关说法正确的是
A.28g乙烯和环丙烷的混合物中,碳原子总数为2
B.25℃,0.01水溶液中的数目小于0.01
C.标准状况下,11.2L HF所含有的分子数为0.5
D.1ml环戊烯()中含有键的数目为5
12.某同学在pH试纸上滴几滴新制氯水,现象如图所示,有关该实验的说法中正确的是
A.该实验说明因具有强氧化性能漂白试纸
B.该实验说明扩散速度比HClO快
C.将实验后的pH试纸在酒精灯上微热,试纸又恢复为原来的颜色
D.若用久置的氯水进行实验,现象相同
13.高纯镓是制备第三代半导体的重要原料,其化学性质与铝相似。下图为工业精炼镓的装置示意图。下列说法不正确的是
A.阴极的电极反应为
B.电解过程中,阳极室中的物质的量减小
C.电路中每转移电子,理论上粗镓熔融液减少
D.电解后粗镓中的以离子形式进入溶液中
14.下列分子或离子中含有孤电子对的是
A.B.C.D.
15.下列各化学图示均能表示乙烯分子,其中更能真实反映乙烯分子结构的是
A.B.
C.D.
16.将4 ml NO(g)和4 ml CO(g)充入一个2 L恒容密闭容器中,发生反应:2NO(g)+2CO(g)2CO2(g)+N2(g) ΔH<0,测得CO的平衡转化率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测CO转化率与反应温度的关系曲线如图2所示。下列说法错误的是
已知:反应速率v=v正−v逆=k正·c2(NO)·c2(CO)−k逆·c2(CO2)·c(N2),k正、k逆分别为正、逆反应速率常数。
A.图像中A点逆反应速率小于B点正反应速率
B.200℃时反应的平衡常数K=0.5
C.200℃时当CO的转化率为40%时,v正∶v逆=20:81
D.C点转化率低于B点的原因可能是催化剂活性降低或平衡逆向移动造成的
五、解答题
17.盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备的工艺流程如图:
已知:常温下,。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的B(OH)3在水中存在平衡:(常温下,);B(OH)3与溶液反应可制备硼砂。常温下,在硼砂溶液中,水解生成等物质的量浓度的B(OH)3和,该水解反应的离子方程式为 ,该溶液pH= 。
(2)滤渣Ⅰ的主要成分是 (填化学式);精制Ⅰ后溶液中Li+浓度为,则常温下精制Ⅱ过程中浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加 的用量(填化学式)。
(3)精制Ⅱ的目的是 ;进行操作X时应选择的试剂是 。
18.在课堂上,老师演示了金属钠与CuSO4溶液的反应,同学们观察到该反应中生成了蓝色的Cu(OH)2沉淀而没有发现铜单质生成。但某同学想:会不会因生成的铜较少被蓝色沉淀所覆盖而没有被发现呢?于是他想课后到实验室继续探究,希望进一步用实验来验证自己的猜测是否正确。
假如该同学是你,请你写一张实验准备单交给老师,请求老师提供必需的用品。
(1)实验探究目的: 。
(2)探究所依据的化学原理: 。
(3)实验必需仪器:小刀、玻璃片、滤纸、漏斗、玻璃棒、铁架台、 和 ;实验药品:金属钠、 和 。该同学在探究实验中意外地发现生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是 ,生成该黑色难溶物的原因是 。
19.研究NOx、CO等大气污染气体的处理及利用的方法具有重要意义,可实现绿色环保、节能减排、废物利用等目的。
(1) 利用甲烷催化还原NOx:
CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=﹣574kJ•ml﹣1
CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=﹣1160kJ•ml﹣1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:CO(g)+H2O(g)H2(g)+CO2(g),500℃时的平衡常数为9,若在该温度下进行,设起始时CO和H2O的起始浓度均为0.020 ml·L-1,则CO的平衡转化率为: 。
(3) 用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图1所示。
①写出总反应化学方程式 。
②测得该反应的平衡常数与温度的关系为:lgK=5.08+217.5/T,该反应是 反应(填“吸热”或“放热”)。
③该反应的含氮气体组分随温度变化如图2所示,当温度达到700K时,发生副反应的化学方程式 。
(4)下图是用食盐水做电解液电解烟气脱氮的一种原理图,NO被阳极产生的氧化性物质氧化为NO3—,尾气经氢氧化钠溶液吸收后排入空气。如下图,电流密度和溶液pH对烟气脱硝的影响。
①NO被阳极产生的氧化性物质氧化为NO3-反应的离子方程式 。
②溶液的pH对NO去除率影响的原因是 。
③若极板面积10cm2,实验烟气含NO 1.5%,流速为0.070L·s-1(气体体积已折算成标准状态,且烟气中无其他气体被氧化),法拉第常数为96500 C·ml-1,测得电流密度为1.0 A·cm-2。列式计算实验中NO除去率 。
六、未知
20.化合物最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,的钙盐是人们喜爱的补钙剂之一,又称为乳酸(A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,可发生如图所示的反应。
(1)化合物的结构简式: ; ; 。
(2)化学方程式: 。
(3)反应类型: 。
相关试卷
这是一份广东省清远市2024-2025学年高三上学期第一次模拟考试化学试题,共6页。
这是一份广东省2024-2025学年高三上学期12月第一次模拟考试化学试题,共14页。试卷主要包含了单选题,非选择题等内容,欢迎下载使用。
这是一份广东省两校2025届高三上学期十月第一次模拟考试化学试题+答案,共17页。








