














初中化学课题2 常见的酸和碱优质ppt课件
展开
这是一份初中化学课题2 常见的酸和碱优质ppt课件,文件包含核心素养人教版化学九年级下册课题2常见的酸和碱第1课时同步课件pptx、核心素养人教版化学九年级下册课题2常见的酸和碱第1课时同步教案docx、核心素养人教版化学九年级下册《课题2常见的酸和碱第1课时》分层作业解析版docx、核心素养人教版化学九年级下册《课题2常见的酸和碱第1课时》分层作业原卷版docx等4份课件配套教学资源,其中PPT共38页, 欢迎下载使用。
1. 以盐酸、硫酸为例,通过实验探究认识酸的主要性质和用途,并能灵活运用酸的性质,解决生活、生产中的实际问题。2.认识酸的腐蚀性及使用时的安全注意事项。3.通过比较、分类、概括的方法,建立物质分类的认识,逐步形成基于物质类别研究物质及其变化的视角。
“酸”最早指“有酸味的酒”。在酿酒的时候,有时把比较珍贵的酒放在窖中保存,酒在微生物的作用下会产生酸味。
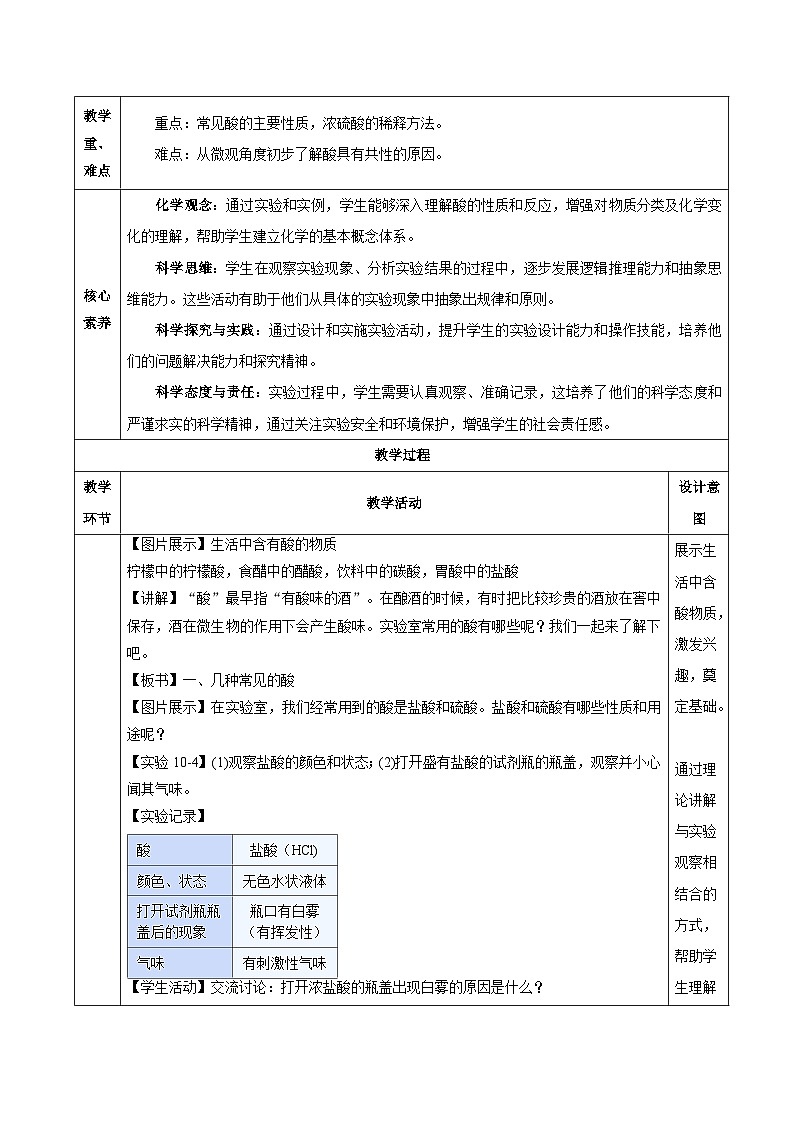
在实验室,我们经常用到的酸是盐酸和硫酸。
盐酸和硫酸有哪些性质和用途呢?
盐酸具有挥发性,浓度越大、温度越高,挥发性越强。
浓盐酸瓶口的白雾是挥发出的氯化氢气体遇到空气中的水蒸气生成的盐酸小液滴。
盐酸是氯化氢气体的水溶液。
思考:实验室制取CO2能否用浓盐酸?
不能,浓盐酸挥发性强,制得的CO2中会混有大量HCl气体。
【实验10-5】浓硫酸的腐蚀性
滴有硫酸的部位变黑甚至形成洞
浓硫酸有强烈的腐蚀性。它能将纸张、木材、布料、皮肤(都由含碳、氢、氧等元素的化合物组成)里的氢、氧按水的组成比脱去,生成黑色的炭,这种作用通常叫脱水作用。
如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后再涂上质量分数为3%~5%的碳酸氢钠溶液。
【实验10-6】浓硫酸的稀释
思考:为什么不能将水注入浓硫酸中呢?
正确操作:把浓硫酸沿着烧杯壁缓缓注入盛有水的烧杯中,并用玻璃棒不断搅拌。
盐酸、硫酸等酸具有非常广泛的用途
浓硫酸具有吸水性(稀硫酸无吸水性),可作气体干燥剂。
交流讨论:分析敞口放置的浓盐酸、浓硫酸的溶液成分变化。
在实验室和化工生产中常用的酸还有硝酸(HNO3)、醋酸(CH3COOH)等。另外,生活中常见的许多物质中也含有酸。
1. 以下关于浓盐酸或浓硫酸的说法正确的是( )A.浓盐酸和浓硫酸都是无色无味的液体B.打开瓶塞,浓盐酸和浓硫酸瓶口会出现白雾C.浓盐酸和浓硫酸长期敞口放置,质量都会变小D.浓硫酸滴到纸张、蔗糖上,会使纸张、蔗糖炭化
2.下列图示的化学实验基本操作中,正确的是( )
【问题与预测】(1)结合课题1的内容,预测稀盐酸、稀硫酸能使石蕊溶液和酚酞溶液分别呈现什么颜色。(2)稀盐酸和稀硫酸是否具有相似的化学性质?
【实验与分析】(1)在白色点滴板上进行实验,观察并记录实验现象。
化学性质1:酸能使紫色石蕊溶液变红,不能使无色酚酞溶液变色。
优点:操作简单、节约药品、显色明显
【实验与分析】(2)写出下面三种金属分别与稀盐酸和稀硫酸反应的化学方程式。
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Mg+H2SO4 = MgSO4+H2↑
Zn+H2SO4 = ZnSO4+ H2↑
Fe+H2SO4 = FeSO4+H2↑
分析:以上反应的生成物有什么共同之处?
化学性质2:通常情况下,酸溶液能与活泼金属(H之前)发生置换反应,生成氢气和该金属的化合物。
【实验与分析】(3)在分别盛有稀盐酸和稀硫酸的试管中各放入生锈的铁钉,过一会儿取出铁钉,用水洗净,铁钉表面和溶液颜色有什么变化?
Fe2O3+3H2SO4 =Fe2(SO4)3 +3H2O
铁锈溶解,溶液由无色变黄色
Fe2O3+6HCl = 2FeCl3 +3H2O
分析:①以上反应的生成物有什么共同之处?
化学性质3:酸能与某些金属氧化物反应生成水和该金属的化合物。注意:反应前后化合价不变!
分析:②利用上面的反应可以清除铁制品表面的锈,除锈时能否将铁制品长时间浸在酸中?为什么?
反应初期:酸溶液与铁锈发生了反应
铁锈消失后:酸溶液又与铁发生了反应
Fe2O3 + 6HCl = 2FeCl3+ 3H2O
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
【结论】根据以上实验与分析,结合前面学过的知识,归纳稀盐酸、稀硫酸等酸有哪些相似的化学性质。
与活泼金属发生置换反应生成氢气
与某些金属氧化物反应生成水
稀盐酸、稀硫酸等酸为什么会有相似的化学性质呢?
【实验10-7】试验物质的导电性
结论:溶液导电说明了溶液中存在着自由移动的带电的粒子。
酸具有相似的化学性质(共性)的原因
酸在水溶液中都能解离出H+和酸根离子
1.草酸是自然界中普遍存在的一种酸,推测它不可能具有的化学性质或用途是 ( )A. 能用于除铁锈B. 能与二氧化碳反应C. 能与酸碱指示剂作用D. 能用于除水壶内的水垢(CaCO3)
2.用足量的盐酸浸泡生锈的铁钉,可观察到的实验现象是( )①铁钉上的铁锈消失;②铁钉上有气泡产生;③溶液呈黄色。A.只有①② B.只有①③ C.只有③ D. ①②③
3.不同的酸具有相似化学性质的原因是( )A.它们都含有酸根B.它们都含有氢元素C.它们溶于水后都能解离出H+D.它们都含有氧元素
4.如图是稀硫酸与不同物质之间发生化学反应的颜色变化
(1)①处所使用的指示剂是 ;
(2)请你在编号②③处各填入一种物质。②是 ;③是 ;
(3)反应②涉及的基本反应类型是 ;
(4)如果想要得到黄色溶液,那么有稀硫酸参与反应的方程式 。
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
与酸碱指示剂作用:使紫色石蕊变红
与活泼金属反应:酸+金属→盐+氢气
与金属氧化物反应:酸+金属氧化物→盐+水
相关课件
这是一份人教版(2024)九年级下册(2024)课题1 化学与人体健康完美版ppt课件,文件包含核心素养人教版化学九年级下册课题1化学与人体健康第2课时同步课件pptx、核心素养人教版化学九年级下册课题1化学与人体健康第2课时分层作业原卷版docx、核心素养人教版化学九年级下册课题1化学与人体健康第2课时分层作业解析版docx等3份课件配套教学资源,其中PPT共31页, 欢迎下载使用。
这是一份人教版(2024)九年级下册(2024)课题1 化学与人体健康一等奖ppt课件,文件包含核心素养人教版化学九年级下册课题1化学与人体健康第1课时同步课件pptx、核心素养人教版化学九年级下册课题1化学与人体健康第1课时分层作业解析版docx、核心素养人教版化学九年级下册课题1化学与人体健康第1课时分层作业原卷版docx等3份课件配套教学资源,其中PPT共34页, 欢迎下载使用。
这是一份初中化学人教版(2024)九年级下册(2024)课题2 常见的酸和碱完美版课件ppt,文件包含核心素养人教版化学九年级下册课题2常见的酸和碱第3课时同步课件pptx、核心素养人教版化学九年级下册课题2常见的酸和碱第3课时同步教案docx、核心素养人教版化学九年级下册《课题2常见的酸和碱第3课时》分层作业原卷版docx、核心素养人教版化学九年级下册《课题2常见的酸和碱第3课时》分层作业解析版docx等4份课件配套教学资源,其中PPT共34页, 欢迎下载使用。









