




所属成套资源:九年级化学人教版(2024)下册同步教学课件
人教版(2024)九年级下册(2024)课题2 溶解度课文内容ppt课件
展开
这是一份人教版(2024)九年级下册(2024)课题2 溶解度课文内容ppt课件,共19页。PPT课件主要包含了固体物质的溶解度,气体的溶解度等内容,欢迎下载使用。
1.能从定性和定量的视角,说明固体溶解度的含义;知道影响气体溶解度的因素。(化学观念)2.能利用物质的溶解性差异,设计物质分离、提纯的方案。(科学探究与实践)3.初步学习绘制和分析溶解度曲线,体验数据处理的过程,学会数据处理的方法。(科学思维)
1.固体物质的溶解度(1)定义:在一定温度下,某固态物质在100 g 溶剂里达到饱和状态时所溶解的质量,叫作这种物质在这种溶剂中的溶解度。若不指明溶剂,通常所说的溶解度是指物质在水里的溶解度。
(1)物质的溶解度会随温度的变化而变化,不指明温度时,溶解度没有意义。(2)规定只有在一定量(100 g)溶剂中达到饱和状态(溶解溶质的最大量)时,所溶解的溶质的量才是一个确定的值。(3)单位:g。
(2)溶解度的含义①已知某物质在一定温度下的溶解度,其含义是指该物质在该温度下,在100 g 溶剂里达到饱和状态时所溶解的质量。②通过溶解度可得到该温度下该物质的饱和溶液中,溶质、溶剂和饱和溶液之间的质量关系,即溶质、溶剂和饱和溶液三者质量比为溶度∶100 g∶ (100 g+溶解度)。
(3)影响固体物质溶解度的因素①内部因素:溶质和溶剂本身的性质(或溶质和溶剂的种类)。②外部因素:温度。
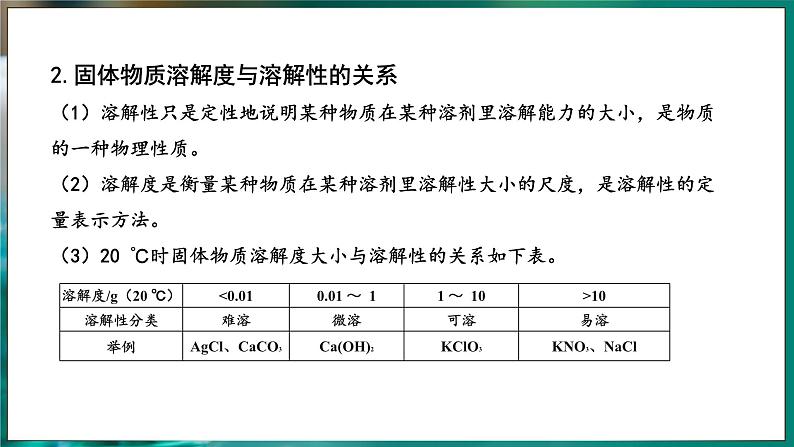
2.固体物质溶解度与溶解性的关系(1)溶解性只是定性地说明某种物质在某种溶剂里溶解能力的大小,是物质的一种物理性质。(2)溶解度是衡量某种物质在某种溶剂里溶解性大小的尺度,是溶解性的定量表示方法。(3)20 ℃时固体物质溶解度大小与溶解性的关系如下表。
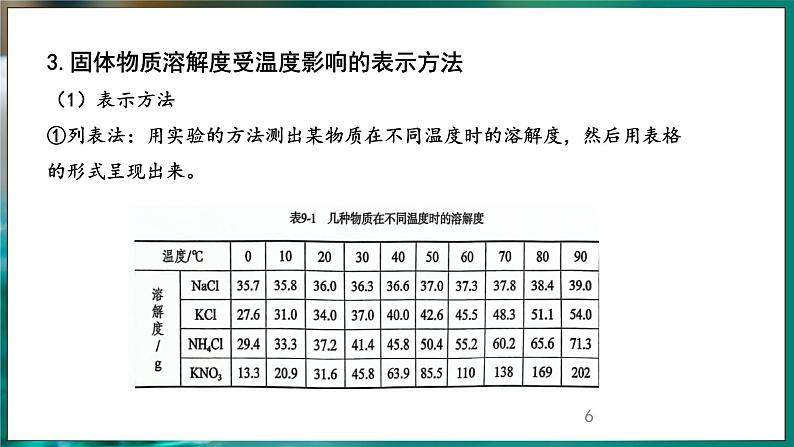
3.固体物质溶解度受温度影响的表示方法(1)表示方法①列表法:用实验的方法测出某物质在不同温度时的溶解度,然后用表格的形式呈现出来。
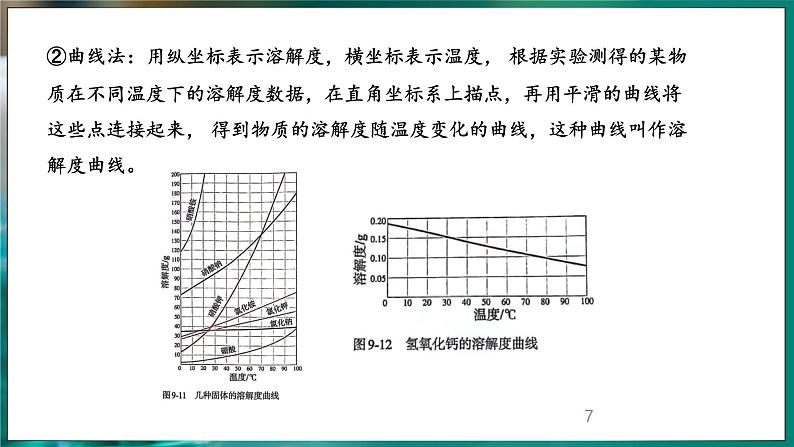
②曲线法:用纵坐标表示溶解度,横坐标表示温度, 根据实验测得的某物质在不同温度下的溶解度数据,在直角坐标系上描点,再用平滑的曲线将这些点连接起来, 得到物质的溶解度随温度变化的曲线,这种曲线叫作溶解度曲线。
(2)溶解度曲线的变化规律大多数固体物质的溶解度随温度的升高而增大,表现在曲线坡度陡增,如KNO3、NH4NO3 等(陡升型)少数固体物质的溶解度受温度变化的影响较小,表现在曲线坡度平缓上升,如NaCl 等(缓升型)极少数固体物质的溶解度随温度升高而减小,表现在曲线坡度下降,如Ca(OH)2 等(下降型)
(3)溶解度曲线的意义
曲线上面的区域表示溶液饱和且有未溶解的固体(按此配成的溶液中固体物质有剩余)。
曲线上的点表示该物质在对应温度时的溶解度。
两曲线的交点表示两物质在对应温度时的溶解度相等。
表示物质在不同温度下的溶解度。
表示物质的溶解度随温度变化的趋势。
曲线下面的区域表示溶液是对应温度下该物质的不饱和溶液。
(4)溶解度曲线的应用
①查出某种物质在某温度时的溶解度。②可以看出物质的溶解度随温度变化的规律。③比较不同物质在同一温度时的溶解度大小。④可以比较不同物质的溶解度受温度变化影响的大小。⑤根据溶解度曲线确定如何制得某温度时该物质的饱和溶液。⑥根据溶解度曲线确定如何通过改变温度实现某物质饱和溶液与不饱和溶液相互转化的方法。⑦根据溶解度曲线确定分离或提纯混合物的方法。
1.概念气体的溶解度是指该气体的压强为101 kPa 和一定温度时,在1 体积水里溶解达到饱和状态时的气体体积。
意义:在压强为101 kPa、温度为0 ℃时,氮气在水中的溶解度为0.024,就是指氮气在压强为101 kPa、温度为0 ℃时,1 体积水里最多能溶解0.024 体积的氮气。
2.影响气体溶解度的因素内部因素:溶质和溶剂本身的性质。外部因素:①温度压强一定时,温度越高,气体的溶解度越小。 ②压强温度一定时,压强越大,气体的溶解度越大。
①打开汽水瓶盖时会有气泡冒出,是因为汽水中溶有大量的CO2,当打开瓶盖时,压强减小,CO2 的溶解度减小,大量的CO2 就会从汽水中逸出形成大量的气泡。②烧水时,刚开始会看到里面有许多小气泡不断上升,是因为溶解在水中的气体(主要为O2)的溶解度随温度的升高而减小,所以会不断冒出气泡。不能用凉开水养鱼就是因为凉开水中溶解的O2 太少,不能供鱼儿呼吸。
3.气体溶解度与固体溶解度的比较
一、固体物质的溶解度 1.固体物质的溶解度 2.固体物质溶解度与溶解性的关系 3.固体物质溶解度受温度影响的表示方法二、气体的溶解度 1.概念 2.影响气体溶解度的因素 3.气体溶解度与固体溶解度的比较
1.20 ℃时,氯化钠的溶解度为36 g。对这句话理解错误的是( )A.20 ℃时,100 g水中最多能溶解氯化钠36 gB.20 ℃时,100 g氯化钠饱和溶液中含氯化钠36 gC.20 ℃时,氯化钠饱和溶液中水与氯化钠的质量比为100∶36D.20 ℃时,将36 g氯化钠溶解于100 g水中,所得溶液为该温度下氯化钠的饱和溶液
2.甲、乙两种物质的溶解度曲线如图所示。下列叙述错误的是( )A.依据溶解度曲线可判断,t2 ℃时甲的溶解度比乙的大B.将t2 ℃时甲的饱和溶液变为不饱和溶液,可采取升温的方法C.将甲、乙的饱和溶液从t2 ℃降到t1 ℃,甲析出晶体的质量比乙多D.t1 ℃时,甲和乙的饱和溶液各100 g,其溶质的质量一定相等
3.下列方法能增加气体物质的溶解度的是( )A.升高温度 B.增加溶质C.加大压强 D.减小压强
4.(1)常温下,打开汽水瓶盖时,汽水会自动喷出来,说明气体在水中的溶解度与 有关。(2)夏天鱼塘中的鱼常常浮在水面呼吸,请从溶解度的角度解释 。
夏天气温高,氧气在水中的溶解度随温度的升高而减小
相关课件
这是一份人教版(2024)九年级下册(2024)课题2 溶解度集体备课ppt课件,共20页。PPT课件主要包含了情境素材1,情境素材2,情境素材3,溶解度,四要素,·标准,·状态,·单位,溶液达到饱和,溶解度单位为“g”等内容,欢迎下载使用。
这是一份人教版(2024)第九单元 溶液课题2 溶解度教课课件ppt,共26页。PPT课件主要包含了情境素材1,情境素材2,情境素材3,氯化钠完全溶解,有部分氯化钠未溶,不饱和溶液,完全溶解,饱和溶液,饱和不饱和溶液,晶体析出等内容,欢迎下载使用。
这是一份人教版(2024)九年级下册(2024)第九单元 溶液课题2 溶解度多媒体教学ppt课件,文件包含第2课时溶解度pptx、固体溶解度mp4、固体溶解度曲线的应用mp4、固体溶解度的表示方法mp4、气体溶解度mp4等5份课件配套教学资源,其中PPT共34页, 欢迎下载使用。









