









主题排查4 化学反应速率与化学平衡 催化机理(讲义+课件 2份打包)2025年高考化学二轮复习
展开
这是一份主题排查4 化学反应速率与化学平衡 催化机理(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查4化学反应速率与化学平衡催化机理pptx、主题排查4化学反应速率与化学平衡催化机理DOC等2份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
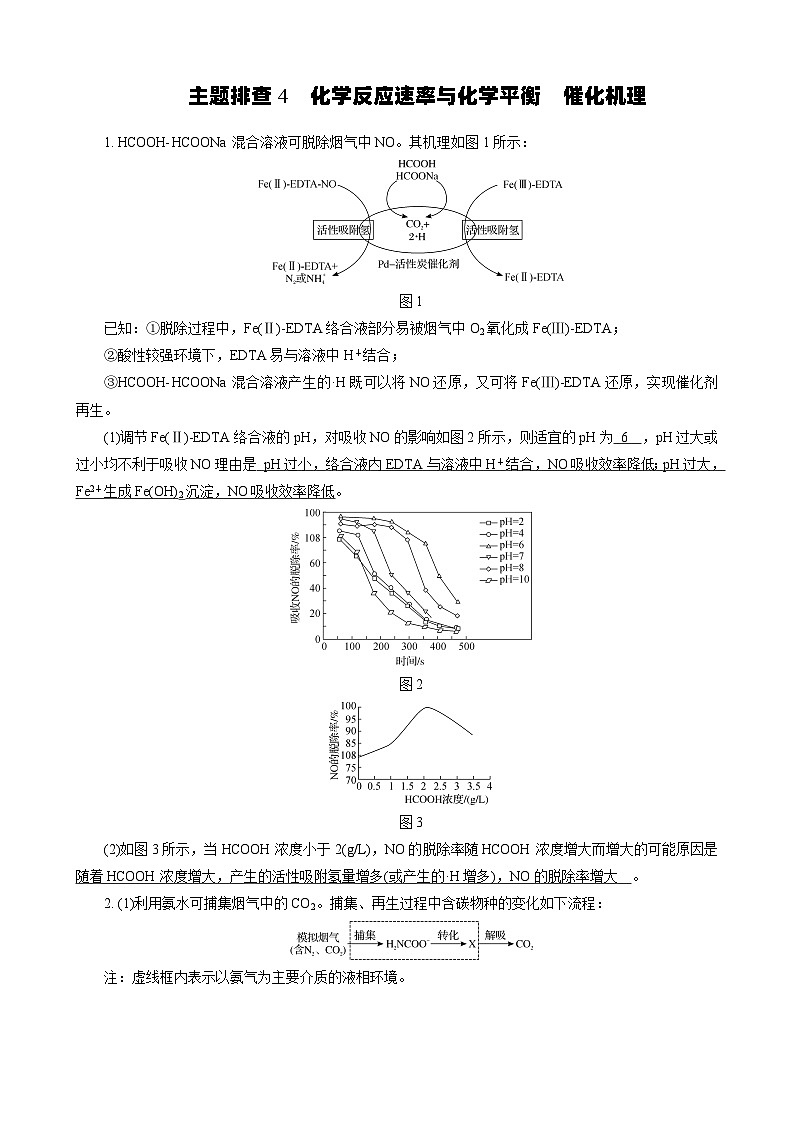
1. HCOOH-HCOONa混合溶液可脱除烟气中NO。其机理如图1所示:
图1已知:①脱除过程中,Fe(Ⅱ)-EDTA络合液部分易被烟气中O2氧化成Fe(Ⅲ)-EDTA;②酸性较强环境下,EDTA易与溶液中H+结合;③HCOOH-HCOONa混合溶液产生的·H既可以将NO还原,又可将Fe(Ⅲ)-EDTA还原,实现催化剂再生。
(1)调节Fe(Ⅱ)-EDTA络合液的pH,对吸收NO的影响如图2所示,则适宜的pH为_________,pH过大或过小均不利于吸收NO理由是__________________________ __________________________________________________________________________________。
pH过小,络合液内EDTA与溶液中H+结合,NO吸收效率降低;pH过大,Fe2+生成Fe(OH)2沉淀,NO吸收效率降低
(2)如图3所示,当HCOOH浓度小于2(g/L),NO的脱除率随HCOOH浓度增大而增大的可能原因是________________________________________________________ ___________________________。
随着HCOOH浓度增大,产生的活性吸附氢量增多(或产生的·H增多),NO的脱除率增大
2. (1)利用氨水可捕集烟气中的CO2。捕集、再生过程中含碳物种的变化如下流程:注:虚线框内表示以氨气为主要介质的液相环境。
C2+可以和更多的NH3配位,更有利于解吸反应正向进行,促进CO2释放
(2)一种负载活性金属原子催化剂可催化还原CO2,在催化剂表面的物质相对能量与反应历程的关系如图1所示。
①反应中催化剂的活性会因为生成CO的不断增多而逐渐减弱,原因是___________________________________________________________________。
CO脱除较难,占据催化剂表面,使催化剂表面活性点位减少
②CH3OH可由中间体X或Y经过如图2所示两步转化得到。X和Y的组成相同,催化剂载体中的活性金属带正电性,Y与活性金属结合后的相对能量低于X。在图3方框内画出Y的结构简式____________。
3. 研究二氧化碳的资源化利用具有重要的意义。(1)CO2催化加氢制CH4是CO2的有机资源转化途径之一。已知发生反应如下:反应Ⅰ. CO2(g)+4H2(g)===CH4(g)+2H2O(g) ΔH1=-164.7 kJ/ml反应Ⅱ. CO2(g)+H2(g)===CO(g)+H2O(g) ΔH2=+41.2 kJ/ml①反应Ⅲ. 2CO(g)+2H2(g)===CO2(g)+CH4(g)的ΔH=__________kJ/ml。
②在密闭容器中,1.01×105 Pa、n起始(CO2)∶n起始(H2)=1∶4时,CO2平衡转化率、在催化剂作用下反应相同时间所测得的CO2实际转化率随温度的变化如图1所示。CO2的平衡转化率在600 ℃之后随温度升高而增大的主要原因是___________ _____________________________________________________________________________________________________________________________________________________________________________________________________________________。
反应Ⅰ的ΔH<0,反应Ⅱ的ΔH>0,温度升高,反应Ⅰ平衡逆向移动,使CO2的平衡转化率减小,反应Ⅱ平衡正向移动,使CO2的平衡转化率增大,600 ℃之后,升高温度,反应Ⅱ的CO2平衡转化率增大的幅度大于反应Ⅰ的CO2平衡转化率减小的幅度
(2)电催化还原法是CO2的有机资源化的研究热点。控制其他条件相同,将一定量的CO2通入盛有酸性溶液的电催化装置中,CO2可转化为有机物,阴极所得产物及其物质的量与电压的关系如图2所示。
①电解电压为U1时,电解时转移电子的物质的量为____________。②电解电压为U2时,阴极由CO2生成甲醇的电极反应式为________________ ____________________。③在实际生产中发现当pH过低时,有机物产率降低,可能的原因是_________ ________________________________________________________________________________________________。
CO2+6e-+6H+===CH3OH+H2O
pH过低时,c(H+)增大,H+在阴极表面得电子,生成的H2增多,CO2被还原为有机物的比例减少,有机物产率降低
②实验中将锰粉、碳酸氢钠和去离子水添加到反应器中,反应一段时间后产生甲酸的速率迅速上升的原因可能是_______________________________。
生成的MnO对反应有催化作用
由k正=1.8k逆可得K=
4. 生物质铁炭纳米材料可以活化过一硫酸盐,降解废水中有机污染物。
②生物质铁炭纳米材料降解有机污染物的机理可描述为_______________ _________________________________________________________________________________________________________________________________。
(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点:____________________________________________________________________________________。
石墨碳层可以增加反应的接触面积;石墨碳层的包裹可以减少铁的渗出,减少二次污染
(3)铁炭纳米材料在不同pH时对有机污染物去除率(C/C0:溶液有机物浓度与初始有机物浓度的比值)的影响如图2所示,pH越小,有机污染物去除率越高的原因:_______________________________________________________________________________________________________________________________________________________________________。
5. 肼(N2H4)及其衍生物的合成与利用具有重要意义。(1)“肼合成酶”以其中的Fe2+配合物为催化中心,可将NH2OH与NH3转化为肼,其反应历程如图所示。
①该反应历程中,步骤Ⅱ、Ⅳ中Fe元素化合价的变化可分别描述为___________________________________________________________________________________。②将NH2OH替换为ND2OD,反应所得产物的化学式为__________________。
该反应历程中,步骤Ⅱ中Fe元素由+2价变成+3价,步骤Ⅳ中Fe元素由+3价变成+2价
(2)在碱性条件下,水合肼(N2H4·H2O)在催化剂Rh(铑)g-C3N4作用下发生如下分解反应:反应Ⅰ. N2H4·H2O===N2↑+2H2↑+H2O反应Ⅱ. 3N2H4·H2O===N2↑+4NH3+3H2O
①催化剂载体g-C3N4可由三聚氰胺(C3H6N6)在空气中焙烧得到。已知C3H6N6具有六元环结构,其结构简式可表示为_____________________。②TOF随c(NaOH)变化的原因是______________________________________ ______________________________________________________________________________________________________________________________________________。
当c(NaOH) 0.75 ml/L时,随c(NaOH)的增大,催化剂活性、H2的选择性均下降,TOF减小
(3)相同条件下,测得CO2诱导肼、甲肼(H2NNHCH3)和偏二甲肼[H2NN(CH3)2]低温反应(均为吸热反应)产物与反应物能量差ΔE、反应速率常数k值(k越大,反应越快)如下表。
①请补充上表所缺反应产物的结构简式:________________。②相较甲肼而言,肼、偏二甲肼与CO2的反应效果不佳的原因分别是______________________________________________________________________。
肼与CO2反应速率相对较慢;偏二甲肼与CO2反应程度相对较小(或反应难度较大)
相关课件
这是一份主题排查8 有机推断与合成(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查8有机推断与合成pptx、主题排查8有机推断与合成DOC等2份课件配套教学资源,其中PPT共20页, 欢迎下载使用。
这是一份主题排查6 归因分析 过程描述(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查6归因分析过程描述pptx、主题排查6归因分析过程描述DOC等2份课件配套教学资源,其中PPT共35页, 欢迎下载使用。
这是一份主题排查5 化学工艺流程(讲义+课件 2份打包)2025年高考化学二轮复习,文件包含主题排查5化学工艺流程pptx、主题排查5化学工艺流程DOC等2份课件配套教学资源,其中PPT共20页, 欢迎下载使用。









