




化学人教版 (2019)第一节 化学反应速率图文ppt课件
展开
这是一份化学人教版 (2019)第一节 化学反应速率图文ppt课件,共15页。PPT课件主要包含了单位时间,生成物浓度的增加,化学反应速率,物质浓度的改变,反应物浓度的减少,均取正值,表达式,mol,smin等内容,欢迎下载使用。
【学习目标与核心素养】
学习目标1、了解化学反应速率的概念及其表示方法2、根据化学反应速率的测定原理设计实验3、学会化学反应速率的测定方法2.证据推理:根据化学反应速率的测定原理设计实验,学会化学反应速率的测定方法,通过对比
核心素养变化观念:能用一定的理论模型发展基于变量关系的证据推理素养。
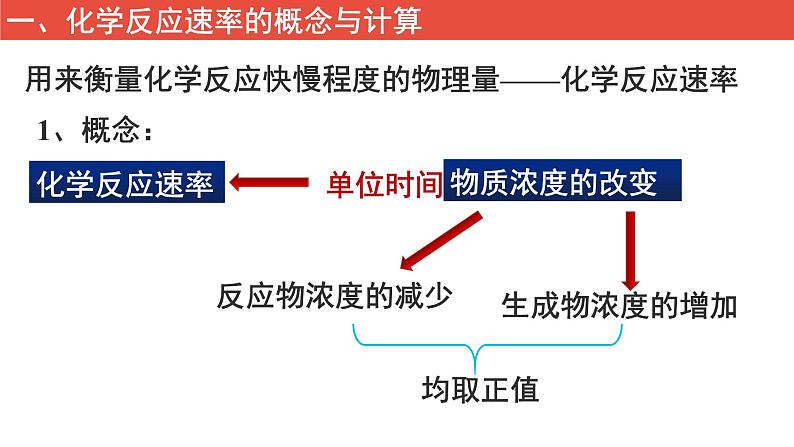
用来衡量化学反应快慢程度的物理量——化学反应速率
一、化学反应速率的概念与计算
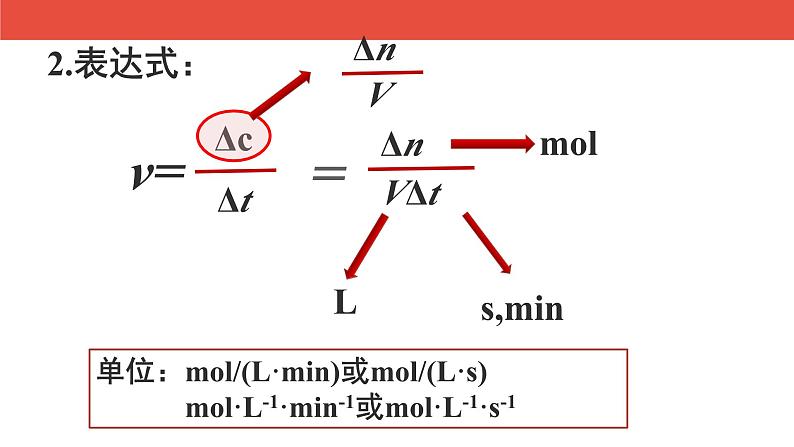
单位:ml/(L·min)或ml/(L·s) ml·L-1·min-1或ml·L-1·s-1
(4) 用不同物质表示的化学反应速率,其值不一定相同,但其表示反应的快慢程度相同——指明具体物质v(A)
(5) 用不同物质表示的化学反应速率之比等于化学计量数之比 反应:mA + nB == pC + qD v(A): v(B): v(C): v(D)=m:n:p:q
(2) 一段时间内的平均速率
(3) 一般不用固体或纯液体表示化学反应速率
(1) 反应速率都为正数
1、判断正误(正确的打“√”,错误的打“x”)。(1)化学反应速率为0.8ml/(L·s)是指1 s时某物质的浓度为0.8 ml/L( )(2)由v计算平均速率,用反应物表示为正值,用生成物表示为负值( )(3)对于化学反应来说,反应速率越大,反应现象就越明显( )(4)可以用单位时间内生成某物质质量的变化量来表示化学反应速率( )(5)同一化学反应中,不同物质表示的化学反应速率可能数值不同,但表示的意义(快慢)相同( )
2、在2L密闭容器中加入1mlN2和3mlH2发生反应 N2 + 3H2 ⇌2NH3 ,2s末时测得容器中含有0.4 mNH3, 求该反应的化学反应速率用不同的物质表示。
c起始 0.5 1.5 0
N2 + 3H2 ⇌2NH3
3、反应 A + 3B = 2C + 2D 在四种不同条件下的反应速率为: (1)v(A)=0.3ml/(L·s) (2)v(B)=0.6ml/(L·s) (3)v(C)=0.4ml/(L·min) (4)v(D)=0.45ml/(L·s) 则该反应速率的快慢顺序为
(1)>(4)>(2)>(3)
①看单位是否统一,若不统一,换算成相同的单位②比较化学反应速率与化学计量数的比值
二、化学反应速率的测量
选择可观测、易操作的变量
找与该物理量化学变化对应的时间
你有哪些方法比较锌粒和1ml/L H2SO4 溶液、4 ml/L H2SO4 溶液化学反应速率的大小?
(1)反应原理:Zn+H2SO4=ZnSO4+H2↑
1.单位时间内收集氢气的体积;2.收集相同体积氢气所需要的时间3.有pH传感器测相同时间内溶液中pH变化,即△c(H+)。4.用传感器测△c(Zn2+)变化。5.测相同时间内△m(Zn)。6.相同时间内恒容压强变化;7.相同时间内绝热容器中温度变化。
用实验法比较化学反应速率大小
结论:质量相同、颗粒大小相同的锌粒分别与1ml/LH2SO4 、4ml/LH2SO4 反应时,与4ml/LH2SO4 反应的速率快,即反应物的浓度越大,反应越快。
1、把下列四种X溶液,分别加进四个盛有10mL浓度为2 ml·L-1 的盐酸的烧杯中,并都加水稀释至50mL,此时,X和盐酸缓慢地进行反应,其中反应速率最大的是( ) A.10 mL、2 ml·L-1 B.20 mL、2 ml·L-1 C.10 mL、4 ml·L-1 D.20 mL、3 ml·L-1
2、在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 ml/L和5.4 ml/L,在一定条件下反应生成NH3,10 min后测得N2的浓度是0.8 ml/L,则在这10 min内NH3的平均反应速率是( )A.0.1 ml·L-1·min-1 B.0.2 ml·L-1·min-1C.0.3 ml·L-1·min-1 D.0.6 ml·L-1·min-1
相关课件
这是一份选择性必修1第一节 化学反应速率教学演示ppt课件,共28页。PPT课件主要包含了化学反应速率的定义,实验探究,实验现象,实验结论,外因外界条件,内因反应物的性质,科学探究实验2-5,较慢产生气泡,冷水中,较快产生气泡等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第一节 化学反应速率背景图ppt课件,共32页。PPT课件主要包含了定义化学反应速率,实验原理,实验用品,简单碰撞理论,基元反应,反应历程反应机理,反应历程又称反应机理,有效碰撞,活化能和活化分子,E1表示反应的活化能等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第一节 化学反应速率评课ppt课件,共27页。PPT课件主要包含了课程目标,催化剂,表面积,压强等,---浓度,实验探究,☂名师点拨,---温度,---催化剂,---压强等内容,欢迎下载使用。










