





高中化学苏教版 (2019)选择性必修1第一单元 化学反应速率示范课ppt课件
展开
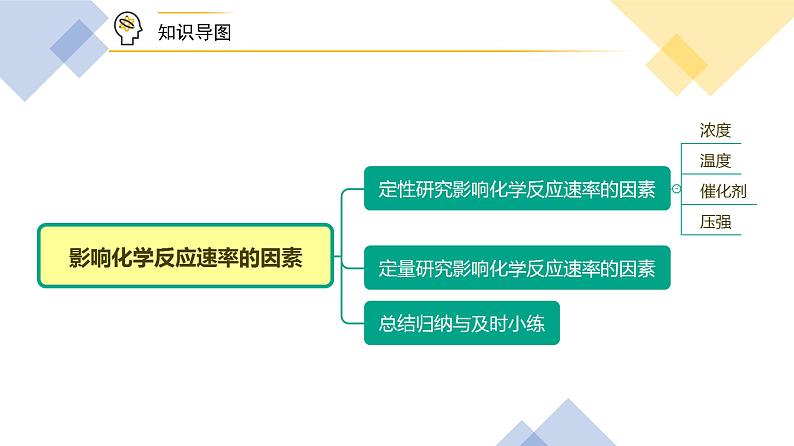
这是一份高中化学苏教版 (2019)选择性必修1第一单元 化学反应速率示范课ppt课件,共28页。PPT课件主要包含了反应物的性质,均变浑浊,先变浑浊,其他条件相同时,没有复燃,实验操作,实验记录等内容,欢迎下载使用。
影响化学反应速率的因素可以分为内因和外因。内因:_______________是决定化学反应速率的重要因素。外因:_______、______、_______、________、固体表面积等。
浓度 温度 压强 催化剂
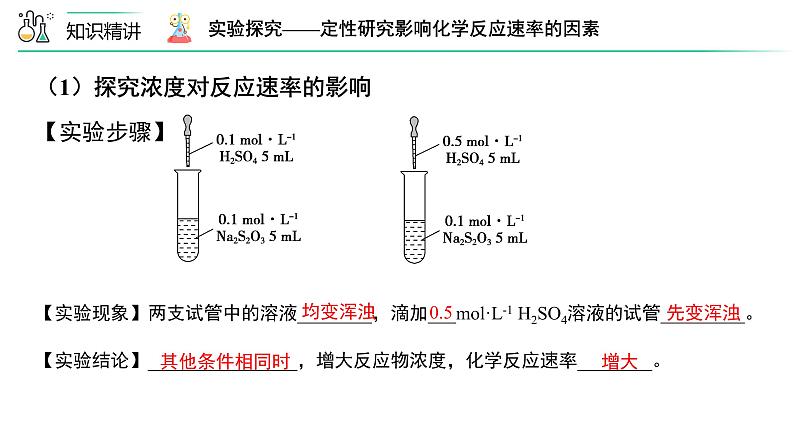
(1)探究浓度对反应速率的影响【实验仪器】烧杯、试管、量筒、试管架、胶头滴管、温度计、秒表。【实验药品】0.1 ml/L Na2S2O3溶液、0.1 ml/L H2SO4溶液、0.5 ml/L H2SO4溶液、5% H2O2溶液、1ml/L FeCl3溶液、蒸馏水、热水。【实验原理】Na2S2O3+H2SO4===____________________________________
Na2SO4+SO2↑+S↓+H2O
(1)探究浓度对反应速率的影响【实验步骤】
【实验现象】两支试管中的溶液________,滴加___ml·L-1 H2SO4溶液的试管_________。
【实验结论】________________,增大反应物浓度,化学反应速率________。
(2)探究温度对反应速率的影响【实验原理】Na2S2O3+H2SO4===Na2SO4+SO2↑+S↓+H2O【实验步骤】
【实验现象】两支试管中的溶液__________,烧杯中装______的试管__________
【实验结论】________________,升高温度,化学反应速率__________。
烧杯中装热水 烧杯中装冷水
(3)探究催化剂对反应速率的影响【实验原理】【实验步骤】
【实验现象】余烬____________ 余烬________
【实验结论】催化剂可以___________化学反应速率。
(4)压强对反应速率的影响
其他条件不变时,对于有气体参与的反应,增大压强(减小容器容积)相当于增大反应物的浓度,化学反应速率增大;减小压强(增大容器容积)相当于减小反应物的浓度,化学反应速率减小。
(1)压强对反应速率的影响,仅针对有气体参与的反应。(2)压强对反应速率的影响,本质是引起浓度的变化:①恒温时,压缩体积→压强增大→气体浓度增大→反应速率增大;②恒温恒容时,充入气体反应物→压强增大→气体反应物浓度增大→反应速率增大; 充入惰性气体→总压强增大→气体浓度不变→反应速率不变。③恒温恒压时,充入惰性气体→压强不变→体积增大→气体浓度减小→反应速率减小。
【实验操作】(1)按下图所示安装装置,在锥形瓶内放入2g锌粒,通过分液漏斗加入40 mL 1 ml/L的稀硫酸,测量收集10 mL H2所用的时间。(2)用4 ml/L的稀硫酸代替1 ml/L的稀硫酸重复上述实验。
【实验结论】4 ml·L-1硫酸与锌反应比1 ml·L-1硫酸与锌反应的速率_______。
①锌粒颗粒大小(表面积)基本相同(控制变量,避免表面积的干扰)。②40 mL的稀硫酸溶液要迅速加入。③装置气密性要好,且计时要迅速、准确。
1.一般情况下,催化剂对反应速率的影响最显著。2.实验表明,温度每升高10℃,反应速率通常增加2 ~ 4倍。3. 一般情况下,温度对化学反应速率的影响比浓度、压强对化学反应速率的影响要大。
思考与交流:一定量的铁粉与过量的盐酸反应,下列措施对生成H2的量及速率有何影响?
【例1】(2021·黑龙江哈尔滨市·哈九中高三开学考试)O3在水中易分解,一定条件下,O3的浓度减少一半所需的时间(t)如表所示。已知:O3的起始浓度为0.0216ml·L—1。下列说法正确的是A.pH增大能加速O3分解,表明对O3分解起催化作用的是H+B.在30℃、pH=4.0条件下,O3的分解速率为1.67×10—6ml(L·s)—1C.根据表中数据可知,O3的分解速率随温度升高而增大,随pH增大而减小D.根据表中数据的递变规律,推测O3在下列条件下分解速率的大小关系为40℃、pH=3.0>30℃、pH=7.0
题型一:影响化学反应速率的因素探究实验
【例2】(2020·浙江温州市·瑞安中学高二期中)为探究催化剂对过氧化氢分解反应速率的影响,某兴趣小组设计如图装置。实验时,通过胶头滴管向容器中各滴入5滴溶液后,每隔10 s观测注射器中气体体积并进行比较。请回答:(1)仪器A的名称是_______。(2)实验前,检验该装置气密性的方法是_______。(3)若甲装置在相同时间内收集到气体体积大于乙装置,能否推测Fe3+对H2O2分解的催化效果比Cu2+的好?_______(填“能”或“不能”),请说明理由_______。
【答案】锥形瓶 塞紧胶塞后,将注射器活塞向外拉出一定距离,一段时间后松开活塞,若能回到原位,则气密性良好 不能 因为所用盐溶液的酸根离子不同,对实验可能产生干扰
【例3】(2021·全国高二课时练习)下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是A.Cu能与浓硝酸反应,但不能与浓盐酸反应B.Cu与浓硝酸反应比与稀硝酸反应快C. 与 在常温、常压下不反应,放电时可反应D.Fe与浓盐酸反应比与稀盐酸反应快
题型二:化学反应速率的影响因素
【例4】(2021·青海海东市·平安一中高二月考)在一密闭容器中充入1 ml H2和1 ml I2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g)=2HI(g)(1)保持容器容积不变,向其中充入1 ml H2,反应速率_________。(2)升高温度,反应速率________。(3)扩大容器体积,反应速率______。(4)保持容器内气体压强不变,向其中充入1 ml H2(g)和1 ml I2(g),反应速率________。(5)保持容器体积不变,向其中充入1 ml N2,反应速率________。(6)保持容器内气体压强不变,向其中充入1 ml N2,反应速率________。
【答案】增大 增大 减小 不变 不变 减小
【例5】(2021·黑龙江哈九中高二开学考试)少量铁粉与100mL0.01ml·L-1的稀盐酸反应,反应速率太慢,为了加快此反应速率而不改变H2的量,可以使用如下方法中的①由铁粉换铁块②加NaNO3固体③将0.01ml·L-1的稀盐酸换成98%的硫酸溶液④加CH3COONa固体⑤加NaCl溶液⑥滴入几滴硫酸铜溶液⑦升高温度(不考虑盐酸挥发)⑧改用100mL0.1ml·L-1盐酸A.③⑤B.①③C.⑥⑦D.⑦⑧
题型三:化学反应速率与反应产量
【例6】(2021·天水市田家炳中学高二月考)将一块质量为5.0 g的铝片投入盛有500 mL 0.5 ml·L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图所示的曲线来表示,回答下列问题:(1)曲线O→a段不产生氢气的原因是_______。(2)曲线a→b段产生氢气的速率较慢的原因是_______。(3)曲线b→c段产生氢气的速率增加较快的主要原因是反应放出的热量使溶液的温度升高而加快反应速率。曲线c点以后产生氢气的速率逐渐下降的主要原因是_______。
题型四:影响化学反应高速率的因素综合
【答案】铝片表面有Al2O3,硫酸首先与Al2O3反应 氧化膜未完全反应掉,铝与硫酸接触的表面积较小 随着反应的进行,硫酸溶液的浓度下降
相关课件
这是一份化学选择性必修1第一单元 化学反应速率课文内容ppt课件,共28页。PPT课件主要包含了m∶n∶p∶q等内容,欢迎下载使用。
这是一份化学第一节 化学反应速率背景图ppt课件,共20页。PPT课件主要包含了影响因素,Mg比Al反应更快,反应物本身的性质,决定因素,有效碰撞理论,分子不接触,分子有接触,分子无规则高速运动,有效碰撞,无效碰撞等内容,欢迎下载使用。
这是一份化学选择性必修1第二章 化学反应速率与化学平衡第一节 化学反应速率教案配套课件ppt,共21页。PPT课件主要包含了分步进行,I·→I2,有效碰撞理论,基元反应,反应机理,自由基,分两步,有效碰撞,碰撞时能量不足,碰撞时取向不合适等内容,欢迎下载使用。










