





高中人教版 (2019)第二节 离子反应精品ppt课件
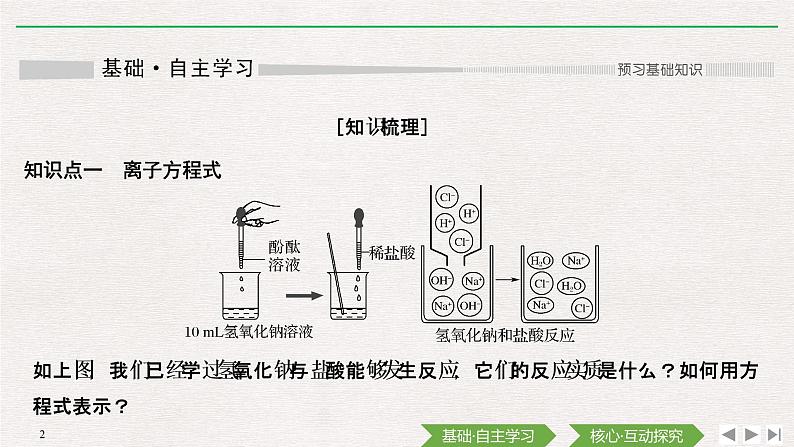
展开如上图,我们已经学过氢氧化钠与盐酸能够发生反应,它们的反应实质是什么?如何用方程式表示?
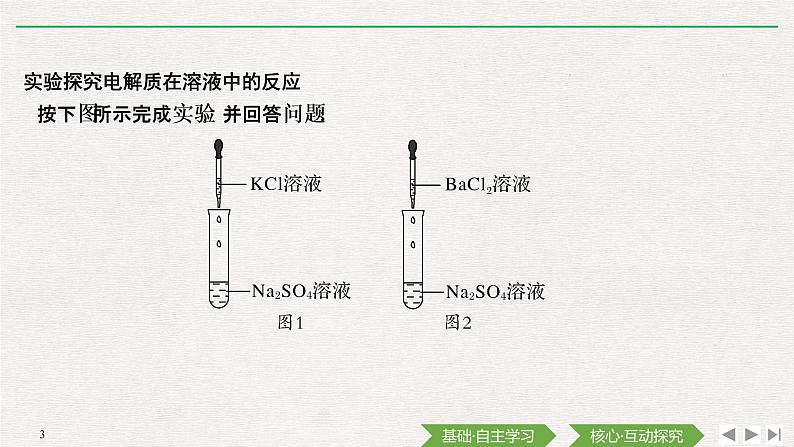
实验探究电解质在溶液中的反应
按下图所示完成实验,并回答问题:
有离子参加或生成的反应
BaCl2+Na2SO4===BaSO4↓+2NaCl
②拆:把易溶于水、易电离的物质拆成离子的形式:_______________________________________________;③删:删去方程式两边不参加反应的离子,并将计量数化为最简整数:_______________________;④查:检查方程式两边各元素的原子个数和电荷总数是否相等、反应条件、沉淀符号、气体符号等。
离子方程式的书写步骤:“写→拆→删→查”。其关键是要将易溶于水、易电离的电解质写成离子的形式,单质、沉淀、气体、难电离的物质(如水、弱酸、弱碱)等写成化学式。
知识点二 离子反应发生的条件
1.两种电解质在溶液中相互交换离子而发生复分解反应。请写出下列复分解反应的离子方程式:
(1)氯化铝溶液和氨水:_________________________________________。
生成难溶的物质,如生成BaSO4、AgCl、CaCO3、Fe(OH)3、Cu(OH)2等沉淀。
(2)碳酸钙和盐酸溶液:____________________________________。
生成气体或易挥发性物质,如生成CO2、SO2、H2S等气体。
(3)硫酸溶液和烧碱溶液:___________________。
生成难电离的物质,如生成H2O等。
锌与盐酸的反应:________________________。
答案 (1)√ (2)× (3)× (4)√ (5)×
微训练1.下列不能发生离子反应的是________。
①NaCl溶液与AgNO3溶液②KNO3溶液与NaOH溶液③稀硫酸与BaCl2溶液④盐酸与Na2CO3溶液⑤Na2CO3溶液与Ca(OH)2溶液⑥NaOH溶液与稀HNO3溶液⑦锌与CuSO4溶液⑧稀H2SO4和NaCl溶液⑨Na2SO4溶液和CuCl2溶液
解析 复分解型离子反应发生的条件是a.生成难溶或微溶物质;b.生成难电离物质(弱酸、弱碱、H2O);c.生成挥发性物质(或气体)。三者满足其一即可发生离子反应,其中①③⑤分别生成AgCl沉淀、BaSO4沉淀、CaCO3沉淀,⑥生成H2O,④生成CO2,⑦Zn与Cu2+发生置换反应,故①③④⑤⑥⑦都能发生离子反应,②⑧⑨不符合离子反应发生的条件,不能发生离子反应。答案 ②⑧⑨
2.根据离子方程式的书写步骤写出CaCO3与稀盐酸反应的离子方程式。
答案 CaCO3+2HCl===CaCl2+H2O+CO2↑CaCO3+2H++2Cl-===Ca2++2Cl-+H2O+CO2↑CaCO3+2H+===Ca2++H2O+CO2↑
答案 (1)H++OH-===H2O(2)Na2CO3+2HCl===2NaCl+CO2↑+H2O(合理即可)
学习任务1 探究溶液中离子反应的实质
为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,实验设计和过程如下:如图所示连接好装置,向烧杯中加入25 mL的Ba(OH)2溶液和2滴酚酞溶液,再一边不断地滴加H2SO4溶液,并轻轻振荡。
(1)实验现象及分析:①溶液颜色变化为__________________________,原因是_____________________________________________________。②灯泡亮度变化:___________________________________________,原因是________________________________________________________。③溶液变浑浊,原因是____________________。(2)实验结论:稀H2SO4与Ba(OH)2溶液反应的实质是_______________________(用离子方程式表示)。
提示 要证实Ba(OH)2和H2SO4溶液的反应是离子反应,则需证明发生反应的离子浓度发生了变化,而离子浓度变化和溶液导电性是有联系的。
1.离子反应发生的条件
2.离子不能大量共存的两类情况
(1)能发生复分解反应。①生成难溶或微溶的物质。如生成BaSO4、AgCl、CaCO3、CaSO4、Ag2SO4、BaCO3、MgCO3、Fe(OH)3等②生成难电离的物质。如生成CH3COOH、HClO、H2O、NH3·H2O等③生成挥发性物质(气体)。如生成CO2、SO2、H2S等。只要具备上述三个条件中的一个,则离子不能大量共存(2)能发生置换反应:金属单质与金属阳离子之间的置换反应,如Fe与CuSO4溶液的反应,实际上是Fe与Cu2+之间的置换反应。
3.离子共存问题中易忽视的三类隐含条件
(3)隐含条件三:碱性环境“强碱性溶液”“使酚酞变红的溶液”“常温下,pH>7的溶液”,一定含有OH-。
【例题1】 加入氢氧化钾溶液之后,溶液中下列离子数目明显减少的是 能与OH-反应的离子?( )
A.硝酸根离子 B.钠离子C.钡离子D.铜离子解析 铜离子与氢氧根反应生成氢氧化铜沉淀。答案 D
变式训练1 在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是 ( )
学习任务2 离子方程式的书写及正误判断
提示 错误。CaCO3难溶于水,不能拆为离子。
2.AgNO3溶液和Cu反应的离子方程式写成Cu+Ag+===Cu2++Ag正确吗?为什么?
提示 错误。该离子方程式电荷不守恒。
1.离子方程式书写及判断的核心
在书写离子方程式和判断离子方程式的正误时要从“两易”“两等”和“两查”入手:
同时满足两个条件的物质才能改写为离子形式,否则用化学式表示
2.“六看”判断离子方程式的正误
3.书写离子方程式时的拆分原则
(1)强酸、强碱和易溶于水的盐改写成离子形式,难溶物质、难电离物质、易挥发物质、单质、氧化物、非电解质等均写化学式。(2)改写微溶物时要看清题目要求:①作为反应物,若是澄清溶液写离子符号,若是悬浊液写化学式。②作为生成物,一般写化学式(标↓号)。(3)氨水作反应物写NH3·H2O;作生成物,若有加热条件或浓度很大时,可写NH3(标↑号)+H2O;若是稀溶液且不加热时,可写成NH3·H2O。
【例题2】 能正确表示下列化学反应的离子方程式的是( )
A.氢氧化钡溶液与硫酸的反应:OH-+H+===H2OB.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+===Ca2++2H2OC.铜片插入硝酸银溶液中:Cu+Ag+===Cu2++AgD.碳酸钙溶于稀盐酸中:CaCO3+2H+===Ca2++H2O+CO2↑
变式训练2 下列离子方程式正确的是( )
A.铜与硝酸银溶液反应Cu+Ag+===Cu2++AgB.CH3COOH溶液与NaOH溶液反应H++OH-===H2OC.碳酸镁与稀H2SO4反应MgCO3+2H+===Mg2++H2O+CO2↑D.石灰乳与稀盐酸反应H++OH-===H2O
解析 A项,电荷不守恒,应为Cu+2Ag+===2Ag+Cu2+;B项,CH3COOH应写成分子形式,应为CH3COOH+OH-===CH3COO-+H2O;D项,石灰乳应写成化学式,应为Ca(OH)2+2H+===Ca2++2H2O。答案 C
学习任务3 (核心素养)与量有关的离子方程式书写
在化学反应中,有时反应物的量不同,发生的反应不同,生成物不同,在书写离子方程式时要注意量的关系。
【素养解题】[典例示范] 写出下列反应的离子方程式:
(1)少量的NaHCO3与Ca(OH)2溶液的反应:_____________________________________________________________________________________。(2)少量的Ca(OH)2溶液与NaHCO3的反应: ______________________________________________________________________________________。
[与量有关的离子方程式书写解题思维模型]
(1)通过实验Ⅰ可以证明_______________________________________。(2)要证明另外两种粒子能否溶解氧化铜,还需要进行实验Ⅱ和Ⅲ,在Ⅱ中加入稀硫酸后氧化铜溶解,则进一步确认的实验操作是:在Ⅲ中先加入________,再加入________。(3)探究结果为________________________________________。(4)反应的离子方程式为________________________________。
高中化学人教版 (2019)必修 第一册第一章 物质及其变化第二节 离子反应图片ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第一章 物质及其变化第二节 离子反应图片ppt课件,共13页。PPT课件主要包含了学习目标,情境导入,学习任务,学习活动,对比实验1,对比实验2,练习与测评等内容,欢迎下载使用。
人教版 (2019)必修 第一册第二节 离子反应完美版ppt课件: 这是一份人教版 (2019)必修 第一册第二节 离子反应完美版ppt课件,共26页。PPT课件主要包含了离子反应,离子方程式,本节重点,本节难点,无明显现象,有白色沉淀产生,Cl-,离子之间,或熔融状态,没有离子的减少等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第一章 物质及其变化第二节 离子反应一等奖课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第一章 物质及其变化第二节 离子反应一等奖课件ppt,共27页。













