

2017-2018学年广西陆川县中学高二上学期期中考试化学试题
展开2017-2018学年广西陆川县中学高二上学期期中考试
化学试题
第I部分 选择题(共48分)
一、选择题(本题包括16小题,每题3分,共48分)
1. 2015年11月30日至12月11日,世界各国领导人在巴黎共同商讨如何应对气候变化、提升经济绿色水平,实现人类可持续发展。要想提升经济绿色水平下列属于最有希望的新能源是( )
①天然气 ②煤 ③石油 ④水能 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能
A.①②③④ B.⑤⑥⑦⑧C.③④⑤⑥ D.除①②外
2.下列说法正确的是( )
A.反应热就是反应中放出的能量
B.已知某反应的焓变小于零,则反应产物的焓大于反应物的焓
C.由C(石墨)―→C(金刚石) ΔH=+1.9 kJ/mol,可知,金刚石比石墨稳定
D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
3..下列物质的溶液经加热、蒸发、浓缩、结晶、灼烧后,所得固体的成分不相同的是( )
A.FeCl2、FeCl3 B.NaHCO3、Na2CO3
C.NaAlO2、AlCl3 D.Mg(HCO3) 2、MgCl2
4.下图是某种酶生物燃料电池的工作原理示意图。下列说法中不正确的是
A.葡萄糖是还原剂
B.外电路中电子由A极移向B极
C.溶液中H+ 由B极区移向A极区
D.B极电极反应式为:H2O2 +2H++2e-=== 2H2O
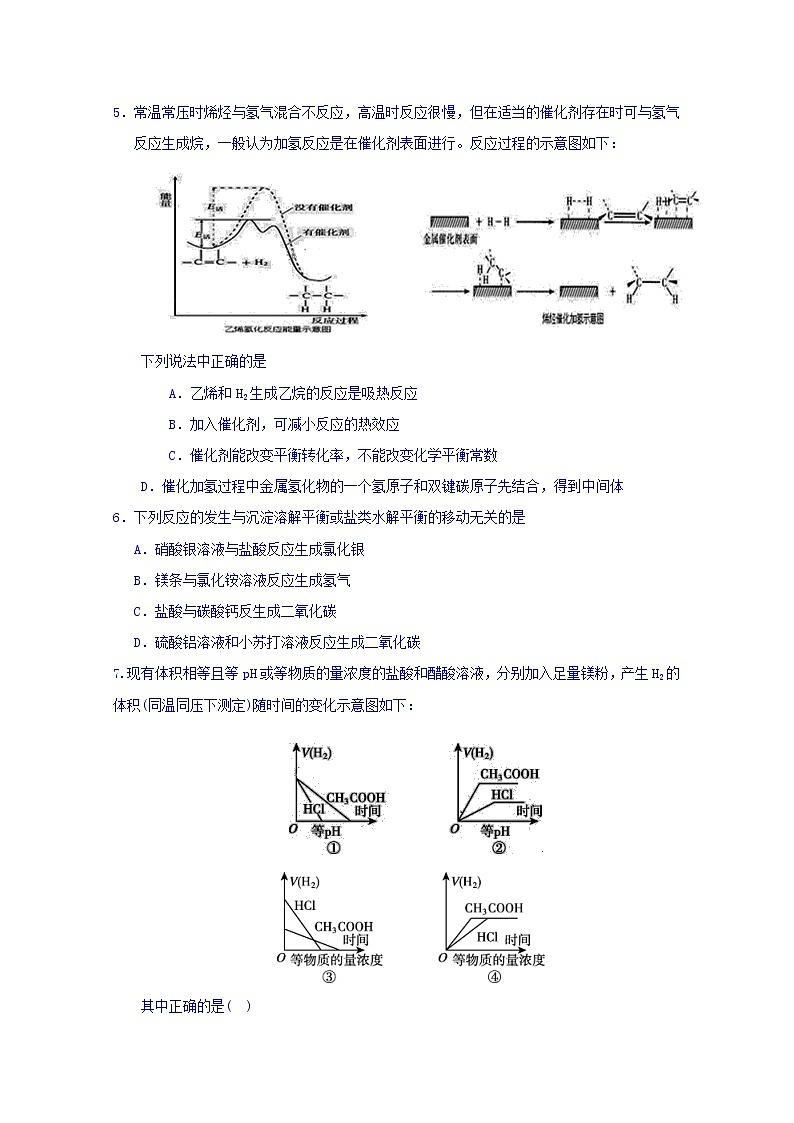
5.常温常压时烯烃与氢气混合不反应,高温时反应很慢,但在适当的催化剂存在时可与氢气反应生成烷,一般认为加氢反应是在催化剂表面进行。反应过程的示意图如下:
下列说法中正确的是
A.乙烯和H2生成乙烷的反应是吸热反应
B.加入催化剂,可减小反应的热效应
C.催化剂能改变平衡转化率,不能改变化学平衡常数
D.催化加氢过程中金属氢化物的一个氢原子和双键碳原子先结合,得到中间体
6.下列反应的发生与沉淀溶解平衡或盐类水解平衡的移动无关的是
A.硝酸银溶液与盐酸反应生成氯化银
B.镁条与氯化铵溶液反应生成氢气
C.盐酸与碳酸钙反生成二氧化碳
D.硫酸铝溶液和小苏打溶液反应生成二氧化碳
7.现有体积相等且等pH或等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁粉,产生H2的体积(同温同压下测定)随时间的变化示意图如下:
其中正确的是( )
A.①③ B.②④ C.①②③④ D.都不对
8.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:
2N2O5(g) 4NO2(g) + O2(g) △H =+Q kJ/mol (Q>0)
某温度下,向2L的密闭容器中通入N2O5,部分实验数据见下表:
时间/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/mol/L | 5.0 | 3.5 | 2.5 | 2.5 |
下列说法正确的是
A.500s内N2O5分解速率为6×10-3mol/(L·s)
B.该温度下的平衡常数K =125
C.反应达平衡时,吸收的热量为5Q kJ
D.其他条件不变,若开始时c(N2O5)=10mol/L,则达平衡后c(N2O5)=5mol/L
9.科学家用氮化镓材料与铜组装如图所示人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4。下列说法不正确的是
A.该过程是将太阳能转化为化学能的过程
B.GaN表面发生氧化反应:2H2O-4 e-=== O2↑+4H+
C.Cu表面的反应是:CO2+8e-+6H2O === CH4+8OH¯
D.H+透过质子交换膜从左向右迁移
10.电解质溶液的电导率越大,导电能力越强。用0.100mol/L的NaOH溶液滴定10.00mL浓度均为0.100mol/L的盐酸和CH3COOH溶液。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是
A.曲线①代表滴定CH3COOH溶液的曲线
B.A、C两点对应溶液均呈中性
C.B点溶液中:c(Na+) > c(OH-) > c(CH3COO-)
D.A点溶液中:c(CH3COO-)+c(OH-)-c(H+)=0.050mol/L
11.下列各项关系中正确的是( )
A.0.1mol/LNa2SO3溶液中:c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3)=0.2mol/L
B.常温下pH=a的稀H2SO4与pH=b的氨水等体积混合后恰好完全反应,则a+b<14
C.0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合:c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH)
D.pH相同的三种溶液①NH4Cl ②(NH4)2SO4 ③NH4HSO4,c(NH4+)大小关系为:①>②>③
12.在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) 3Z(g) ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是( )
A. Q点时,Y的转化率最大
B.W点X的正反应速率等于M点X的正反应速率
C.升高温度,平衡常数增大
D.温度一定,平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
13.常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,溶液的pH
随溶液体积变化的曲线如图所示,则下列叙述正确的是
A. b、c两点溶液的导电能力b>c
B.用等浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,
消耗盐酸体积Vb>Vc
C. c点溶液中c( H十)=c ( OH一)+c(CH3COOH)
D. a、b、c三点溶液中水的电离程度a>c>b
14.关于室温下下列溶液的说法不正确的是( )
编号 | ① | ② | ③ | ④ |
溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
pH | 11 | 11 | 3 | 3 |
A.水的电离程度:①=②=③=④
B.分别加水稀释10倍,溶液的pH:①>②>③>④
C.①③两溶液等体积混合:c(Cl-)>c(NH)>c(H+)>c(OH-)
D.V1 L溶液②与V2 L溶液③混合,若V1∶V2=9∶11,则混合溶液pH=4(忽略溶液体积变化)
15.将0.2 mol•L-1NaHCO3溶液与0.1 mol•L-1KOH溶液等体积混合,下列粒子浓度关系正确的是( )
A.c(K+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B.c(Na+)>c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)
C.c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.1mol•L-1
D.3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
16.己知:Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,Ksp(Ag2CrO4)=2.0×10-12,则下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl >AgI> Ag2CrO4 B.AgCl> Ag2CrO4 >AgI
C.Ag2CrO4>AgCl >AgI D.Ag2CrO4>AgI >AgCl
第Ⅱ卷(非选择题,共52分)
二、非选择题(本题包括4小题,共52分)
17.(14分)原子序数依次增大的A、B、C、D、E、F六种元素。其中A的基态原子有3个不同的能级,各能级中的电子数相等;C的基态原子2p能级上的未成对电子数与A原子的相同;D为它所在周期中原子半径最大的主族元素;E和C位于同一主族,F的原子序数为29。
(1)F基态原子的核外电子排布式为______________________。
(2)在A、B、C三种元素中,第一电离能由小到大的顺序是___________(用元素符号回答)。
(3)元素B的简单气态氢化物的沸点___________(填“高于”或“低于”)元素A的简单气态氢化物的沸点,其主要原因是______________________。
(4)由A、B、C形成的离子CAB−与AC2互为等电子体,则CAB−的结构式为___________。
(5)由B、C、D三种元素形成的化合物晶体的晶胞如图所示,则该化合物的化学式为___________。
(6)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因______________________。
18. (16分)卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于元素周期表的 区;溴的价电子排布式为 .
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是 .
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是 .
| 氟 | 氯 | 溴 | 碘 |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图1、2所示:
请比较二者酸性强弱:HIO3 H5IO6(填“>”、“<”或“=”).
(5)已知ClO2﹣为角型,中心氯原子周围有四对价层电子.写出一个ClO2﹣的等电子体 .
(6)图3为碘晶体晶胞结构.有关说法中正确的是 .
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图4)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为 .
19.(10分)乙醇是生活中常见的物质,用途广泛,其合成方法和性质也具有研究价值。
I.直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。
碱性乙醇燃料电池 酸性乙醇燃料电池 熔融盐乙醇燃料电池
(1)三种乙醇燃料电池中正极反应物均为 。
(2)碱性乙醇燃料电池中,电极a上发生的电极反应式为 ,使用空气代替氧气,电池工作过程中碱性会不断下降,其原因是 。
(3)酸性乙醇燃料电池中,电极b上发生的电极反应式为 ,通过质子交换膜的离子是 。
(4)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO32-向电极
(填“a”或“b”)移动,电极b上发生的电极反应式为 。
II.已知气相直接水合法可以制取乙醇:H2O(g) + C2H4(g) CH3CH2OH(g)。当n(H2O)︰n(C2H4)=1︰1时,乙烯的平衡转化率与温度、压强的关系如下图:
(1)图中压强P1、P2、P3、P4的大小顺序为: ,理由是:
______________________________________________________________________。
(2)气相直接水合法采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290 ℃,压强6.9MPa,n(H2O)︰n(C2H4)=0.6︰1。该条件下乙烯的转化率为5℅。若要进一步提高乙烯的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有 。
20.(12分)下图表示从废旧普通锌锰电池内容物中回收制备KMnO4等物质的一种工艺(不考虑废旧电池中实际存在的少量其他金属)。
(1)KMnO4稀溶液是一种常用消毒剂,其消毒机理与下列物质相似的是 (填序号)
A.双氧水 B.75%酒精 D.84消毒液(NaClO溶液)
(2)①黑色固体混合物水浸时为提高浸出速率,常采用的措施为 (答出两条即可)。
②滤渣水洗灼烧后固体是一种黑色的化合物,操作a中得到熔块的主要成分是K2MnO4和KCl,该过程中发生反应的化学方程式为: 。
③图中产物A是一种难溶于水的黑色固体,其化学式为: 。
(3)测定KMnO4产品的纯度可用标准Na2S2O3溶液进行滴定。
①配制250 mL 0.100 0 mol·L-1标准Na2S2O3溶液,需要使用的玻璃仪器有烧杯、胶头滴管、量筒和 、 ;
②取上述制得的KMnO4产品0.700 0 g,酸化后用0.100 0 mol·L-1标准Na2S2O3溶液进行滴定,滴定至终点记录实验消耗Na2S2O3溶液的体积,重复步骤②,三次平行实验数据如下表。
实验次数 | 1 | 2 | 3 |
消耗Na2S2O3溶液体积/mL | 19.30 | 20.98 | 21.02 |
(有关离子方程式为:MnO4-+S2O32-+H+—SO42-+Mn2++H2O,未配平
将0.100 0 mol·L-1标准Na2S2O3溶液盛装在 (填“酸式”或“碱式”)滴定管中进行滴定。计算该KMnO4产品的纯度 。
化学答案
1.B 2.D 3. C 4. C 5. D 6. A 7. D 8. B 9. C 10. B
11. B 12. A 13. D 14. C 15.D 16.C
17.(1)1s22s22p63s23p63d104s1或3d104s1
(2)C<O<N
(3)高于 NH3分子之间存在氢键,而CH4分子间的作用是范德华力,氢键比范德华力更强
(4)[N=C=O]−
(5) NaNO2
(6) Cu+外围电子3d10轨道全充满稳定,Cu2+外围电子3d9轨道电子非全充满状态不稳定
解析:A的基态原子有3个不同的能级,各能级中的电子数相等,因此A的核外电子排布式为1s22s22p2,即A为C,C的基态原子2p能级上的未成对电子数与A原子的相同,则C为O,则B为N,E和C位于同一主族,则E为S,D为所在周期中原子半径最大的主族元素,即D为Na,F的原子序数为29,则F为Cu,(1)F为ds区,因此核外电子排布式为:1s22s22p63s23p63d104s1或3d104s1;(2)同周期从左向右第一电离能增大,但IIA>IIIA、VA>VIA,第一电离能大小顺序是N>O>C;(3)B的氢化物是NH3,A的简单氢化物是CH4,NH3分子之间存在氢键,而CH4分子间的作用是范德华力,氢键比范德华力更强;(4)CAB-的化学式为OCN-,AC2的化学式为CO2,两者为等电子体,它们的结构相似,因此OCN-的结构式为:[N=C=O]− ;(5)形成的化合物是CS2,结构式为S=C=S,杂化轨道数等于价层电子对数,即C的杂化类型为sp;(6)根据半径大小,打黑球是Na,大黑球位于晶胞的棱上,因此真正属于晶胞的个数为8×1/4=2,大白球为N,小白球为O,两者形成离子是NO2-,其位于顶点和体心,真正的个数为8×1/8=1=2,因此化学式为NaNO2;(7)FC为CuO,F2C为Cu2O,Cu的核外电子排布式1s22s22p63s23p63d104s1,Cu2+的电子排布式为1s22s22p63s23p63d9,Cu+的电子排布式为1s22s22p63s23p63d10,根据洪特规则,处于半满、全满、全空,相对稳定,原因是Cu+外围电子3d10轨道全充满稳定,Cu2+外围电子3d9轨道电子非全充满状态不稳定。
18.(1)配位键(2分)
(2)BH4-或BeH42-(2分)(3)sp2和sp3(共2分) 12(2分) (4)cd(2分)
试题分析:(1)溴化铜(Ⅱ)甲基咪唑中Cu2+与1-甲基咪唑间形成的化学键称为配位键;Br的原子序数是35,Br-基态核外电子排布式为[Ar]3d104s24p6或1s22s22p63s23p63d104s24p6。
(2)原子数和价电子数分别都相等的互为等电子体,则与NH4+互为等电子体的阴离子为BH4-或BeH42-。
(3)MIm中碳原子既有甲基,还有形成碳碳双键的碳原子,其杂化轨道类型为sp2和sp3;单键都是键,双键中还含有一个键,则1molMIm中含键数目为12mol。
(4)a.该晶胞中含有4个铜原子,溴原子的个数是8×1/8+6×1/2=4,所以化合物的化学式为CuBr,a错误;b.铜的配位数为4,b错误;c.与每个Br紧邻的Br有12个,c正确;d.由图中P点和Q点的原子坐标参数,可确定R点的原子坐标参数为(,,),d正确。答案选cd;
19.(10分)(每空1分)
Ⅱ.(1)氧气(2)C2H5OH+16OH--12e-2CO32-+11H2O
空气中的CO2会与KOH溶液反应,降低溶液的碱性,同时反应中也会消耗KOH。
(3)3O2+12H+ +12e-6H2O, H+
(4)a O2+ 2CO2 +4e-2CO32-
Ⅲ.(1)P4>P3>P2>P1
反应为气体体积减小的反应,增大压强平衡正向移动,乙烯的转化率增大,所以相同条件下,转化率越大的代表压强越大。
(2)增加H2O(g)的量、移出生成物。
20. (12分)(除标明外各2分)
(1)AD
(2)①加热、将固体混合物粉碎、搅拌(2分,答出其中一条得1分,其他合理答案均可)
② 3MnO2 + KClO3 + 6KOH 3K2MnO4 +KCl+3H2O(2分,熔融也可用加热、高温,没有扣1分)
③ MnO2(1分)
(3)①玻璃棒(1分)、250mL容量瓶(1分) ②碱式 (1分) 75.84%








