

(杭州专版)2020中考化学复习方案课时训练08盐和化肥
展开课时训练(八) 盐和化肥
(限时:45分钟)
|基础过关|
1.[2018·龙东]小明发现自家农田里的作物叶色发黄,并且茎秆软弱容易倒伏,他应该施用下列化肥 ( )
A.KNO3 B.CO(NH2)2 C.K2CO3 D.Ca3(PO4)3
2.下列是关于久置于空气中的NaOH固体的相关实验分析(不考虑水分),其中合理的是 ( )
序号 | 实验目的 | 实验方案 |
① | 证明变质 | 取少量固体,加水溶解,滴加足量稀盐酸,观察是否有气泡产生 |
② | 确定成分 | 取少量固体,加入石灰水,过滤,向滤液中滴加酚酞试液 |
③ | 测定纯度 | 取a g样品与足量氯化钡溶液充分反应,将沉淀过滤、洗涤、干燥,得到m g固体 |
④ | 除去杂质 | 取固体,加水溶解,滴加氯化钙溶液至恰好完全反应,过滤 |
A.①② B.①③ C.②④ D.③④
3.能证明“CaCO3并非绝对不溶于水”的实验事实是 ( )
A.向少许CaCO3粉末加入NaOH溶液充分振荡,无明显现象
B.向少许CaCO3粉末加入过量稀盐酸充分振荡,粉末消失且有气泡产生
C.向2颗蚕豆粒般大小的石灰石固体加入3 mL蒸馏水,滴入酚酞试液片刻内不变红
D.向少许CaCO3粉末加入3 mL蒸馏水充分振荡,滴入酚酞试液即变红
4.下列所示用品的有效成分及用途对应错误的是 ( )
选项 | A | B | C | D |
用品 | ||||
有效成分 | NaCl | CO(NH2)2 | C12H22O11 | Ca(OH)2 |
用途 | 作调味品 | 作复合肥 | 作甜味剂 | 改良酸性土壤 |
5.小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现如图HK8-1所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是 ( )
图HK8-1
A.HCl NaOH BaCl2 Na2SO4
B.HCl Ba(OH)2 Na2SO4 BaCl2
C.H2SO4 Ba(OH)2 Na2SO4 BaCl2
D.H2SO4 NaOH BaCl2 Na2SO4
6.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
n(H+)与n(OH-)的相对大小 | 溶液的酸碱性 |
n(H+)>n(OH-) | 酸性 |
n(H+)=n(OH-) | 中性 |
n(H+)<n(OH-) | 碱性 |
(1)常温下测得水中pH=7,可知水中n(H+) (填“>”“<”或“=”,下同)n(OH-).
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是 ,原因是该溶液中n(H+)
n(OH-).
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+) n(OH-).
7.含有相同离子的盐具有相似的性质.
(1)CuSO4溶液和FeSO4溶液都含有大量的
(填离子符号).
(2)向FeSO4溶液中加入BaCl2溶液,充分振荡,反应的化学方程式为 .
(3)向CuSO4溶液中加入光亮的过量镁条,充分反应后,可观察到的现象是 .
图HK8-2表示该反应前后溶液中存在的主要离子,请写出反应后溶液中“○”代表的离子符号: .
图HK8-2
(4)除上述实验外,在溶液中与FeSO4和CuSO4均能反应的物质还有 (填序号).
A.NaOH B.Fe C.Ba(NO3)2 D.MgCl2
8.[2018·绥化改编]海洋中有丰富的水生生物和化学资源.海水晒盐能得到粗盐和苦卤,粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等).请回答下列问题.
图HK8-3
(1)若要去除粗盐中可溶性的杂质氯化镁和氯化钙,可依次加入过量的X和碳酸钠两种溶液.下列物质中,可作为X的物质有 .
A.KOH B.Ba(OH)2 C.Ca(OH)2 D.NaOH
(2)操作Ⅱ后向所得滤液中加入适量的盐酸,其目的是 ,最后通过蒸发结晶得到较为纯净的氯化钠.
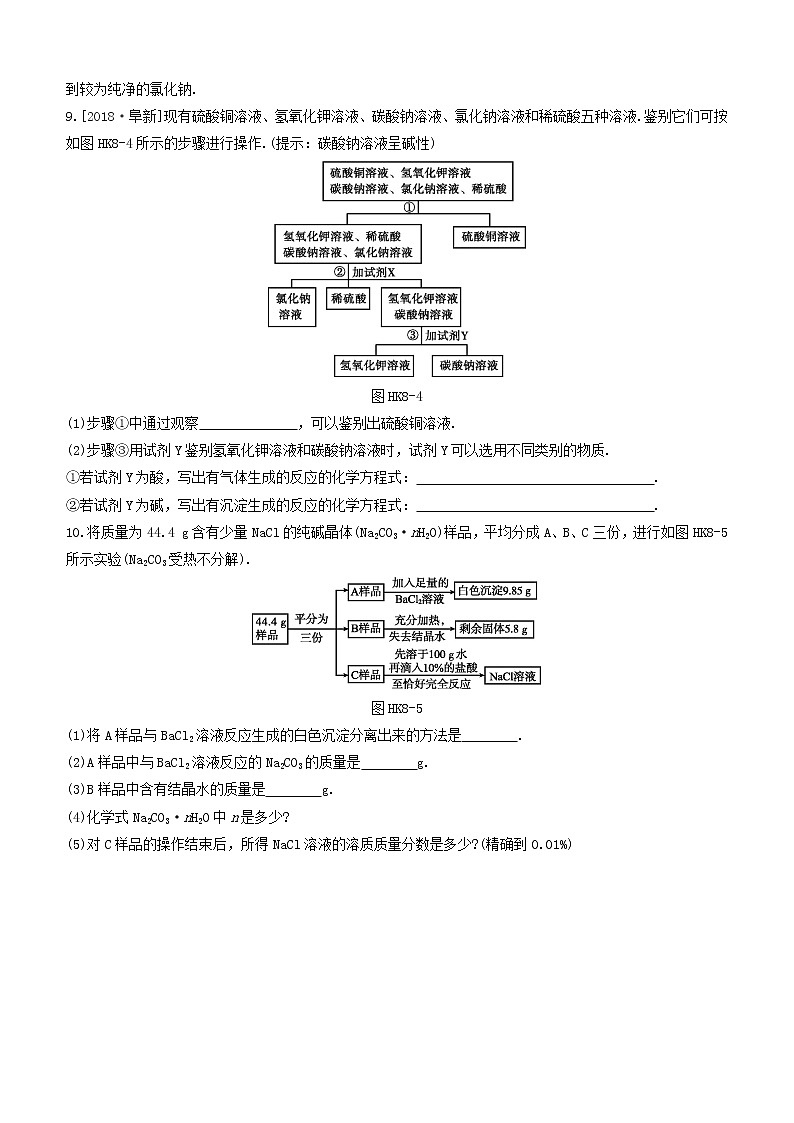
9.[2018·阜新]现有硫酸铜溶液、氢氧化钾溶液、碳酸钠溶液、氯化钠溶液和稀硫酸五种溶液.鉴别它们可按如图HK8-4所示的步骤进行操作.(提示:碳酸钠溶液呈碱性)
图HK8-4
(1)步骤①中通过观察 ,可以鉴别出硫酸铜溶液.
(2)步骤③用试剂Y鉴别氢氧化钾溶液和碳酸钠溶液时,试剂Y可以选用不同类别的物质.
①若试剂Y为酸,写出有气体生成的反应的化学方程式: .
②若试剂Y为碱,写出有沉淀生成的反应的化学方程式: .
10.将质量为44.4 g含有少量NaCl的纯碱晶体(Na2CO3·nH2O)样品,平均分成A、B、C三份,进行如图HK8-5所示实验(Na2CO3受热不分解).
图HK8-5
(1)将A样品与BaCl2溶液反应生成的白色沉淀分离出来的方法是 .
(2)A样品中与BaCl2溶液反应的Na2CO3的质量是 g.
(3)B样品中含有结晶水的质量是 g.
(4)化学式Na2CO3·nH2O中n是多少?
(5)对C样品的操作结束后,所得NaCl溶液的溶质质量分数是多少?(精确到0.01%)
|走进重高|
1.有一包白色固体,可能含有Na2SO4、Na2CO3、Ba(NO3)2、NaCl中的一种或几种,取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,沉淀的质量、产生气体的质量与加入盐酸体积的关系如图HK8-6所示,由此推断白色固体中 ( )
图HK8-6
A.可能存在NaCl
B.可能存在Na2SO4
C.肯定不存在BaCl2
D.肯定只存在Na2CO3
2.CaCO3在生产生活中有广泛的用途.
(1)煅烧石灰石可制得活性CaO,反应的化学方程式为 .为测定不同煅烧温度对CaO活性的影响,取石灰石样品分为三等份,在同一设备中分别于800 ℃、900 ℃和1 000 ℃条件下煅烧,所得固体分别与等质量的水完全反应,测得反应液温度随时间的变化如图HK8-7所示.可知:CaO与水反应会
(填“放出”或“吸收”)热量;上述温度中, ℃煅烧所得CaO活性最高.要得出正确结论,煅烧时还需控制的条件是 .
图HK8-7
(2)以电石渣[主要成分为Ca(OH)2,还含有少量MgO等杂质]为原料制备高纯CaCO3的流程如下:
图HK8-8
①如图HK8-9为NH4Cl浓度对钙、镁浸出率的影响(浸出率=×100%).
可知:较适宜的NH4Cl溶液的质量分数为 ;浸取时主要反应的化学方程式为 .
图HK8-9
②流程中虚线框内部分若改用 (填化学式)溶液,可一步得到与原流程完全相同的生成物.
③流程中方框内部若改用Na2CO3溶液,也能得到高纯CaCO3,试从生物的角度分析原流程的优点:
a.NH3可循环利用;
b. .
3.[2018·武汉]实验室现有一瓶含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,某化学兴趣小组利用如图HK8-10所示装置进行实验(该装置气密性良好,装置B、C中所装药品均足量,碱石灰是氧化钙和氢氧化钠的混合物).已知:碳酸氢铵受热易分解,反应的化学方程式为NH4HCO3NH3↑+H2O↑+CO2↑,NH3能被酸溶液吸收.
图HK8-10
部分实验步骤如下:
Ⅰ.打开弹簧夹,通入一段时间的氮气;
Ⅱ.关闭弹簧夹,给碳酸氢铵样品加热;
Ⅲ.当样品反应完全……再停止加热,直到玻璃管冷却;
Ⅳ.实验完毕,测得装置B、C中药品的质量分别增加了m1、m2.
请回答下列问题.
(1)NH4HCO3属于 (填“氮肥”“磷肥”“钾肥”或“复合肥”),装置B中盛放的液体是 .
(2)装置C中发生反应的化学方程式为 .
(3)步骤Ⅲ中,停止加热前应进行的操作是 .
(4)该样品中碳酸氢铵的质量分数的表达式为 (用m1、m2的代数式表示).
【参考答案】
基础过关
1.A 2.B 3.D 4.B 5.C
6.(1)= (2)溶液变为红色 < (3)>
7.(1)S
(2)BaCl2+FeSO4BaSO4↓+FeCl2
(3)产生红色固体,溶液由蓝色变成无色 Mg2+
(4)AC
8.(1)BCD
(2)除去滤液中的碳酸钠和氢氧化钠
9.(1)溶液的颜色
(2)①2HCl+Na2CO32NaCl+H2O+CO2↑
②Ca(OH)2+Na2CO3CaCO3↓+2NaOH
10.(1)过滤 (2)5.3 (3)9
解:(4)由于B样品中Na2CO3的质量与A相等,也为5.3 g,结晶水的质量为9 g,所以碳酸钠与结晶水的质量比为106∶(18×n)=5.3 g∶9 g,解得n=10.
(5)设滴入盐酸的质量为x,生成氯化钠的质量为y,生成二氧化碳的质量为z.
Na2CO3+2HCl2NaCl+H2O+CO2↑
106 73 117 44
5.3 g x×10% y z
= x=36.5 g
= y=5.85 g
= z=2.2 g
氯化钠溶液的质量为
+100 g+36.5 g-2.2 g=149.1 g.
溶质氯化钠的质量为
-5.3 g-9 g+5.85 g=6.35 g.
氯化钠溶液中溶质的质量分数为×100%≈4.26%.
答:(4)化学式Na2CO3·nH2O中n=10;(5)所得NaCl溶液的溶质质量分数为4.26%.
走进重高
1.A
2.(1)CaCO3CaO+CO2↑ 放出 900
煅烧的时间相同
(2)①10%
2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O
②NH4HCO3 ③NH4Cl可以循环使用
3.(1)氮肥 浓硫酸
(2)2NaOH+CO2Na2CO3+H2O
(3)打开弹簧夹,通入一段时间的氮气
(4)×100%








