

【化学】安省省合肥一六八中学2018-2019学年高一上学期期中考试(凌志班)试卷
展开安省省合肥一六八中学2018-2019学年高一上学期期中考试(凌志班)试卷
命题人:高德胜 审题人:朱毓卿
相对原子质量:H∶1 C∶12 O∶16 Na∶23 S∶32 Cl∶35.5 K∶39 Mn∶55 Fe∶56
第I卷
一、选择题(每小题3分,共48分,每小题只有一个选项符合题意)
1.我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3 nm)恢复了磁性“钴酞菁”分子的 结构和性质与人体内的血红素及植物体内的叶绿素非常相似。下列说法中正确的是( )
A.“钴酞菁”分子能透过半透膜
B.“钴酞菁”分子分散在水中所形成的分散系带电
C.此项工作可以用来改变分子的某些物理性质
D.“钴酞菁”分子分散在水中所形成的分散系为溶液
2.逻辑推理是化学学习常用的思维方法,下列推理正确的是( )
A.氧化物都含有氧元素,含有氧元素的化合物一定是氧化物
B.氧化还原反应中有元素化合价的改变,有元素化合价改变的化学反应一定是氧化还原反应
C.电解质是溶于水或熔融状态下能够导电的化合物,溶于水能导电的化合物一定是电解质
D.中和反应有盐和水生成,有盐和水生成的反应一定是中和反应
3.下列叙述中,正确的是( )
A.H2SO4的摩尔质量是98
B.S2和S8的混合物共6.4 g,所含硫原子数为0.2NA
C.等质量的CO与CO2中所含碳原子数之比为7︰11
D.98g H2SO4溶解于500mL水中,所得溶液中硫酸的物质的量浓度为2 mol·L−1
4.下列操作能达到实验目的的是( )
A.除去铝粉中混有的少量铁粉,可加入过量的盐酸溶液,完全反应后过滤
B.将碘的饱和水溶液中的碘提取出来,可用四氯化碳进行萃取
C.制备Fe(OH)3胶体,通常是将FeCl3溶液注入热水中,并搅拌均匀
D.除去Na2CO3溶液中少量的Na2SO4,可加入适量氯化钡,过滤
5.实验室制取氧气的反应为 2 KClO32 KCl+ 3 O2↑ ,反应后从剩余物中回收二氧化锰的操作顺序正确的是(已知MnO2为黑色难溶于水的固体)( )
A、溶解、蒸发、洗涤、过滤 B、溶解、过滤、蒸发、洗涤
C、溶解、过滤、洗涤、干燥 D、溶解、洗涤、过滤、加热
6.等质量的CO和N2,下列叙述不正确的是( )
A.密度一定相同 B.分子数一定相同
C.原子数一定相同 D.物质的量一定相同
7.NA表示阿伏加德罗常数。下列叙述中正确的是( )
A.标准状况下,22.4 L水中含有的水分子数为NA
B.4.0 g NaOH固体溶于100 mL水中,得到1 mol·L−1的NaOH溶液
C.常温、常压下,22 g CO2中含有的氧原子数为NA
D.1 L 0.5 mol·L−1 Na2SO4溶液中,含有的氧原子总数为2NA
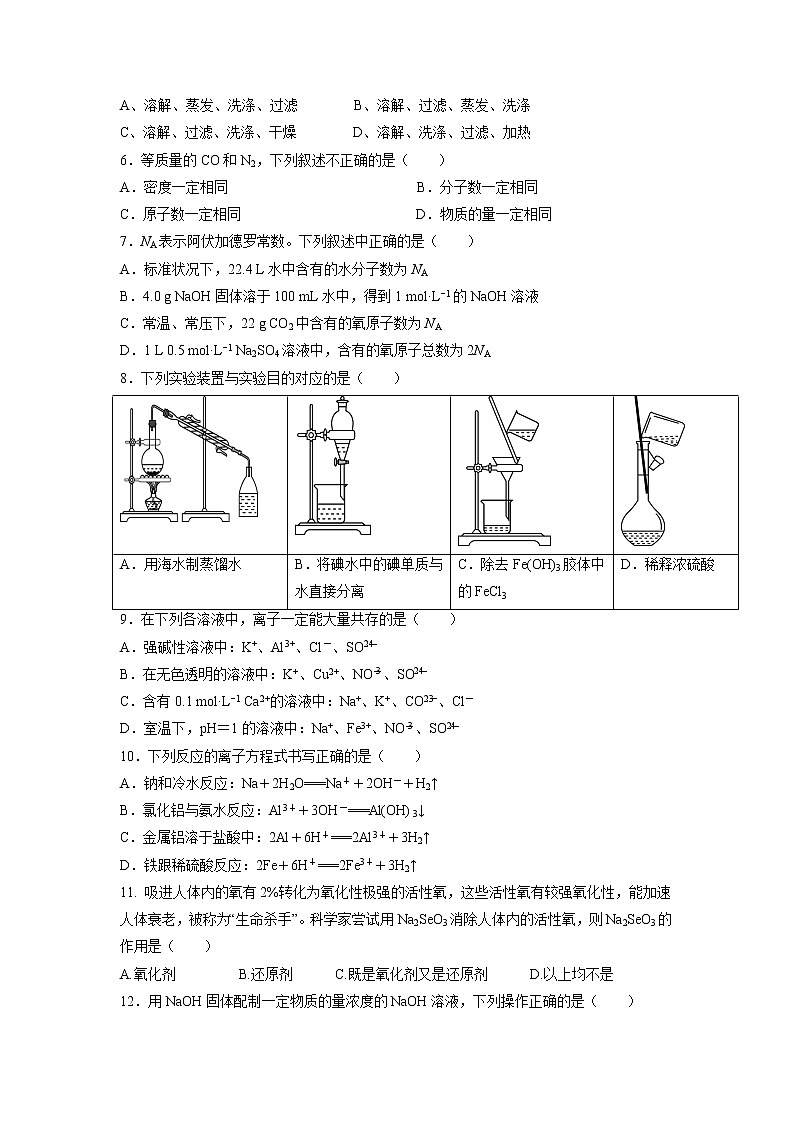
8.下列实验装置与实验目的对应的是( )
A.用海水制蒸馏水 | B.将碘水中的碘单质与水直接分离 | C.除去Fe(OH)3胶体中的FeCl3 | D.稀释浓硫酸 |
9.在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+、Al3+、Cl-、SO
B.在无色透明的溶液中:K+、Cu2+、NO、SO
C.含有0.1 mol·L−1 Ca2+的溶液中:Na+、K+、CO、Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、NO、SO
10.下列反应的离子方程式书写正确的是( )
A.钠和冷水反应:Na+2H2O===Na++2OH-+H2↑
B.氯化铝与氨水反应:Al3++3OH-===Al(OH)3↓
C.金属铝溶于盐酸中:2Al+6H+===2Al3++3H2↑
D.铁跟稀硫酸反应:2Fe+6H+===2Fe3++3H2↑
11. 吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧有较强氧化性,能加速人体衰老,被称为“生命杀手”。科学家尝试用Na2SeO3消除人体内的活性氧,则Na2SeO3的作用是( )
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.以上均不是
12.用NaOH固体配制一定物质的量浓度的NaOH溶液,下列操作正确的是( )
A.称量时,将固体NaOH放在纸片上,放在天平左盘上称量
B.将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解
C.将烧杯中溶解固体NaOH所得溶液,冷却到室温后转移至容量瓶中
D.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
13.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4===2ClO2↑+K2SO4+2CO2↑+2H2 O,下列说法正确的是( )
A.KClO3在反应中失去电子 B.ClO2是氧化产物
C.H2C2O4在反应中被氧化 D.KClO3是还原剂
14.有些离子方程式能表示一类反应,有些离子方程式却只能表示一个反应。下列离子方程式中,只能表示一个化学反应的是( )
A.OH-+HCO===CO+H2O B.Cl2+H2OH++Cl-+HClO
C.CO+2H+===CO2↑+H2O D.Ag+Cl-===AgCl↓
15.某溶液中,若忽略水的电离,只含有下表中所示的四种离子,试推测X离子及其个数b可能为 ( )
离子 | Na+ | Al3+ | Cl- | X |
个数 | 3a | 2a | a | b |
A.SO42—、4 a B.NO3—、4 a C.OH—、8 a D.SO42—、8 a
16.向0.1 mol·L-1 NaOH溶液中加入0.1 mol·L-1的盐酸。若用x代表加入盐酸的体积,y代表溶液中离子的总数,则下列曲线中正确的是( )
A B C D
第Ⅱ卷
二、非选择题(共5小题)
17.(14分)我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。
Ⅰ.(1)上述过程中没有涉及到的四大基本反应类型是______;
a.化合反应 b.分解反应 c.置换反应 d.复分解反应
(2)步骤1中分离操作的名称是___________;
(3)粗盐中含有Ca2+、Mg2+、SO等杂质,精制时所用试剂为:a.盐酸;b.BaCl2溶液;c.NaOH溶液;d.Na2CO3溶液。加入试剂的顺序是_________________________________;
II.实验室利用精盐配制480mL 2.0mol·L-1NaCl溶液。
(4)除容量瓶外,还需要的玻璃仪器有___________________;
(5)用托盘天平称取固体NaCl________g;
(6)配制时,按以下几个步骤进行:①计算 ②称量 ③溶解 ④冷却 ⑤转移 ⑥定容 ⑦摇匀
⑧装瓶。操作中还缺少一个重要步骤是______________________;
(7)下列错误操作可使所配制氯化钠溶液浓度偏低的是_________。
a.容量瓶洗净后残留了部分的水
b.转移时溶液溅到容量瓶外面
c.定容时俯视容量瓶的刻度线
d.摇匀后见液面下降,再加水至刻度线
18.(6分)请回答下列问题:
(1)现有下列状态的物质:①干冰 ②NaHCO3晶体 ③氨水 ④纯醋酸 ⑤FeCl3溶液 ⑥铜 ⑦熔融KOH ⑧盐酸。其中能导电的是__________,(填序号,下同),属于电解质的是___________,属于非电解质的是___________。
(2)下列所给出的几组物质中:含有分子数最少的是___________;含有原子数最多的是________;
标准状况下体积最小的是____________。
①1g H2 ②2.408×1023个CH4分子 ③10.8g H2O ④标准状况下6.72L CO2。
19.(10分)向Ba(OH)2和NaOH的混合溶液中逐渐通入CO2气体至过量,生成沉淀的物质的量(n)和通入CO2气体的(V)的关系如图所示,试回答:
(1)0到a点之间的反应的离子方程式__________
(2)a到b点之间的反应的离子方程式__________
(3)b点之后的反应的离子方程式______________
(4)c点CO2的体积__________mL(同温同压下)。
(5)混合溶液中Ba(OH)2和NaOH 的物质的量之比为__________
20、(10分)一个体重50 kg的健康人含铁元素2 g,这2 g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。
⑴人体中经常进行Fe2+与Fe3+的转化,可表示为Fe2+ Fe3+。在过程A中,Fe2+作 剂,过程B中,Fe3+被 。
⑵“服用维生素C可使食物中的Fe3+转化为Fe2+”这句话指出,维生素C在这个反应中作 剂,具 性。
⑶已知下列反应在一定条件下发生:
在以上的反应中,Fe2+实际上起着 的作用。
21.(12分)将11.2g铁投入200mL某浓度的盐酸中,铁和盐酸恰好完全反应。求:
(1)11.2g铁的物质的量
(2)所用盐酸中HCl的物质的量浓度
(3)反应中生成的H2在标准状况下的体积(要求写出计算过程)
【参考答案】
1—16 CBBBC ACADC BCCBAB
17【答案】Ⅰ.(1)c
(2)过滤
(3)bdca或cbda或bcda
(4)烧杯、玻璃棒、胶头滴管
(5)58.5
(6)洗涤(烧杯和玻璃棒)
(7)bd
18、【答案】(1)③⑤⑥⑦⑧;②④⑦;① (2)④;②;③
19、【答案】(1)Ba2++2OH+CO2===BaCO3↓+H2O
(2)2OH+CO2===CO+H2O、CO+CO2+H2O===2HCO
(3)BaCO3+CO2+H2O===Ba2++2HCO
(4)40
(5)1∶2
20、(1)还原;还原 (2)还原;还原 (3)催化剂(每空2分)
21、【答案】(1)0.2mol
(2)2 mol·L−1
(3)4.48L








