
广东省揭阳市揭西县2020届高三下学期综合测试(四)化学试题
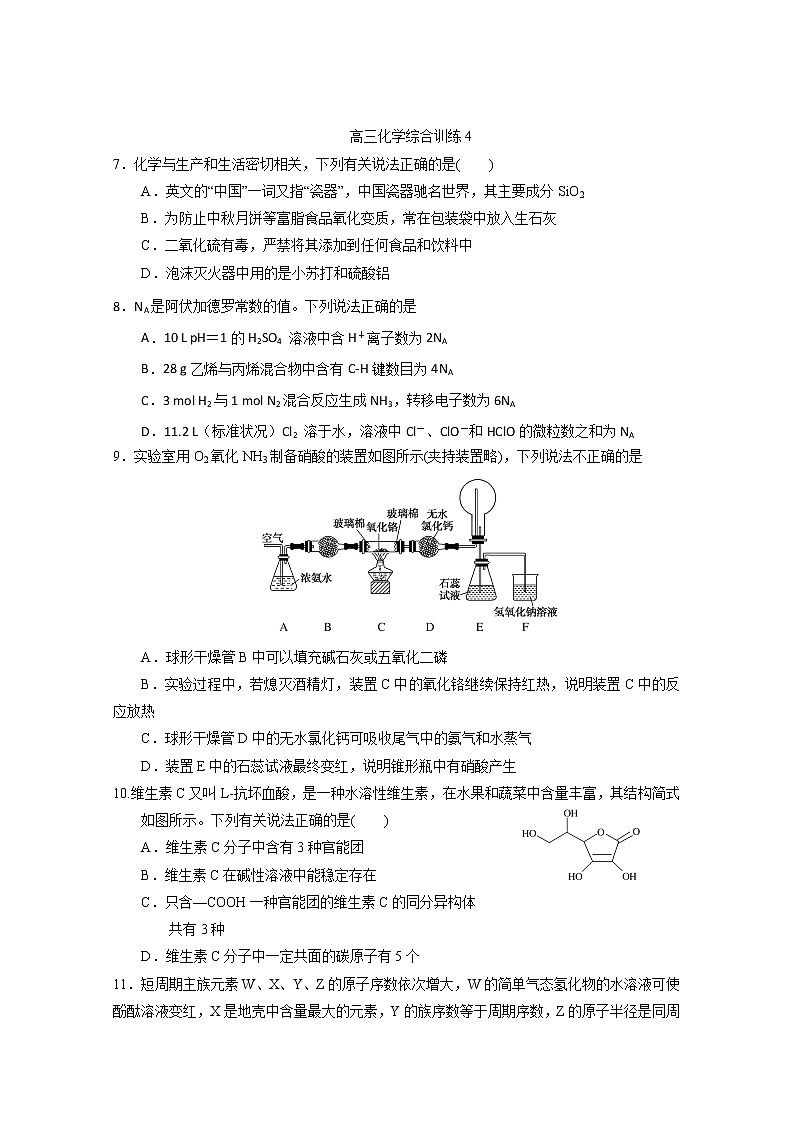
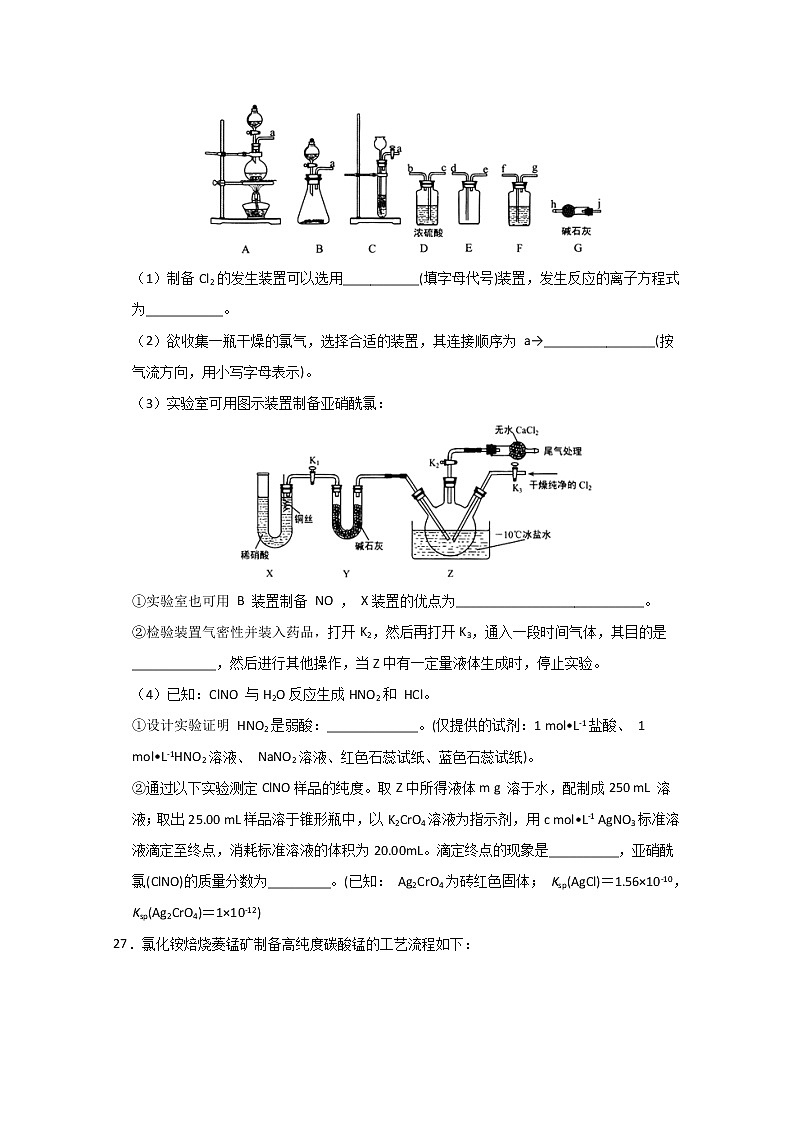
展开高三化学综合训练47.化学与生产和生活密切相关,下列有关说法正确的是( )A.英文的“中国”一词又指“瓷器”,中国瓷器驰名世界,其主要成分SiO2B.为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰C.二氧化硫有毒,严禁将其添加到任何食品和饮料中D.泡沫灭火器中用的是小苏打和硫酸铝8.NA是阿伏加德罗常数的值。下列说法正确的是 A.10 L pH=1的H2SO4 溶液中含H+离子数为2NA B.28 g乙烯与丙烯混合物中含有C-H键数目为4NA C.3 mol H2与1 mol N2混合反应生成NH3,转移电子数为6NA D.11.2 L(标准状况)Cl2 溶于水,溶液中Cl-、ClO-和HClO的微粒数之和为NA9.实验室用O2氧化NH3制备硝酸的装置如图所示(夹持装置略),下列说法不正确的是A.球形干燥管B中可以填充碱石灰或五氧化二磷B.实验过程中,若熄灭酒精灯,装置C中的氧化铬继续保持红热,说明装置C中的反应放热C.球形干燥管D中的无水氯化钙可吸收尾气中的氨气和水蒸气D.装置E中的石蕊试液最终变红,说明锥形瓶中有硝酸产生10.维生素C又叫L抗坏血酸,是一种水溶性维生素,在水果和蔬菜中含量丰富,其结构简式如图所示。下列有关说法正确的是( )A.维生素C分子中含有3种官能团B.维生素C在碱性溶液中能稳定存在C.只含—COOH一种官能团的维生素C的同分异构体共有3种D.维生素C分子中一定共面的碳原子有5个11.短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单气态氢化物的水溶液可使酚酞溶液变红,X是地壳中含量最大的元素,Y的族序数等于周期序数,Z的原子半径是同周期主族元素中最小的。下列说法正确的是( )A.简单离子半径:W<X<ZB.简单气态氢化物的稳定性:W<XC.W、Z的氧化物的水化物均为强酸D.工业上电解Y、Z形成的化合物制备单质Y12.利用CH4燃料电池电解制备Ca(H2PO4)2并得到副产物NaOH、H2、Cl2,装置如图所示。下列说法正确的是( )A.a极反应:CH4+8e-+4O2-===CO2+2H2O B.A膜和C膜均为阴离子交换膜C.可用铁电极替换阴极的石墨电极D.a极上通入2.24 L甲烷,阳极室Ca2+减少0.4 mol13、常温下,向10mL0.10 mol/L CuCl2溶液中滴加0.10mol/L Na2S溶液,滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。下列说法正确的是A.Ksp(CuS)的数量级为10-21B.曲线上a点溶液中,c(S2-)•c(Cu2+) > Ksp(CuS)C.a、b、c三点溶液中,C(H+)和C(OH-)的积最小的为b点D.c点溶液中:c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)26.亚硝酰氯(ClNO)是有机物合成中的重要试剂,其沸点为-5.5℃,易水解。已知:AgNO2微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某学习小组在实验室用Cl2和NO制备ClNO并测定其纯度,相关实验装置如图所示。(1)制备Cl2的发生装置可以选用___________(填字母代号)装置,发生反应的离子方程式为___________。 (2)欲收集一瓶干燥的氯气,选择合适的装置,其连接顺序为 a→________________(按气流方向,用小写字母表示)。(3)实验室可用图示装置制备亚硝酰氯:①实验室也可用 B 装置制备 NO , X装置的优点为___________________________。②检验装置气密性并装入药品,打开K2,然后再打开K3,通入一段时间气体,其目的是____________,然后进行其他操作,当Z中有一定量液体生成时,停止实验。 (4)已知:ClNO 与H2O反应生成HNO2和 HCl。①设计实验证明 HNO2是弱酸:_____________。(仅提供的试剂:1 mol•L-1盐酸、 1 mol•L-1HNO2溶液、 NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)。②通过以下实验测定ClNO样品的纯度。取Z中所得液体m g 溶于水,配制成250 mL 溶液;取出25.00 mL样品溶于锥形瓶中,以K2CrO4溶液为指示剂,用c mol•L-1 AgNO3标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。滴定终点的现象是__________,亚硝酰氯(ClNO)的质量分数为_________。(已知: Ag2CrO4为砖红色固体; Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)27.氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下: 已知:①菱锰矿石主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素; ②相关金属离子[c(Mn+)=0.1 mol·L−1]形成氯氧化物沉淀时的pH如下: 金属离子Al3+Fe3+Fe2+Ca2+Mn2+Mg2+开始沉淀的pH3.81.56.310.68.89.6沉淀完全的pH5.22.88.312.610.811.6③常温下,CaCl2、MnCl2的溶度积分别为回答下列问题: (1)“焙烧”时发生的主要化学反应方程式为_____________________。 (2)分析下列图1、图2、图3,氯化铵焙烧菱镁矿的最佳条件是: 焙烧温度_________,氯化铵与菱镁矿粉的质量之比为__________,焙烧时间为________。(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式为________________________________________;然后调节溶液pH使Fe3+、Al3+沉淀完全,此时溶液的pH范围为___________________________。再加入NH4F沉淀Ca2+、Mg2+,当c(Ca2+)=1.0×10−5 mol·L−1时,c(Mg2+)=__________________mol·L−1。(4)碳化结晶时,发生反应的离子方程式为___________。 (5)流程中能循环利用的固态物质是____________。28.(15分)磷酸是重要的化学试剂和工业原料。请回答下列问题:(1)已知:25 ℃时,磷酸和氢氟酸的电离常数如下表所示。物质H3PO4HF电离常数Ka1=7.1×10-3;Ka2=6.3×10-8;Ka3=4.2×10-13Ka=6.6×10-4向NaF溶液中滴加少量H3PO4溶液,反应的离子方程式为_____________________。 (2)已知:Ⅰ.CaO(s)+H2SO4(l)⇌CaSO4(s)+H2O(l) ΔH=-271 kJ·mol-1Ⅱ.5CaO(s)+3H3PO4(l)+HF(g)⇌Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1则:①工业上用Ca5(PO4)3F和硫酸反应制备磷酸的热化学方程式为____________。②一定条件下,在密闭容器中只发生反应Ⅱ,达到平衡后缩小容器容积,HF的平衡转化率________(填“增大”“减小”或“不变”,下同);HF的平衡浓度________。(3)工业上用磷尾矿制备Ca5(PO4)3F时生成的副产物CO可用于制备H2,原理为CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH。①一定温度下,向10 L密闭容器中充入0.5 mol CO和1 mol H2O(g),2 min达到平衡时,测得0~2 min内用CO2表示的反应速率v(CO2)=0.02 mol·L-1·min-1。则CO的平衡转化率α=________;该反应的平衡常数K=________。②在压强不变的密闭容器中发生上述反应,设起始的=y,CO的平衡体积分数(φ)与温度(T)的关系如图所示。则:该反应的ΔH________0(填“>”“<”或“=”,下同)。a________1,理由为_____________________________。36.[化学——选修5:有机化学基础](15分)顺丁烯二酸也称马来酸,是食品饮料工业中的新型酸味剂。马来酸酐()是一种重要的化工原料,可用于合成可降解的高聚物树脂H。流程中E的产量常作为衡量一个国家石油化工发展水平的重要标志。回答下列问题:(1)E的名称为____________;I中含有官能团的名称是____________。(2)F为环状结构,核磁共振氢谱只有一组峰,其结构简式为________。(3)顺丁烯二酸的结构简式为________。(4)I生成J的反应类型为________反应。(5)写出D与G反应生成H的化学方程式________。(6)同时符合下列条件的有机物共有________种,写出核磁共振氢谱峰面积比为3:3:1:1的一种同分异构体的结构简式________(不考虑立体异构)。①相对分子质量比J大14②与J具有相同官能团③可发生银镜反应 高三化学综合训练4参考答案题号78910111213答案DBAABCD26、【答案】(1)A(或B) MnO2+4H++2Cl-Mn2++ Cl2↑+2H2O(或2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O)(2)f→g→c→b→d→e→j→h(3)①随开随用,随关随停 ②排干净三颈烧瓶中的空气(4)①用玻璃棒蘸取NaNO2溶液,点在红色石蕊试纸中央,若试纸变蓝,说明HNO2是弱酸 ②滴入最后一滴标准液,生成砖红色沉淀,且半分钟内无变化 % 27、【答案】(1)MnCO3+2NH4ClMnCl2+2NH3↑+CO2↑+H2O (2)500℃ 1.10 60min (3)MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O 5.2≤pH<8.8 5×10-6 (4)Mn2++2HCO3-MnCO3↓+CO2↑+H2O (5)NH4Cl 28、答案:(1)H3PO4+F-===H2PO+HF(2分)(2)①Ca5(PO4)3F(s)+5H2SO4(l)3H3PO4(l)+HF(g)+5CaSO4(s) ΔH=-418 kJ/mol(2分) ②增大(1分) 不变(1分)(3)①80%(2分) 8/3(2分) ②<(1分) <(2分) 相同温度下,n(CO)/n(H2O)越小,CO的转化率越大,其平衡体积分数越小(2分)36、答案:(除标明外,每空1分)(1)乙烯 碳碳双键、羧基(2分)(2) (3) (2分) (4)酯化(取代)(5)HOHOO+(2n-1)H2O (2分)(6)8(2分)





