

福建省师范大学附属中学2019-2020学年高一上学期期中考试化学试题
展开www.ks5u.com福建师大附中2019-2020学年上学期期中考试
高一化学试卷
试卷说明:
(1)本卷共两大题,24小题,解答写在答卷的指定位置上,考试结束后,只交答卷。
(2)考试过程中不得使用计算器或具有计算功能的电子设备。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5
K-39 Ba-137
第Ⅰ卷(选择题,共45分)
一、选择题:共20小题,其中1-15题,每题2分,16-20题,每题3分,共45分。
1. 对下列物质进行的分类正确的是( )
A. 纯碱、烧碱均属于碱
B. CuSO4·5H2O属于纯净物
C. 凡能电离出H+的化合物均属于酸
D. 盐类物质一定含有金属阳离子
2. 下列关于胶体的有关说法中,不正确的是( )
A. 用丁达尔效应可以鉴别氯化铁溶液和氢氧化铁胶体
B. 明矾能净水,是因为溶于水能形成胶体,吸附性强
C. 胶体静置片刻后会出现分层现象
D. 胶体、溶液和浊液的本质区别是分散质粒子的大小不同
3. 简单原子的原子结构可用如图表示方法形象表示:
●表示质子或电子,◯表示中子,则下列有关①②③的叙述正确的是( )
A. ①②③互为同位素
B. ①②③为同素异形体
C. ①②③是三种化学性质不同的粒子
D. ①②③具有相同的质量数
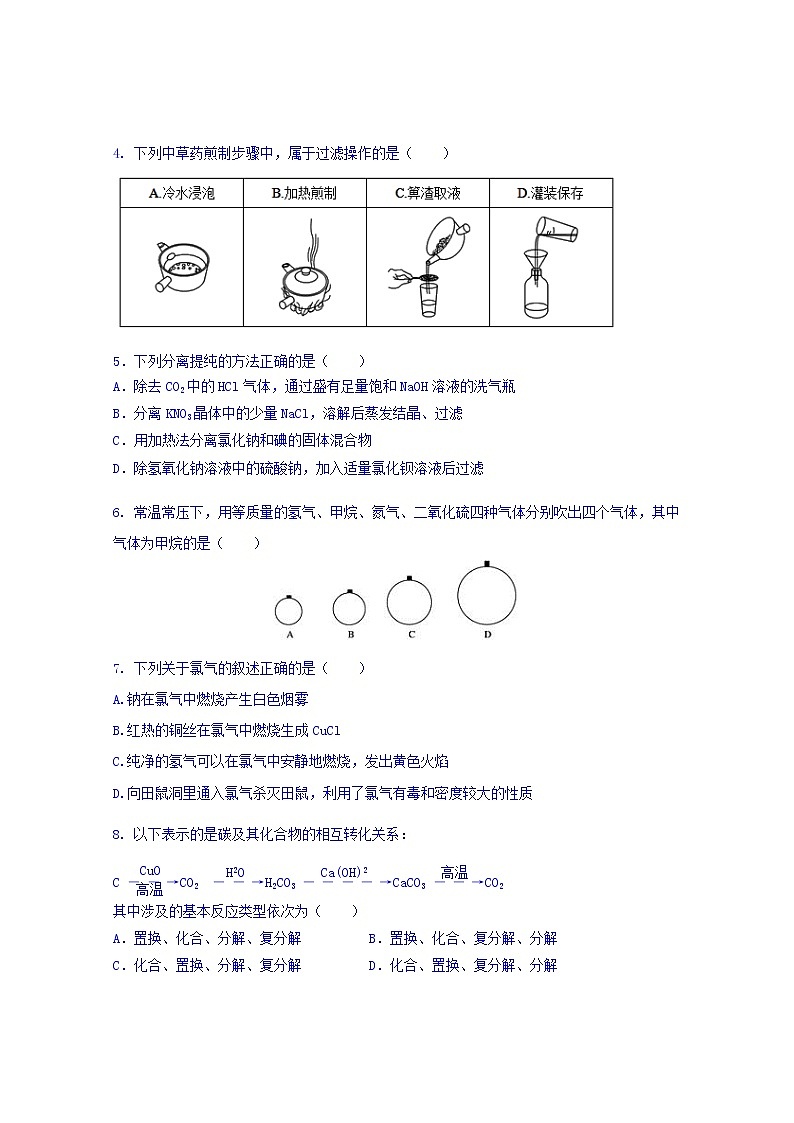
- 下列中草药煎制步骤中,属于过滤操作的是( )
5.下列分离提纯的方法正确的是( )
A.除去CO2中的HCl气体,通过盛有足量饱和NaOH溶液的洗气瓶
B.分离KNO3晶体中的少量NaCl,溶解后蒸发结晶、过滤
C.用加热法分离氯化钠和碘的固体混合物
D.除氢氧化钠溶液中的硫酸钠,加入适量氯化钡溶液后过滤
6. 常温常压下,用等质量的氢气、甲烷、氮气、二氧化硫四种气体分别吹出四个气体,其中气体为甲烷的是( )
- 下列关于氯气的叙述正确的是( )
A.钠在氯气中燃烧产生白色烟雾
B.红热的铜丝在氯气中燃烧生成CuCl
C.纯净的氢气可以在氯气中安静地燃烧,发出黄色火焰
D.向田鼠洞里通入氯气杀灭田鼠,利用了氯气有毒和密度较大的性质
8. 以下表示的是碳及其化合物的相互转化关系:
CCO2 H2CO3CaCO3CO2
其中涉及的基本反应类型依次为( )
A.置换、化合、分解、复分解 B.置换、化合、复分解、分解
C.化合、置换、分解、复分解 D.化合、置换、复分解、分解
9.下列对进行焰色反应实验操作注意事项的说明正确的是( )
①要透过蓝色钴玻璃观察钾的火焰颜色 ②先把铂丝烧到与原来火焰颜色相同,再蘸取被检测的物质 ③每次实验后,要用盐酸把铂丝洗净 ④实验时最好选择本身颜色较微弱的火焰 ⑤没有铂丝,也可以用光洁无锈的铁丝代替
A.仅有③不正确 B.仅有④不正确
C.仅有⑤不正确 D.全部正确
10.下列关于摩尔质量的描述或应用中正确的是( )
A.1 mol OH-的质量是17
B.二氧化碳的摩尔质量是44 g
C.铁原子的摩尔质量等于它的相对原子质量
D.一个钠原子的质量约为 g
11.下列说法正确的是( )
A.标准状况下,22.4 L任何气体都约含有6.02×1023个分子
B.含1 mol氦原子的氦气在标准状况下的体积约为11.2 L
C.常温常压下,11.2 L Cl2含有的分子数为0.5NA
D.标准状况下,11.2 L蔗糖含有的分子数为0.5NA
12.mg某金属M与足量盐酸完全反应,生成MCl2和nmol 氢气,则该金属的相对原子质量为( )
A. B. C. D.
13.用10 mL 0.1 mol·L-1 BaCl2溶液恰好可使相同体积的Fe2(SO4)3、K2SO4和ZnSO4三种溶液中的SO42-完全转化为BaSO4沉淀,则三种硫酸盐溶液物质的量浓度之比是( )
A.3∶2∶2 B.1∶2∶3
C.1∶3∶3 D.3∶1∶1
14.某溶液中含有较大量的Cl-、CO、OH-等三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次检验出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③
C.①②③②④ D.④②③②①
15.下列实验过程中出现的异常情况,其可能原因分析错误的是( )
选项 | 异常情况 | 可能原因分析 |
A | 蒸发结晶:蒸发皿破裂 | 将溶液蒸干或酒精灯灯芯碰到热的蒸发皿底部 |
B | 分液:分液漏斗中的液体难以滴下 | 没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
C | 萃取:液体静置不分层 | 加入萃取剂的量较多 |
D | 蒸馏:冷凝管破裂 | 冷凝管没有通水或先加热后通水 |
16.从2 mol·L-1的氯化铜溶液中取出含Cl-为3.55 g的溶液,所取溶液的体积是( )
A.25 mL B.50 mL C.12.5 mL D.0.025 mL
17.下列有关阿伏加德罗常数( NA)的说法错误的是( )
A. 25℃、101kPa条件下22克CO2所含的原子数目为1.5 NA
B. 标准状况下0.1mol H2O含有的分子数目为0.1 NA
C. 0℃、101kPa条件下,0.3 NA氧气的体积时6.72升
D. 58.5克NaCl固体中含有的离子数目为NA
18.在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A. 甲的分子数比乙的分子数多
B. 甲的摩尔体积比乙的摩尔体积小
C. 甲的相对分子质量比乙的相对分子质量小
D. 甲的物质的量比乙的物质的量少
19.300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1 Ba(OH)2溶液300 mL,反应后溶液中SO的物质的量浓度为( )
A.0.1 mol·L-1 B.0.2 mol·L-1
C.0.3 mol·L-1 D.0.4 mol·L-1
20.已知阴离子R2−的原子核内有n个中子,R原子的质量数为m,则w g R2−所含有电子的物质的量是( )
A. B.
C. D.
第II卷(非选择题,共55分)
二、非选择题:共4小题,共55分。
21.(6分)下列物质中:A.NaCl晶体;B.CH3CH2OH(酒精);C.H2SO4溶液;D.单质铜;E.HNO3溶液;F.熔融氯化钾;G.SO2气体;H.液态氯化氢
(1)能导电的是_____________________________________________________。
(2)属于电解质的是_________________________________________________。
(3)属于非电解质的是_______________________________________________。
22.(11分)氯水中含有多种成分,因而具有多种性质,根据新制氯水分别与如图四种物质发生的反应填空(a、b、c、d、e中重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是 (填“a”“b”“c”或“d”);
(2)c过程中的现象是 ;
(3)e过程中的化学方程式为 ;
(4)实验室保存饱和氯水的方法是 。
23.(18分))欲提纯混有硫酸钠、碳酸氢铵的氯化钠固体,某学生设计了如下方案:
请根据操作流程回答下列问题:
(1)操作①在加热时应选择 盛装混合物(填仪器名称)。
(2)进行操作②后,判断SO42−已沉淀完全的方法是 。
(3)操作③的化学方程式为 。
(4)操作④的目的是 。
(5)实验室进行操作⑤的具体步骤是 。
(6)某同学欲用制得的氯化钠固体配制100mL0.2mol⋅L−1的氯化钠溶液。
①配制NaCl溶液时需用到的主要仪器有托盘天平、药匙、烧杯、玻璃棒、量筒、__、__。
②下列操作会使所配氯化钠溶液浓度偏小的是 (请填序号)。
A. 加水定容时俯视刻度线
B. 容量瓶内壁附有水珠而未干燥处理
C. 在溶解过程中有少量液体溅出烧杯外
D. 颠倒摇匀后发现凹液面低于刻度线又加水补上
24.(20分)Ⅰ.根据下列各题中所给出的数据,可分别求出其溶液中溶质的质量分数或溶液中溶质的物质的量浓度,试判断并求解。
(1)已知某氢氧化钠溶液V L中含有n个氢氧根离子,可求出此溶液的 是 。
(2)已知某氢氧化钠溶液中Na+与H2O的个数之比为1:a,则可求出此溶液的 为 。
Ⅱ.常温下,10.0mL 1.0mol•L-1的H2SO4(aq),加水稀释到500mL,所得H2SO4溶液的浓度为 mol•L-1;蒸发浓缩使溶液的体积为2.40mL,所得H2SO4溶液的浓度为 mol•L-1。(结果保留小数点后一位)
Ⅲ.已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中溶质的质量分数为 。(结果保留小数点后一位)
Ⅳ.现有一混合物的水溶液,可能含有以下离子中的几种:、、、、、、现取三份各100mL溶液进行如下实验: 第一份加入AgNO3溶液有沉淀产生;第二份加足量NaOH溶液加热后,收集到气体;第三份加足量溶液后,得到干燥沉淀,经足量盐酸洗涤、干燥后,沉淀质量为。
该混合液中一定含有 ,可能含 ,且n(K+) (填取值范围)
福建师大附中2019-2020学年上学期期中考试
高一化学答案
一、选择题(共20小题,其中1-15题,每题2分,16-20题,每题3分,共45分)
1.B 2.C 3.A 4.C 5.C 6.C 7.D 8. B 9.D 10.D 11.A 12.D
13.C 14.B 15.C 16.A 17.D 18.D 19.A 20.D
二、非选择题(共4小题,共55分)
21.(6分)
(1)CDEF (2分)
(2)AFH(2分)
(3)BG(2分)
- (11分)
(1)d;(2分)
(2)有白色沉淀生成;(3分)
(3)Cl2+2NaOH═NaCl+NaClO(3分)
(4)在阴凉处置于棕色试剂瓶中密封保存。(3分)
23.(18分)
(1)坩埚;(2分)
(2)静置,往上层清液中维续滴加BaCl2溶液,若不出现浑浊,则SO42-已沉淀完全(3分)
(3)BaCl2+Na2CO3=BaCO3↓+2NaCl(3分)
(4)除去溶解在溶液中过量的HCl和CO2;(3分)
(5)将溶液置于蒸发皿中,加热蒸发,并用玻璃棒不断搅拌,加热蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干;(3分)
(6)①胶头滴管、100mL容量瓶;(2分)②CD(2分)
24.(20分)
Ⅰ.(1)溶质的物质的量浓度 (2分) n/VNA mol/L;(2分)
(2)溶质的质量分数(2分);40/(40+18a)×100%;(2分)
Ⅱ.0.02;(2分)4.2;(2分)Ⅲ 44.9%。(2分)
Ⅳ.该混合液中一定含有:、、、(2分),可能含(2分),且(2分)








