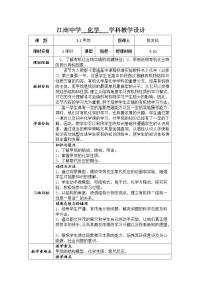
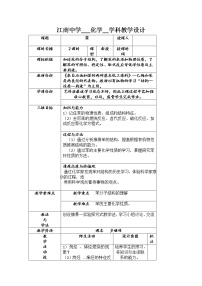
高中化学人教版 (新课标)必修2第三节 化学键教学设计及反思
展开
|
|
|
| 编号 | 07 | |||||||||||||||||||||||||||||||||||||||||
课题 | 离子键 | |||||||||||||||||||||||||||||||||||||||||||||
三 维 目 标 | 知识与 技能 | 1.使学生理解离子键的概念,能用电子式表示离子化合物的形成。 2.使学生了解化学键的概念和化学反应的本质 | ||||||||||||||||||||||||||||||||||||||||||||
过程与 方法 | 通过离子键教学,培养对微观粒子运动的想像力。
| |||||||||||||||||||||||||||||||||||||||||||||
情感态度与价值观 | 通过离子键的教学,培养对微观粒子运动的想像力。
| |||||||||||||||||||||||||||||||||||||||||||||
教学重点 | 离子键 | |||||||||||||||||||||||||||||||||||||||||||||
教学难点 | 化学键的概念,化学反应的本质 | |||||||||||||||||||||||||||||||||||||||||||||
教学方法 |
| |||||||||||||||||||||||||||||||||||||||||||||
教学媒体 |
| |||||||||||||||||||||||||||||||||||||||||||||
教学内容 | 师生活动 | 修改建议 | ||||||||||||||||||||||||||||||||||||||||||||
| 同学们,我们的生活中离不开食盐,食盐对维持人体的生命活动有着重要的意义,我们知道食盐就是氯化钠,它是由钠和氯两种元素组成的,那么,钠和氯是如何形成氯化钠的?是什么作用使得Na+和Cl-紧密的结合在一起的?这节课我们就研究这个问题。 第三节 化学键 钠在氯气中的燃烧实验 钠在氯气中剧烈燃烧有大量的白烟生成,白烟就是氯化钠的固体小颗粒,叫做氯化钠晶体。氯化钠晶体呈什么形状?它的空间结构又是怎样的? 展示NaCl的晶体样品、晶体空间结构模型。 与Na+较近是Cl-,与Cl-较近是Na+,Na+ 与Na+、 Cl-与 Cl-未能直接相连;无数个Na+与 Cl-相互连接向空间无限延伸排列就形成了NaCl的晶体。 Na+ 与Cl-通过什么方式形成 NaCl的呢? 1、请同学们写出Na和Cl的原子结构示意图?Na和Cl的原子结构是否稳定?通过什么途径才能达到稳定结构? 2、请写出Na+ 和Cl-结构示意图,并用原子结构示意图表示NaCl的形成过程。 用原子结构示意图表示NaCl的形成过程。 原子结构示意图必须把原子核所带电荷和核外不同层上的电子数全部表示出来,钠原子失去最外层的一个电子变成Na+达到8电子稳定结构,氯原子得一个电子变成Cl-也达到8电子稳定结构,Na+ 与Cl-相互结合就形成了NaCl。 Na+ 与Cl-之间是一种什么作用使它们不能相互远离?为什么? Na+带正电荷、Cl-带负电荷,它们所带电荷电性相反相互吸引而靠近。 Na+ 与Cl-能否无限制的靠近呢? (把原子结构示意图表示NaCl的形成过程投影出来,对照分析。)Na+ 与Cl-它们的原子核都带正电荷而排斥,同时原子核外的电子与电子之间都带负电荷也相互排斥,所以 Na+ 与Cl-两者要相互远离;又因静电吸引作用而靠近,当Na+ 与Cl-接近到一定的距离时静电吸引作用和静电排斥作用达到平衡,于是就形成了稳定的离子键,形成了离子化合物NaCl。任何事物都存在着矛盾的两方面,是既对立又统一,任何事物都是对立统一体。离子键就是阴阳离子的静电吸引作用和静电排斥作用的对立统一体。 带有正电荷的Na+ 与带有负电荷的Cl-相互靠近,到了一定的距离时不在移动。多次重复上述操作让学生看个明白。 一、离子键 1、使阴、阳离子形成化合物的静电作用叫离子键 通过离子键的概念我们可以了解形成离子键的粒子是什么,粒子之间形成化合物的作用方式是什么,可以看到新的物质的生成必须有新的化学键的生成,这就是化学反应的本质。 1、形成离子键的粒子是什么?这些粒子又是怎样形成的?它们的活泼性怎样? 2、离子键的本质是什么?您是怎样理解的? 3、NH4+与Cl-、CO32-能形成离子键吗?为什么?Na+与CO32-、SO42-呢?你还能举出哪些粒子可以形成离子键? (在学生讨论的基础上)形成离子键的粒子是阴阳离子,阴阳离子是由活泼的金属原子和活泼的非金属原子得失电子而形成的。离子键的本质是静电作用,既有静电吸引作用又有静电排斥作用,大多数的情况下只要有阴阳离子就可以形成离子键,大多数的盐和强碱都是离子化合物,因此也存在离子键。阴阳离子之间有静电排斥作用,所以不会出现阴阳离子所带电荷的中和。 2、离子键的本质与形成条件和形成原因 1、成键本质:静电作用 2、成键条件: (1)活泼金属元素与活泼非金属元素之间易形成离子键。即元素周表中ⅠA、ⅡA主族元素和ⅥA、ⅦA之间易形成离子键。 (2)有些带电荷的原子团之间或与活泼的非金属、金属的离子之间也能行成离子键。 (3)强碱与大多数盐都存在离子键。 练习 1、下列说法正确的是:( ) A.离子键就是阴阳离子间的静电引力 B.所有金属元素与所有非金属元素间都能形成离子键 C.钠原子与氯原子结合成氯化钠后体系能量降低 D.在离子化合物CaCl2中,两个氯离子间也存在离子键 2、下列各数值表示有关元素的原子序数,能以离子键相互结合成稳定化合物的是:( ) A.10与19 B.6与16 C. 11与17 D.14与8 答案 1、主要考查离子键的概念 (C ) 2、主要考查离子键的形成条件。方法一:可以先根据原子序数判断元素的名称,然后判断金属性和非金属性的强弱,再判断能否形成离子键。方法二:可以根据原子的最外层上的电子数判断元素所在的主族,在判断金属性和非金属性的强弱,从而判断能否形成离子键。(C) 用原子结构示意图表示NaCl的形成过程。 同学们,NaCl的形成可以用化学方程式表达,但是这只是表达了钠和氯气可以生成了NaCl,而钠和氯气通过什么方式生成NaCl的没有表达出来;用原子结构示意图表示NaCl的形成过程很麻烦、难书写。能否用一种简单的形式表示NaCl的形成过程呢? 我们知道在化学反应中一般是原子的最外层电子发生变化,原子的最外层电子决定元素的化学性质,也体现了原子结构的特点,我们只需要在元素符号周围把原子的最外层的电子表达出来就可以把原子的结构特点表达出来,这就是电子式。 3、用电子式表示离子化合物的形成过程 (1)电子式:在元素符号的周围用小黑点(·或 )来表示原子的最外层电子,这种式子叫做电子式。 H、Na、 Mg、Cl、O等原子的电子式。
1、电子式中的电子一般要成对书写。但Mg、O等原子的电子式常按上述方式书写. 2、同主族原子的电子式基本相同 你是否能写Na+ 、 Cl- 、 Mg2+ 、 O2-等离子的电子式? (略)
金属原子失去了最外层上的电子变成阳离子达到稳定结构,书写电子式时阳离子最外层上的电子通常不表达出来,所以阳离子的离子符号就是它的电子式;非金属原子得到电子最外层达到8电子的稳定结构,所以阴离子的电子式要在元素符号的周围用小黑点表示最外层的8个电子并且加上n-来表示,n表示阴离子带的电荷数 。 讨论如何表示NaCl 、Na2O、CaCl2等化合物的电子式?
NaCl的电子式的书写是把Cl-的电子式表达出来放Na+之后,Na2O的电子式是在O2-的电子式的两边分别写上两个Na+的电子式,CaCl2的电子式是在Ca2+的电子式的两边分别写上两个Cl- 的电子式。 练习 下列电子式的书写是否正确,为什么? 1、错误,表达不明确。如果是氧原子的电子式,就多了两个电子;如果是氧离子的电子式,则漏掉了括号和电荷。2、错误,Na原子失去了最外层上的电子,次外层变成了最外层,一般不把次外层上的电子表达出来,阳离子的离子符号就是它的电子式。 3、错误,-2表示硫的化合价而不是硫离子带的电荷。4、错误,硫离子的电子式应该加上括号。5、错误,应该把Cl-的电子式写在Ca2+的电子式的两侧。6、错误,应该把Na+的电子式写在O2-的电子式的两侧。
为什么氯化钙的化学式写成CaCl2 的形式,而它的电子式必须写成 这样的形式? CaCl2只表示氯化钙的化学组成和Ca2+与Cl-个数比例关系,电子式不仅表示组成和比例特点,还表示了离子键的特点,它表示的是Ca2+与Cl-以离子键的方式相结合,而不是Cl-与Cl-以离子键结合,如果把两个Cl-的电子式写在一起就容易引起混淆,所以应该把Cl-的电子式写在Ca2+的电子式的两侧。
怎样用电子式表示离子化合物NaCl、MgCl2的行成过程?
箭号左方相同的微粒可以和并,箭号右方相同的微粒不可以和并。用电子式可以直观的简洁的表示出原子之间是怎样形成离子的,又是怎样形成离子键的,这也反映了化学反映的本质,即发生化学反应就有新键的生成。 1、用电子式表示氯化钠的形成过程和用化学方程式表示氯化钠的生成的区别和联系
请回顾本节课学习的内容并作小结。 同学们通过讨论学习,了解了离子键的概念,明确了离子键的形成条件、原因和性质,要求我们在深入理解概念的基础上,掌握用电子式表示离子化合物的形成过程。
|
多媒体展示氯化钠 的形状及空间结构
投影形成过程
离子键成键的本质:静电作用。
多媒体投影
重点讲解电子式的书写及形成过程
多媒体投影练习
| ||||||||||||||||||||||||||||||||||||||||||||
布置作业 | 用电子式表示下列离子化合物的形成过程: BaCI2 NaF MgS K2O | |||||||||||||||||||||||||||||||||||||||||||||
板书设计 |
第三节 化学键 一、离子键 1、使阴、阳离子形成化合物的静电作用叫离子键 2、离子键的本质与形成条件和形成原因 1、成键本质:静电作用 2、成键条件 3.形成过程 | |||||||||||||||||||||||||||||||||||||||||||||
课后反思 | 本节课的重点是一些化学符号的电子式的书写 学生对于掌握电子式以及形成过程感觉较吃力,需多花时间加大练习进行巩固。
| |||||||||||||||||||||||||||||||||||||||||||||
苏教版必修二专题1 微观结构与物质的多样性第二单元 微粒之间的相互作用力教学设计及反思: 这是一份苏教版必修二专题1 微观结构与物质的多样性第二单元 微粒之间的相互作用力教学设计及反思,共4页。
高中化学人教版 (新课标)必修2第一节 化学能与热能教案及反思: 这是一份高中化学人教版 (新课标)必修2第一节 化学能与热能教案及反思,共12页。
高中化学人教版 (新课标)必修2第三节 生活中两种常见的有机物教学设计及反思: 这是一份高中化学人教版 (新课标)必修2第三节 生活中两种常见的有机物教学设计及反思,共8页。