化学人教版 (新课标)第一节 化学能与热能第2课时教案设计
展开第一节 化学能与热能
第2课时
【教学目标】
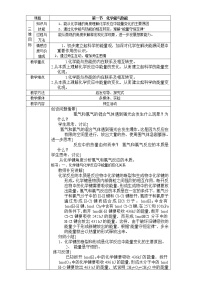
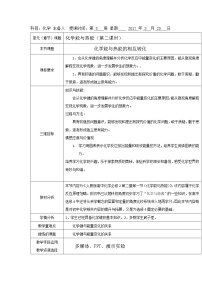
1、通过实验知道化学反应中能量变化的主要表现形式,能根据事实判断吸热反应、放热反应,能说出中和热的涵义。
2、通过实验探究体验科学研究的一般过程,了解科学研究基本方法。
3、通过实验发展学习化学的兴趣,进一步形成交流、合作、反思、评价的学习习惯。
【重点难点】吸热反应、放热反应、中和热等基本概念。
【教学方法】讨论、实验、比较
【教学过程】
[创设问题情景]
在我们接触的化学反应中,物质在发生化学反应的同时还伴随着能量的变化
[实验2-1]
[思考]:
1、 实验的目的是?
2、铝条为什么要打磨?
3、在感知盐酸和铝反应是否有热量的变化时,用的是温度计,还可以用什么来感知?各有什么优缺点?
[实验2-2]
[思考]
1、 实验的目的是?
2、猜测反应放出的气体是什么?
3、氯化铵晶体和Ba(OH)2•8H2O晶体要研细?
[实验2-3]
[思考和交流]
1、实验的目的是?
2、酸和碱发生中和反应生成1 mol H2O时所释放的热量称为中和热。如果要你来测量,在反应的装置上,你认为要注意什么?试画出测量的装置图。
3、为了保证20ml 2mol/L NaOH完全反应,通常加适当过量的盐酸,如25ml 2mol/L HCl ,问若加15ml 2mol/L HCl,所测得的中和热是 (填偏大、偏小、不变)。
4、用HNO3和KOH来做这个实验,所测得的中和热结果和盐酸、氢氧化钠这组比较数值 (填偏大、偏小、不变)。
[归纳小结]
物质在发生化学反应的同时还伴随着能量的变化,这些能量变化通常又表现为热量的变化(也有其他形式,如发光)。对于化学反应我们有时是利用它的产物,有时我们利用的却是它的能量!如化石燃料的燃烧等。
[思考]
1、结合物质的燃烧,吸热反应一定要加热吗?放热反应就一定不用加热吗?
[小结]常见的放热反应有:
常见的吸热反应有:
2、氢气和氧气反应是放热反应,2 mol氢气和1 mol氧气反应时,若一种是生成2 mol水蒸气,一种是生成2 mol液态水,两种情况下放出的热量同吗?若不同,谁的大?
[思考与交流]
反应放出或吸收的热量和反应物、生成物的状态有关吗?
人教版 (新课标)必修2第二章 化学反应与能量第一节 化学能与热能教学设计: 这是一份人教版 (新课标)必修2第二章 化学反应与能量第一节 化学能与热能教学设计,共2页。教案主要包含了学习目标,学习重难点,学习过程等内容,欢迎下载使用。
人教版 (新课标)必修2第一节 化学能与热能第2课时教案设计: 这是一份人教版 (新课标)必修2第一节 化学能与热能第2课时教案设计,共3页。教案主要包含了化学能与热能的相互转化等内容,欢迎下载使用。
人教版 (新课标)必修2第一节 化学能与热能第1课时教案及反思: 这是一份人教版 (新课标)必修2第一节 化学能与热能第1课时教案及反思,共5页。教案主要包含了化学能与热能的相互转化,常见的吸热反应和放热反应,化学能的利用等内容,欢迎下载使用。