





化学必修 第一册第一节 铁及其化合物示范课课件ppt
展开今天你都看到了什么金属材料?
合金是由两种或两种以上的金属或金属与非金属熔合而成的具有金属特性的物质。
生活中用到的金属材料是纯金属较多还是合金较多?
合金的性能比纯金属更优良
常见合金的硬度会比其成分金属大,合金的熔点一般比成分金属低。
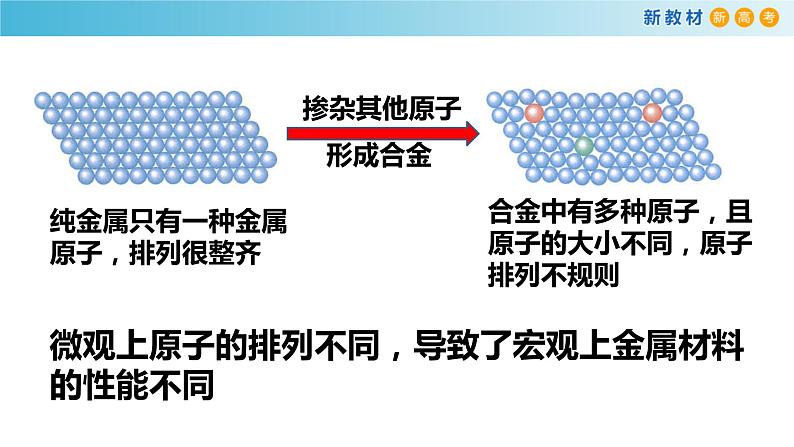
纯金属只有一种金属原子,排列很整齐
合金中有多种原子,且原子的大小不同,原子排列不规则
微观上原子的排列不同,导致了宏观上金属材料的性能不同
含碳量在2%~4.3%之间
含碳量在0.03%~2%之间
硬度大、抗压、性脆、可以铸造成型
延展性和机械性能好、可以锻轧和铸造
(含碳0.3%~0.6%)
(含碳0.03%~0.3%)
(含碳0.6%~2% )
在碳素钢中加入铬、锰、钨、硅等合金元素,使其具有特殊性能
不锈钢是最常见的合金钢,其合金元素是Cr和Ni
铝比较活泼,很容易与空气中的氧气反应在其表面形成一层致密的氧化膜,所以铝不要特殊的防腐措施。
分别向盐酸和氢氧化钠溶液中加入铝片,观察现象
刚开始反应较慢,后反应剧烈,生成气体,可以点燃
实验:在盐酸和氢氧化钠溶液中分别加铝片
单质铝和盐酸、氢氧化钠溶液都反应,现象相似,都生成氢气
2Al + 6HCl = 2AlCl3 + 3H2↑
等质量的铝与盐酸或者氢氧化钠溶液反应生成相同量的氢气
2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑
【练习】相同质量的两份铝,分别放入足量的盐酸和氢氧化钠溶液中,生成的氢气在同温同压下体积比为 。
2Al + 2OH- + 2H2O = 2AlO2- + 3H2↑
【思考与交流】在上面的实验中,我们还观察到,反应开始的时候气泡很少,后期才有大量气泡,产生这种现象的原因是什么?
铝的表面有氧化铝,刚开始是氧化铝和溶液反应,然后才是单质铝与溶液反应生成大量的氢气,这说明氧化铝和盐酸、氢氧化钠都能发生反应
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Al2O3 + 2NaOH = 2NaAlO2 + H2O
既能与酸反应生成盐和水,也能与碱反应生成盐和水的氧化物,叫做两性氧化物。
铝制餐具是否可以蒸煮或长时间存放酸(碱)性食物?
练习:根据氧化物的性质对下列氧化物进行分类:Na2O CO2 CO SO3 CaO FeO H2O Al2O3①酸性氧化物: 。②碱性氧化物: 。③两性氧化物: 。④和酸碱都不反应的是 。
CO2 SO3
Na2O CaO FeO
为什么生活中很少见到以纯铝为材料的制品?
纯铝的硬度和强度都比较小,不适合作为生产生活中的材料使用,使用较多的是具有不同组成和性质的铝合金。
硬铝中含Cu 4%、Mg 0.5%、Mn 0.5%、Si 0.7%,它密度小、强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料。
高中化学人教版 (2019)必修 第一册第二节 金属材料课堂教学ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二节 金属材料课堂教学ppt课件,共17页。PPT课件主要包含了金属特性,硬度大于各成分金属,熔点低于各成分金属,一般来说,碳素钢,低碳钢,高碳钢,中碳钢,铁合金,铁合金的分类等内容,欢迎下载使用。
高中化学必修一 3.2.1 铁合金 铝和铝合金课件: 这是一份高中化学必修一 3.2.1 铁合金 铝和铝合金课件,共14页。
高中化学必修一 3.2.1 铁合金 铝和铝合金课件新: 这是一份高中化学必修一 3.2.1 铁合金 铝和铝合金课件新,共19页。













