
高中化学人教版 (2019)必修 第一册实验活动2 铁及其化合物的性质第2课时教案设计
展开
这是一份高中化学人教版 (2019)必修 第一册实验活动2 铁及其化合物的性质第2课时教案设计,共6页。教案主要包含了Al3 的制备,铝的重要化合物等内容,欢迎下载使用。
课题
金属的化学性质
授课人
谭宗芹
课时安排
3
课型
新授课
授课时间
第9周
课标依据
根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要应用。
教材分析
在本节之前已经介绍了了金属钠、铝的化学性质,本节开始学习金属的重要化合物。本节是金属化学性质知识的延伸,知识由简单到复杂,符合学生的学习规律。
学情分析
高一1班:学生对于化学知识储备上,在已经学习了一些金属及其化合物的知识,学生容易接受,初步具备分析总结的能力,可以通过对已有知识的复习引导学生进行新课,在学习特点上比较被动,需要教师在课堂上灵活转变教学。
高一2班:在知识储备上和1班情况相同,课堂较不活跃,但有几个积极分子可以带活班级学习气氛。
高一4班:在知识储备上和前两个班情况相同,课堂较活跃,学生在学习积极性上较好。
三维目标
知识与能力
1、了解氧化铝的性质和主要用途
2、通过实验探究,认识氢氧化铝的的性质、实验室制备方法和主要用途
3、通过氧化铝和氢氧化铝的学习,了解两性氧化物和两性氢氧化物的性质。
过程与方法
1、培养学生发现问题、分析问题、解决问题的综合能力
2、加深对基本的理解和对化学反应规律的认识
情感态度与价值观
通过化学知识在日常生活中的具体应用,激发学生对化学的学习兴趣。
教学重难点
教学重点
氧化铝的两性和氢氧化铝的两性
教学难点
两性氢氧化物概念的形成
教法
与
学法
通过已有知识和实验现象加以引导,使学生自主得到结论。指导学生画铝及相关重要化合物的转化关系图
教学资源
Ppt 实验视频
教
学
活
动
设
计
师生活动
设计意图
批注
情景创设
ppt展示
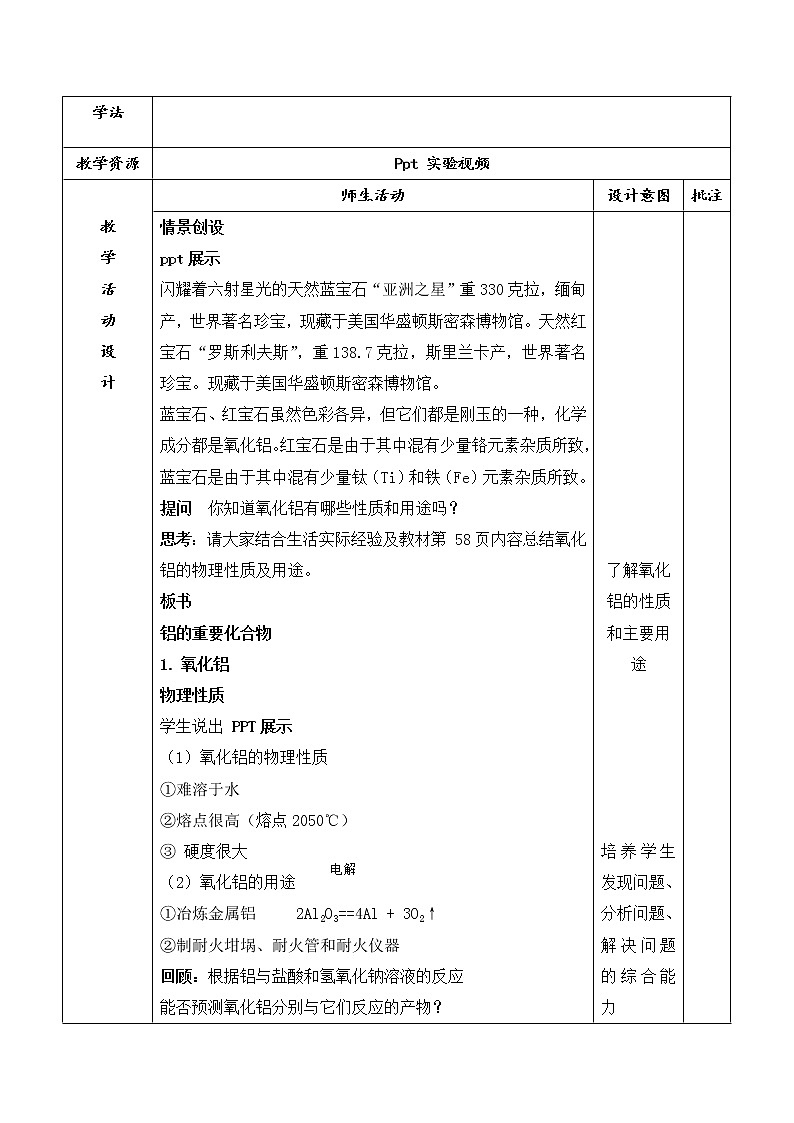
闪耀着六射星光的天然蓝宝石“亚洲之星”重330克拉,缅甸产,世界著名珍宝,现藏于美国华盛顿斯密森博物馆。天然红宝石“罗斯利夫斯”,重138.7克拉,斯里兰卡产,世界著名珍宝。现藏于美国华盛顿斯密森博物馆。
蓝宝石、红宝石虽然色彩各异,但它们都是刚玉的一种,化学成分都是氧化铝。红宝石是由于其中混有少量铬元素杂质所致,蓝宝石是由于其中混有少量钛(Ti)和铁(Fe)元素杂质所致。
提问 你知道氧化铝有哪些性质和用途吗?
思考:请大家结合生活实际经验及教材第 58页内容总结氧化铝的物理性质及用途。
板书
铝的重要化合物
氧化铝
物理性质
学生说出 PPT展示
(1)氧化铝的物理性质
①难溶于水
②熔点很高(熔点2050℃)
电解
③ 硬度很大
(2)氧化铝的用途
①冶炼金属铝 2Al2O3==4Al + 3O2↑
②制耐火坩埚、耐火管和耐火仪器
回顾:根据铝与盐酸和氢氧化钠溶液的反应
能否预测氧化铝分别与它们反应的产物?
板书
(3) 化学性质
引导学生自己写出化学方程式,并改写成离子方程式
板书
①与酸反应:Al2O3+ 6H+ = 2Al3++3H2O
②与碱反应:Al2O3+2OH– = 2AlO2–+H2O
结论:氧化铝既能跟强酸反应生成盐和水,又能跟强碱反应生成盐和水,所以氧化铝是两性氧化物。
讲Al2O3呈两性,那么它对应的水化物――Al(OH)3的性质又怎么样呢?
PPT展示
Al(OH)3的两性实验
板书2、氢氧化铝
问 我们从实验能得到什么结论?
板书
Al(OH)3是典型的两性氢氧化物
讲实验表明,Al(OH)3在HCl和NaOH溶液里都能溶解,这就说明它既能跟酸起反应,又能跟碱起反应。
引导学生自己写出化学方程式并拆成离子方程式。
板书(1)化学性质:
Al(OH)3+3H+==Al3++3H2O
Al(OH)3+OH―==AlO2―+2H2O
结论:氢氧化铝既能跟强酸反应生成盐和水,又能跟强碱反应生成盐和水,所以氢氧化铝是两性氢氧化物。
思考Al(OH)3能与所有碱液发生反应呢?
(不能,只能强碱溶液起反应)
板书氢氧化铝的不稳定性
2Al(OH)3Al2O3+3H2O
三、Al(OH)3 的制备
在实验室可以用铝盐溶液与NH3 ·H2O 反应来制取Al(OH)3
Al2(SO4)3+6NH3 ·H2O ==2Al(OH)3↓+3 (NH4)2SO4
引导学生拆写成离子方程式
Al3++3NH3 ·H2O == Al(OH)3 ↓+ 3NH4+
提问 实验室为什么常用氨水与硫酸铝溶液反应制取氢氧化铝,而不用氢氧化钠溶液呢?
由于 Al(OH)3不溶于弱酸、弱碱,用氢氧化钠溶液与硫酸铝溶液反应时,若加入NaOH溶液的量不足, Al3+不能完全转化为Al(OH)3;若加入NaOH溶液过量,则生成的Al(OH)3会被部分溶解,不易控制反应物的量。
Al(OH)3 的用途
净水
脱色剂
中和胃酸(胃舒平)
讨论:中和胃酸为什么要用Al(OH)3?能不能用其他的代替?
检测 引导学生画铝及相关重要化合物的转化关系图
了解氧化铝的性质和主要用途
培养学生发现问题、分析问题、解决问题的综合能力
通过实验探究,认识氢氧化铝的的性质、实验室制备方法和主要用途
通过氧化铝和氢氧化铝的学习,了解两性氧化物和两性氢氧化物的性质
通过化学知识在日常生活中的具体应用,激发学生对化学的学习兴趣。
当堂检测
有效练习
引导学生画铝及相关重要化合物的转化关系图
作业布置
铝及相关重要化合物的转化关系图中各个化学方程式和离子方程式
板书设计
二、铝的重要化合物
1、氧化铝(两性氧化物)
物理性质
化学性质
与酸反应Al2O3+6H+==2Al3++3H2O
与碱反应Al2O3+6OH―==2AlO2―+H2O
2、氢氧化铝(两性氢氧化物)
物理性质
化学性质:
与酸反应Al(OH)3+3H+==Al3++3H2O
与碱反应Al(OH)3+OH―==AlO2―+2H2O
不稳定 2Al(OH)3Al2O3+3H2O
(2)Al (OH)3 的制备
Al2(SO4)3+6NH3 ·H2O ==2Al(OH)3↓+3 (NH4)2SO4
Al3++3NH3 ·H2O == Al(OH)3 ↓+ 3NH4+
教学反思
备注
相关教案
这是一份人教版 (2019)必修 第一册第三章 铁 金属材料实验活动2 铁及其化合物的性质第2课时教案,共7页。教案主要包含了二氧化氮和一氧化氮等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)必修 第一册实验活动2 铁及其化合物的性质第2课时教学设计,共10页。教案主要包含了教师总结,演示实验,播放视频,教师启发等内容,欢迎下载使用。
这是一份人教版 (2019)实验活动1 配制一定物质的量浓度的溶液第1课时教案及反思,共11页。教案主要包含了钠的重要化合物等内容,欢迎下载使用。