所属成套资源:化学鲁科版必修1精品教案
高中化学鲁科版必修1第2节 氮的循环第1课时教案
展开
这是一份高中化学鲁科版必修1第2节 氮的循环第1课时教案,共7页。
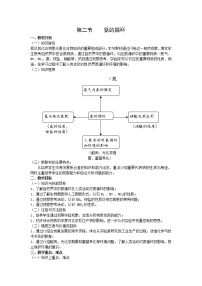
第2节 氮的循环知识脉络氮及其化合物是元素化合物知识的重要组成部分。本节教材通过闪电这一自然现象,激发学生思考自然界中的含氮物质,通过自然界中的氮循环,引出氮循环中的重要物质——氮气、NO、NO2、氨、铵盐、硝酸等,然后通过观察思考、实验探究认识这些重要物质的性质、用途。在学习过程中了解人类活动对自然界氮循环和环境的影响。本节教材内容知识框架教材特点从培养学生终身发展所必备的知识和能力出发,重点介绍重要代表物的性质与用途,同时注重培养学生的观察能力和综合分析问题的能力。课时分配:共2课时第1课时 自然界中的氮循环 氮气、一氧化氮和二氧化氮教学目标 1.课标要求(1)掌握氮气的化学性质(与氧气、氢气的反应)(2)了解一氧化氮、二氧化氮的物理性质(3)掌握一氧化氮与氧气的反应,二氧化氮与水的反应(4)认识氮循环对维持生态平衡的作用2.三维目标(1)知识与技能①了解自然界中的氮循环及人类活动对氮循环的影响;②通过了解生物固氮和人工固氮形式,认识N2、NO、NO2的性质。(2)过程与方法①培养学生搜集信息、处理信息的能力;②培养学生探究、观察、总结、分析问题的能力。(3)情感态度与价值观①通过介绍合成氨发展的艰辛历程,体会从实验室研究到工业生产的过程,渗透化学与技术关系的教育;②通过介绍酸雨,光化学烟雾和富营养化等环境问题,了解人类活动对氮循环的影响,树立保护环境的意识。教学分析 1.教材分析本节教材是以氮元素在自然界存在的形式为背景,引发学生联想自然界中的“闪电”现象,让学生带着“闪电时,空气中的氮气发生了哪些化学变化?变化过程产生的物质对人类的生活与生产有什么意义?”等质疑进入自然界中氮循环的学习,并以氮循环中N2、NO、NO2、HNO3、NH3、铵盐等重要的物质的性质及相互转化为核心知识,同时联系环境保护问题,让学生初步了解人类活动对自然界氮循环和环境的影响。教材采用了“从自然界→化学→社会→实验室→社会生活”教学脉络,进一步拓宽了学生认识元素与物质的视野,为今后构建重要的元素及物质的知识网络奠定重要基础。2.学情分析关于元素化合物的学习,在第1章已经学习了研究物质性质的基本方法和程序,在第3章第1节又学习了碳的多样性,这是学生已有的基础知识储备,另一方面氮及其化合物的知识学生相对陌生,本节以氮在自然界中的循环为探究的起点,符合学生的认知情况。教学重点、难点 1.重点 氮气、氮的氧化物(NO、NO2)的性质、氮的固定2.难点 氮气、氮的氧化物(NO、NO2)的性质教学方法 实验引导法、探究法、归纳法课前准备 1.教学媒体、课件;2.相关实验仪器及药品仪器:空矿泉水塑料瓶、感应圈、单孔橡皮塞药品:蒸馏水、红色石蕊试纸板书设计 第3章 自然界中的元素第2节 氮的循环一、氮在自然界中的循环1.存在:游离态和化合态2.基本过程及示意分析(学生汇报展示)二、氮循环中的重要物质及其变化1.氮气与氮的固定(1)N2+O2,2NO(NO有毒、无色气体、难溶于水)(2)2NO+O2===2NO2(NO2有毒、红棕色气体、能与水反应)(3)3NO2+H2O===2HNO3+NON2+3H22NH3(可逆反应)氮的固定情景导入 导入设计一:播放 “闪电”“雷雨发庄稼”等动画及幻灯片。并提出问题:闪电是我们生活中司空见惯的现象,为什么闪电过后庄稼长势会更旺,这里面涉及了哪些物质发生了哪些反应?今天我们就一起来研究《氮的循环》这一节内容。【设计思路】以学生所熟悉的自然界的“闪电”和农谚入手,创设相关问题和情景,让学生认识到含氮元素的物质广泛存在于自然界中,它们之间可以相互转化,激发学生学习新课的兴趣和探究的动机。导入设计二闪电是我们最熟悉的自然现象,让我们来感受一下!(利用多媒体给学生展示电闪雷鸣的情景——动画伴声音),在这电闪雷鸣的雨天,空气中的氮气能否发生某些反应,这些反应对我们的生产和生活有什么实际意义?我们带着这些疑问来学习本节内容——氮的循环。【设计思路】从熟悉的自然现象入手,引发思考,聚敛思维,把学生带入本节课学习的场景中来。推进新课 【问题思考】上节课后老师给大家布置了以下2项探究任务:请以小组为单位汇报你们的探究结果任务1.预习课本查阅资料,查找为什么“雷雨能发庄稼”?在电闪雷鸣时,氮气和有关氮的化合物发生了哪些反应?这些反应和生成的物质对人类的生产生活有什么影响?任务2.查找氮循环的资料,小组合作画出氮循环简单图示,并写出短文,重点说明氮循环中涉及哪些含氮元素的物质,它们是如何转化的?【成果展示】学生汇报展示查阅课本或相关资料所得结论。(也可上黑板演示画图,以下是部分小组的氮循环示意图) 【设计思路】学生能解决的问题一定要让学生自己解决。通过提前布置任务让学生查阅课本资料及联系身边化学,了解氮元素在自然界存在形式。让学生分组交流,培养学生自主探究及小组合作学习意识,让学生进一步认识到空气中的氮元素与前一节课学过的碳元素一样在自然界中能实现循环,为下面要学习的各种重要物质做铺垫,也为日后学生的研究性学习提供素材。【概括整合】自然界中氮元素存在的形式有两种:一种是游离态,如N2;另一种是化合态,如铵盐、硝酸盐(如KNO3、NaNO3)、氨、蛋白质等。【情景导入】在氮循环中涉及了较多重要的含氮元素的物质及其变化,下面我们一起来探讨这些物质的性质及转化。【设计思路】将教学内容自然转移到第二部分氮循环中的重要物质及其变化。【问题思考】N2在空气中的体积分数约占78%,N2与O2一样,可以说与我们朝夕相处,请同学们谈一下对N2的认识。【设计思路】由于学生在日常生活及初中化学中已经对氮气的物理性质和化学性质有所了解,所以设计这一环节的目的是温故知新,使学生意识到氮气的化学性质不活泼,从而激发学生对氮气性质稳定原因的思考。【知识支持】氮气是由氮原子构成的双原子分子,两个氮原子间共用三对电子,使每个原子都达到稳定结构。要破坏这种牢固的结合,需要很高的能量。故常温下,氮气的化学性质不活泼,很难与其他物质发生反应。但在一定的条件下,氮气能与氧气、氢气等物质发生反应。下面我们就通过一个实验来模拟放电条件下氮气和氧气的反应。【设计思路】结构决定性质,此处把N2的结构做一简略介绍,目的是帮助学生进一步理解N2性质稳定的原因。此处学生可能较难理解,可以打一个比喻,“一根筷子,三根筷子,哪个更容易断?学生自然就理解了。【观察思考】在一个空矿泉水塑料瓶距瓶底10 cm处,对称地钻两个小孔,然后放在感应圈上,将感应圈的两根极针通过小孔插入瓶中,使两根极针成一条直线,且针尖之间相距0.5 cm(如图),接通电源观察实验现象。待矿泉水瓶中产生红棕色气体后,加入蒸馏水振荡,用蓝色石蕊试纸检验产生的溶液。(若条件不允许可以播放N2与O2反应的视频)【讨论互动】请仔细观察实验现象,结合前面提到的“闪电”等现象,思考并回答以下两个问题:1.为什么通电时矿泉水瓶中会产生红棕色气体?2.蓝色石蕊试纸颜色为什么会变红?请推测生成的产物是什么?【设计思路】自然界中的闪电司空见惯,但在电闪雷鸣之际到底发生了哪些化学反应,可能知之者甚少,此处将自然界的现象拿到实验室中进行模拟实验,通过演示实验及问题的提出,培养学生的观察能力、分析能力及解决问题的能力,让学生进一步体会化学科学的魅力与作用。【归纳总结】在放电或高温的条件下,空气中的氮气能与氧气发生反应,生成一氧化氮,一氧化氮在空气中很不稳定,易被氧化成二氧化氮,二氧化氮与水反应生成硝酸。【板书】①N2+O2,2NO(NO有毒、无色气体、难溶于水)②2NO+O2===2NO2(NO2有毒、红棕色气体、能与水反应)③3NO2+H2O===2HNO3+NO【设计思路】通过对演示实验或视频的分析师生一起总结出“雷雨发庄稼”的原因,解决了课前导入所提出的问题,也解决了这节课的重难点问题。【概括整合】氮的氧化物都有毒,都是大气污染物。请比较它们的性质,完成下表。 NONO2物理性质____色____溶于水的有毒气体____色有____气味,____溶于水的有毒气体化学性质H2O O2 收集方法只能用________________________________法【设计思路】以表格的形式进一步明确NO、NO2的主要性质,培养学生分析对比能力。【情景导入】植物只能利用化合态的氮,除了闪电等自然方法外,能否用人工的方法把空气中的氮气转化为植物可吸收的含氮化合物呢?通过大量实验研究,科学家们发现在一定条件下,氮气和氢气可以直接化合生成氨。【设计思路】此处意在由自然固氮转到人工固氮。【自主学习】引导学生阅读课本72页合成氨的反应方程式及[知识点击]栏目,认识什么是可逆反应。【板书】N2+3H22NH3(可逆反应)【设计思路】指导学生阅读教材[知识点击],让学生初步认识什么是可逆反应,为后续研究化学平衡的移动建立基础。【教师点拨】像这样使空气中游离态的氮转化为化合态的氮的方法叫做氮的固定。【研究学习】请同学们根据刚才的讲解以及教材内容总结氮的固定的方式。【概括整合】氮的固定课堂小结 留给学生一定时间自主概括整合本节所学。教学反思 我们的教学设计应“以生为本”,落实“提高学生科学素养”的教育宗旨,渗透STS教育,促进学生的自我发展。知识技能可以通过学习来获得,但是过程与方法、情感态度与价值观却难以靠知识灌输来形成,它们必须靠在具体的活动过程中不断体验、内化而形成。因此本课时以“固氮”为线索,设计以学生为中心的探究活动,将课堂还给学生。这样做有两方面的好处:一是教学内容设计更加连贯和系统,学生对知识的掌握更加深刻,学习效果好。二是学生通过直观生动的实验来学习,印象深刻,学习热情高,能主动思考,课堂气氛活跃,增强了学生之间合作学习,分析解决问题的能力,体现了新的教育理念。课堂作业 1.在新疆和青海两省交界处,有一狭长山谷,有时牧民和牲畜进入后,风和日丽的晴天顷刻间会电闪雷鸣,狂风大作,人畜常遇雷击而倒毙,被当地牧民称为“魔鬼谷”。奇怪的是这里草木茂盛,你知道其中的原因吗?写出有关的化学方程式。答案:其化学方程式是:N2+O22NO 2NO+O2===2NO2 3NO2+H2O===2HNO3+NO2.下列反应中,起固氮作用的是( )。A.N2与H2在一定条件下反应生成NH3B.硝酸工厂用NH3氧化制NOC.雷雨时空气中的N2转化为NOD.由NH3制碳酸氢铵和硫酸铵答案:AC3.在大气中N2是很有用的,因为( )。A.助燃B.稀释大气中O2的浓度,使燃烧及腐败速度减慢C.帮助呼吸D.帮助植物光合作用答案:B4.在NO2与水的反应中,NO2( )。A.既不是氧化剂,又不是还原剂B.只是氧化剂C.既是氧化剂,又是还原剂D.只是还原剂答案:C5.用大试管收集一试管NO2气体,倒扣在盛水的水槽里,不久看到试管红棕色气体消失,试管里水面上升至容积的大约2/3处。再往试管里通入适量的氧气,又出现红棕色,接着红棕色又消失,液面又上升。试解释上述现象的原因。答案:NO2为红棕色、有刺激性气味的气体,它与水反应生成硝酸与一氧化氮,3体积的二氧化氮与水反应减少了2体积,故水的液面上升至容积的2/3处。通入氧气后,一氧化氮与氧气反应再生成二氧化氮,二氧化氮又与水反应,液面又会上升。
相关教案
这是一份高中化学鲁科版必修1第2节 氮的循环第2课时教案,共10页。
这是一份高中化学第3章 自然界中的元素第2节 氮的循环教学设计,共8页。
这是一份高中鲁科版第2节 氮的循环教学设计,共7页。