

2020版新一线高考化学(人教版)一轮复习教学案:第8章第3节 盐类的水解
展开第三节 盐类的水解
考纲定位 | 核心素养 |
1.了解盐类水解的原理。 2.了解影响盐类水解的主要因素。 3.了解盐类水解的应用。 4.能正确书写盐类水解的化学或离子方程式。 | 1.变化观念——从盐类的水解反应认识化学变化的原理及应用。 2.平衡思想——能从动态的角度分析水解平衡的实质原理、特征和影响因素。 3.模型认知——建立溶液中粒子浓度比较模型如电荷守恒、物料守恒和质子守恒模型。 |
考点一| 盐类的水解原理
1.盐类的水解实质与特点
(1)定义
在溶液中盐电离出来的离子跟水电离产生的H+或OH-结合生成弱电解质的反应。
(2)实质
―→c(H+)≠c(OH-)―→溶液不再呈中性。
(3)水解常数(Kh)
以CH3COO-+H2OCH3COOH+OH-为例,表达式为=Kh=。
(4)特点
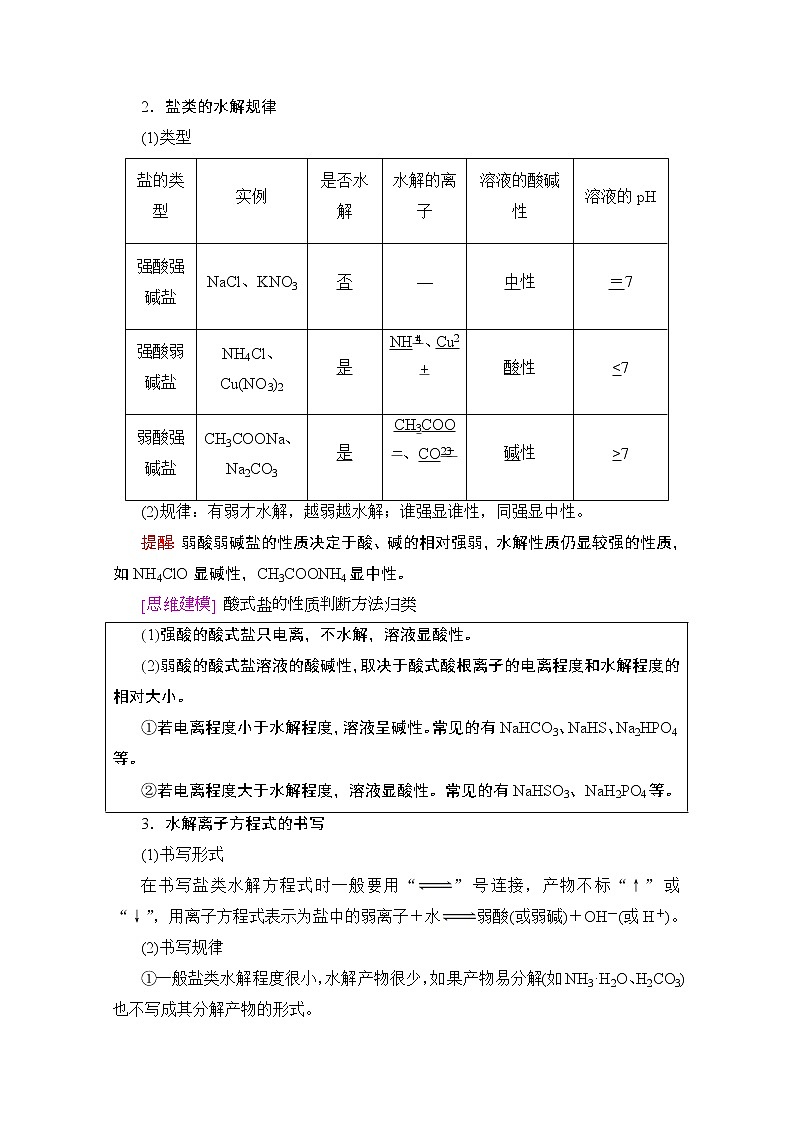
2.盐类的水解规律
(1)类型
盐的类型 | 实例 | 是否水解 | 水解的离子 | 溶液的酸碱性 | 溶液的pH |
强酸强碱盐 | NaCl、KNO3 | 否 | — | 中性 | =7 |
强酸弱碱盐 | NH4Cl、Cu(NO3)2 | 是 | NH、Cu2+ | 酸性 | <7 |
弱酸强碱盐 | CH3COONa、Na2CO3 | 是 | CH3COO-、CO | 碱性 | >7 |
(2)规律:有弱才水解,越弱越水解;谁强显谁性,同强显中性。
提醒:弱酸弱碱盐的性质决定于酸、碱的相对强弱,水解性质仍显较强的性质,如NH4ClO显碱性,CH3COONH4显中性。
1强酸的酸式盐只电离,不水解,溶液显酸性。
2弱酸的酸式盐溶液的酸碱性,取决于酸式酸根离子的电离程度和水解程度的相对大小。
①若电离程度小于水解程度,溶液呈碱性。常见的有NaHCO3、NaHS、Na2HPO4等。
②若电离程度大于水解程度,溶液显酸性。常见的有NaHSO3、NaH2PO4等。
3.水解离子方程式的书写
(1)书写形式
在书写盐类水解方程式时一般要用“”号连接,产物不标“↑”或“↓”,用离子方程式表示为盐中的弱离子+水弱酸(或弱碱)+OH-(或H+)。
(2)书写规律
①一般盐类水解程度很小,水解产物很少,如果产物易分解(如NH3·H2O、H2CO3)也不写成其分解产物的形式。
②多元弱酸盐的水解分步进行,以第一步为主,一般只写第一步水解的离子方程式,如Na2CO3的水解离子方程式:CO+H2OHCO+OH-。
③多元弱碱阳离子的水解方程式一步写完,如FeCl3的水解离子方程式:Fe3++3H2OFe(OH)3+3H+。
提醒:水解分别是酸性和碱性的离子组由于相互促进水解程度较大生成气体或沉淀的,书写时要用“===”“↑”“↓”,但水解不生成气体或沉淀,水解不完全,书写仍用“”。如2Al3++3CO+3H2O===2Al(OH)3↓+3CO2↑;CH3COO-+NH+H2OCH3COOH+NH3·H2O。
1.正误判断(正确的打“√”,错误的打“×”)
(1)盐类水解的实质是促进水电离,水电离平衡右移。 ( )
(2)能水解的盐溶液一定呈酸性或碱性,不可能呈中性。 ( )
(3)NaHSO3溶液显酸性的理由是HSO只电离不水解。 ( )
(4)25 ℃,pH=11的Na2CO3溶液中水电离出的c(OH-)=1×10-11 mol·L-1。
( )
(5)25 ℃,水电离出的c(H+)=1×10-5 mol·L-1的溶液一定显酸性。 ( )
答案:(1)√ (2)× (3)× (4)× (5)×
2.写出下列盐的水解离子方程式。
(1)(NH4)2SO4______________________________________________。
(2)Na2S___________________________________________________。
(3)NaHSO3________________________________________________。
(4)NaAlO2_________________________________________________。
(5)FeCl3___________________________________________________。
答案:(1)NH+H2ONH3·H2O+H+
(2)S2-+H2OHS-+OH-
(3)HSO+H2OH2SO3+OH-
(4)AlO+2H2OAl(OH)3+OH-
(5)Fe3++3H2OFe(OH)3+3H+
⊙考法1 盐类水解的实质规律
1.25 ℃时,浓度均为0.1 mol·L-1的溶液,其pH如下表所示。有关说法正确的是( )
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.0 | 8.4 |
A.酸性强弱:H2CO3>HF
B.水的电离程度:①=②
C.③中水电离出的c(OH-)=1×10-8 mol·L-1
D.④中显碱性的原因是HCO的水解程度大于其电离程度
D [A项,水解程度越大,酸越弱,故酸性H2CO3<HF,错误;B项,CH3COONH4水解,NaCl不水解,水的电离程度不同,错误;C项,NaF水解促进水的电离,c(OH-)H2O=10-6 mol·L-1,错误;D项正确。]
2.(2019·大庆模拟)25 ℃时,实验测得0.10 mol·L-1的NaHB溶液的pH=9.1。下列说法中正确的是( )
A.NaHB的电离方程式为:NaHB===Na++H++B2-
B.HB-在水溶液中只存在HB-的水解平衡
C.HB-的水解程度大于电离程度
D.溶液中水电离出的c(H+)为10-9.1 mol·L-1
C [HB-在水中不完全电离,A错误;HB-在水中水解程度大于电离程度,B错误,C正确;HB-以水解为主,促进水的电离,D错误。]
⊙考法2 Kh的有关计算与换算
3.25 ℃ 0.01 mol·L-1的NaA溶液pH=10-10,则A-的水解常数表达式为________,其值约为________。
解析:Kh=≈≈10-6。
答案:Kh= 10-6
4.已知常温下H2SO3的电离常数Ka1=1.0×10-2,Ka2=6.0×10-8,则SO的水解常数Kh1=________,Kh2=________。若常温下,pH=9的Na2SO3溶液中=________。
解析:SO+H2OHSO+OH-
HSO+H2OH2SO3+OH-
Kh1===,
故==60,
Kh2===1×10-12。
答案:1.67×10-7 1×10-12 60
考点二| 盐类水解的影响因素及应用
1.盐类水解的影响因素
(1)内因——主要因素
弱酸根离子、弱碱阳离子对应的酸、碱越弱,就越易发生水解,溶液的碱性或酸性越强。
如酸性(或Ka)CH3COOH>H2CO3>HCO可知同浓度的CH3COONa、NaHCO3、Na2CO3的水解程度依次增大,pH依次增大。
(2)外界因素对盐类水解的影响
因素 | 水解平衡 | 水解程度 | 水解产生离子的浓度 | |
温度 | 升高 | 右移 | 增大 | 增大 |
浓度 | 增大 | 右移 | 减小 | 增大 |
减小(即稀释) | 右移 | 增大 | 减小 | |
外加酸、碱 | 酸 | 弱碱阳离子的水解程度减小 | ||
碱 | 弱酸根离子的水解程度减小 | |||
外加其他盐 | 水解形式相同的盐 | 相互抑制(如NH4Cl中加FeCl3) | ||
水解形式相反的盐 | 相互促进[如Al2(SO4)3中加NaHCO3] | |||
提醒:(1)稀溶液中,盐的浓度越小,水解程度越大,但由于溶液体积的增大是主要的,故水解产生的H+或OH-的浓度是减小的,则溶液酸性(或碱性)越弱;(2)向CH3COONa溶液中加入少量冰醋酸,并不会与CH3COONa溶液水解产生的OH-反应,使平衡向水解方向移动,原因是体系中c(CH3COOH)增大是主要因素,会使平衡CH3COO-+H2OCH3COOH+OH-左移。
2.盐类水解的“六”大类应用
(1)判断离子能否共存
若阴、阳离子发生水解相互促进的反应,水解程度较大而不能大量共存,有的甚至水解完全。常见的水解相互促进的反应进行完全的有:
①Al3+与HCO、CO、AlO、SiO、HS-、S2-、ClO-。
②Fe3+与HCO、CO、AlO、SiO、ClO-。
③NH与SiO、AlO。
(2)判断盐溶液蒸干时所得的产物
①盐溶液水解生成难挥发性酸和酸根阴离子易水解的强碱盐,蒸干后一般得原物质,如CuSO4(aq)蒸干得CuSO4;Na2CO3(aq)蒸干得Na2CO3(s)。
②盐溶液水解生成易挥发性酸时,蒸干灼烧后一般得对应的氧化物,如AlCl3(aq)蒸干得Al(OH)3,灼烧得Al2O3。
③弱酸的铵盐蒸干后无固体。如NH4HCO3、(NH4)2CO3。
(3)保存、配制某些盐溶液
如配制FeCl3溶液时,为防止出现Fe(OH)3沉淀,常加几滴盐酸来抑制FeCl3的水解;在实验室盛放Na2CO3、CH3COONa、Na2S等溶液的试剂瓶不能用玻璃塞,应用橡胶塞。
(4)利用盐类的水解反应制取胶体、净水
如实验室制备Fe(OH)3胶体的原理为
FeCl3+3H2OFe(OH)3(胶体)+3HCl。
明矾净水的原理为Al3+水解生成氢氧化铝胶体,胶体具有很大的表面积,吸附水中悬浮物而聚沉。
(5)泡沫灭火器的原理
NaHCO3与Al2(SO4)3的饱和溶液混合
Al3++3HCO===Al(OH)3↓+3CO2↑。
(6)铵态氮肥与草木灰不能混用,某些盐溶液(如ZnCl2、NH4Cl)作除锈剂。
正误判断(正确的打“√”,错误的打“×”)
(1)因为0.1 mol·L-1 Na2CO3溶液的pH大于0.1 mol·L-1 Na2SO3溶液的pH故可推知酸性H2CO3<H2SO3。 ( )
(2)加热0.1 mol·L-1 Na2CO3溶液,CO的水解程度和溶液的pH均增大。
( )
(3)将氯化铵溶液加水稀释时,的值减小。 ( )
(4)配制FeCl3溶液时可以用稀盐酸溶解FeCl3。 ( )
(5)NH4F溶液可以放在带塑料塞的玻璃瓶中。 ( )
(6)铁盐和铝盐可作净水剂的原因是二者水解生成胶体。 ( )
答案:(1)× (2)√ (3)√ (4)√ (5)× (6)√
⊙考法1 盐类水解的影响因素
1.用一价离子组成的四种盐溶液:AC、BD、AD、BC,其物质的量浓度均为1 mol·L-1。在室温下前两种溶液的pH=7,第三种溶液的pH>7,最后一种溶液pH<7,则正确的是( )
| A | B | C | D |
碱性 | AOH>BOH | AOH<BOH | AOH>BOH | AOH<BOH |
酸性 | HC>HD | HC>HD | HC<HD | HC<HD |
A [根据AD溶液pH>7,D-一定水解;根据BC溶液pH<7,B+一定水解;根据BD溶液pH=7,B+、D-的水解程度相同;A+、C-均不水解,或水解程度比B+、D-弱,所以碱性:AOH>BOH,酸性:HC>HD。]
2.(2019·武汉模拟)已知常温下浓度为0.1 mol·L-1的下列溶液的pH如表所示:
溶质 | NaF | NaClO | Na2CO3 |
pH | 7.5 | 9.7 | 11.6 |
下列说法正确的是( )
A.加热0.1 mol·L-1 NaClO溶液测其pH,pH小于9.7
B.0.1 mol·L-1 Na2CO3溶液加水稀释,CO的水解平衡右移,pH变大
C.根据上表数据得出三种酸电离平衡常数大小关系为HF>HClO>H2CO3(二级电离平衡常数)
D.0.1 mol·L-1 NaF溶液中加入Na2CO3,F-的水解程度变大
C [A项,加热促进盐水解,pH>9.7,错误;B项,加水稀释碱性变弱,pH变小,错误;C项,水解程度越大,pH越大,相应的酸越弱,正确;D项,加Na2CO3,抑制F-水解,错误。]
⊙考法2 盐类水解的应用
3.下列根据反应原理设计的应用,不正确的是( )
A.CO+H2OHCO+OH- 热的纯碱溶液清洗油污
B.Al3++3H2OAl(OH)3+3H+ 明矾净水
C.TiCl4+(x+2)H2O(过量) TiO2·xH2O↓+4HCl 制备TiO2·xH2O
D.SnCl2+H2OSn(OH)Cl+HCl 配制氯化亚锡溶液时加入氢氧化钠
D [热的纯碱溶液碱性增强、去污能力增强;Al3+水解生成Al(OH)3胶体,吸附水中的悬浮物,具有净水作用;TiCl4与H2O作用水解可以制得纳米材料TiO2·xH2O,A、B、C项正确;SnCl2易水解,配制SnCl2溶液时若加入NaOH溶液,会促进SnCl2水解而生成Sn(OH)Cl或Sn(OH)2沉淀,所以配制SnCl2溶液应将SnCl2固体溶于浓盐酸中,再稀释至所需浓度。]
4.(2019·佛山模拟)下列物质的水溶液在空气中小心加热蒸干至质量不再减少为止,能得到较纯净的原溶质的是( )
①CuSO4 ②FeSO4 ③K2CO3 ④Ca(HCO3)2
⑤NH4HCO3 ⑥KMnO4 ⑦FeCl3
A.全部都可以 B.仅①②③
C.仅①③⑥ D.仅①③
D [FeSO4溶液加热过程中生成Fe(OH)2和H2SO4,又由于Fe(OH)2会被氧化生成Fe(OH)3,故蒸干后得不到原溶后;Ca(HCO3)2受热会分解生成CaCO3;NH4HCO3受热分解;KMnO4受热分解生成K2MnO4和MnO2;FeCl3受热促进水解生成Fe(OH)3和盐酸,而盐酸挥发进一步促进其水解,最终水解彻底,得不到原溶质。]
课堂反馈 真题体验
1.(2017·全国卷Ⅱ,T12)改变0.1 mol·L-1二元弱酸H2A溶液的pH,溶液中H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示[已知δ(X)=]。
下列叙述错误的是( )
A.pH=1.2时,c(H2A)=c(HA-)
B.lg[K2(H2A)]=-4.2
C.pH=2.7时,c(HA-)>c(H2A)=c(A2-)
D.pH=4.2时,c(HA-)=c(A2-)=c(H+)
D
2.(2014·全国卷Ⅱ,T11)一定温度下,下列溶液的离子浓度关系式正确的是( )
A.pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol·L-1
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+c(H+)=c(OH-)+c(HC2O)
D.pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>②>③
D [A.pH=5的H2S溶液中H+的浓度为1×10-5 mol·L-1,但是HS-的浓度会小于H+的浓度,H+来自于H2S的第一步电离、HS-的电离和水的电离,故H+的浓度大于HS-的浓度,错误。B.弱碱不完全电离,弱碱稀释10倍时,pH减小不到一个单位,a<b+1,故不正确。C.草酸是弱酸,氢氧化钠是强碱,无论怎样混合得到的溶液都符合电荷守恒,而该等式中缺少草酸根,不符合电荷守恒,故不正确。D.因为醋酸的酸性>碳酸的酸性>次氯酸的酸性,根据越弱越水解的原则,pH相同的三种钠盐,浓度的大小关系为醋酸钠>碳酸氢钠>次氯酸钠,则钠离子的浓度为①>②>③,故D正确。]








