

【化学】广东省佛山一中、石门中学、顺德一中、国华纪中2018-2019学年高二下学期期末四校联考试题
展开广东省佛山一中、石门中学、顺德一中、国华纪中2018-2019学年高二下学期期末四校联考试题
注意事项:
1.答题前,考生务必用黑色笔迹的钢笔或签字笔将自己的班级、姓名、考号填写在答题卡上。
2.第I卷答在答题卡上,每小题选出答案后,用 2B 铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3. 非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如要作图(含辅助线)或画表,先用铅笔进行画线、绘图,再用黑色字迹的钢笔或签字笔描黑。如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.作答选做题时,请先用 2B 铅笔填涂选做题的题组号对应的信息点,再作答。漏涂、错涂、多涂的,答案无效。
5. 本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共6页,满分100分,考试用时90分钟。
6. 可能用到的相对原子质量: H 1 B 11 C 12 N 14 O 16 Na 23 Si 28 Cl 35.5 Ar 40 Ca 40 Ni 59 Fe 56 Cu 64
第I部分(选择题,分为必做和选做,共40分)
一、必做选择题(本题包括1-10小题,只有一个选项符合题意。每小题2分,共20分)
1.下列说法错误的是( )
A.熊猫可以竹子为食,研究其消化机理有可能用来解决人类粮食危机;
B.中医是传统瑰宝之一,中草药的研究和应用可以解决人类某些重大疾病;
C.煤焦炭可以用来较大规模地制取钻石,钻石永流传的说法值得怀疑;
D.塑料的大量使用可能会产生白色污染,因此全球应该禁止广泛使用。
2.下列用品中主要由合成材料制造的是( )
A.宇航服 B.宣纸 C.羊绒衫 D.棉衬衣
3.下列有关有机物的说法不正确的是( )
A.酒精中是否含有水,可用金属钠检验
B.有机酸和醇脱水合成的某些酯,可用作糖果、化妆品中的香料
C.蛋白质在一定条件下能发生水解反应,生成氨基酸
D.乙烯通过聚合反应可合成聚乙烯,聚乙烯塑料可用来制造多种包装材料
4.下列关于有机化合物的说法正确的是( )
A.2-甲基丁烷也称异丁烷
B.三元轴烯()与苯互为同分异构体
C.C4H9Cl有3种同分异构体
D.烷烃的正确命名是2-甲基-3-丙基戊烷
5.下列关于有机化合物的说法正确的是( )
A.乙醇和乙酸都存在碳氧双键
B.甲烷和乙烯都可以与氯气反应
C.高锰酸钾可以氧化苯和甲烷
D.乙烯可以与氢气发生加成反应,苯不能与氢气加成
6. 某有机物的结构为 , 这种有机物不可能具有的性质是( )
A.能跟NaOH溶液反应 B.能使酸性KMnO4溶液褪色
C.能发生酯化反应 D.能发生水解反应
7.下列关于有机物的说法正确的是( )
A.实验室制备硝基苯加入试剂的顺序为:先加入浓硫酸,再滴加苯,最后滴加浓硝酸
B.蔗糖和葡萄糖不是同分异构体,但属同系物
C.可用金属钠区分乙酸、乙醇和苯
D.石油裂解和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化
8. 苯环结构中,不存在单双键交替结构,可以作为证据的事实是( )
①苯不能使酸性KMnO4溶液褪色 ②苯分子中碳原子间的距离均相等 ③苯能在一定条件下跟H2加成生成环已烷 ④经实验测得邻二甲苯仅一种结构 ⑤苯在FeBr3存在条件下与液溴发生取代反应,但不因化学变化而使溴水褪色
A.②③④⑤ B.①②③④ C.①②④⑤ D.①③④⑤
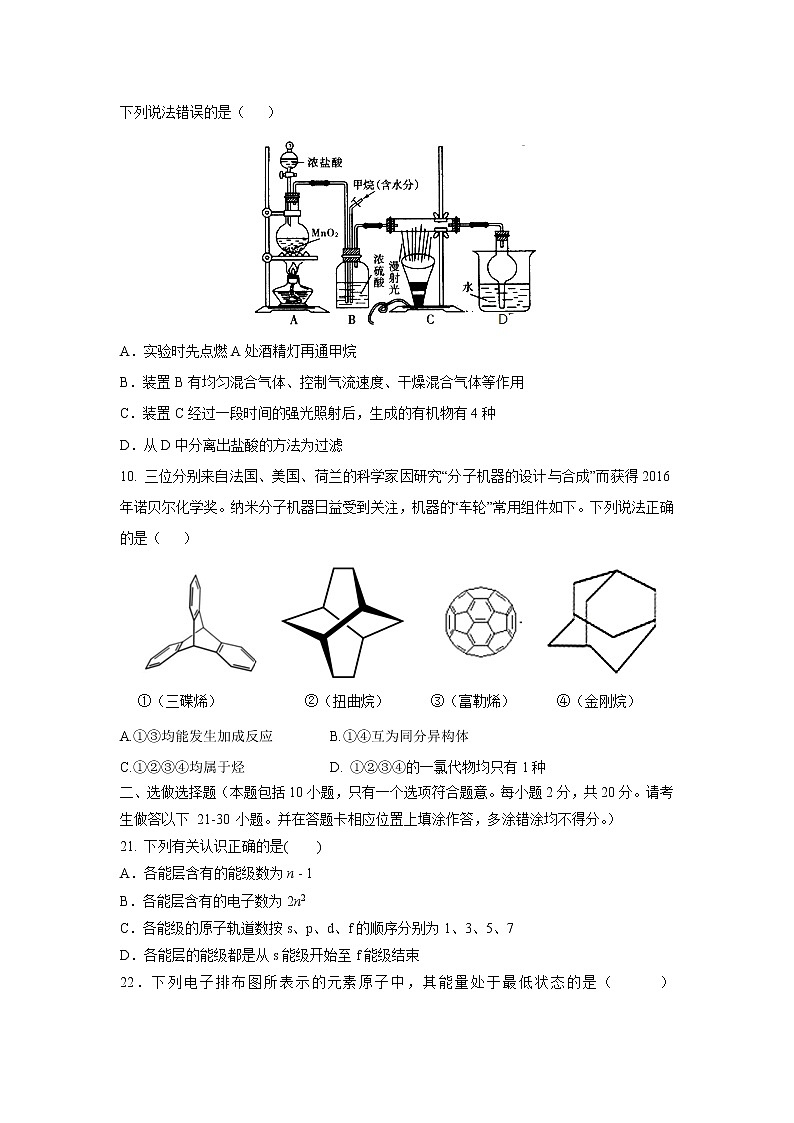
9.兴趣小组在实验室中模拟利用甲烷和氯气发生取代反应制取副产品盐酸,设计如图装置,下列说法错误的是( )
A.实验时先点燃A处酒精灯再通甲烷
B.装置B有均匀混合气体、控制气流速度、干燥混合气体等作用
C.装置C经过一段时间的强光照射后,生成的有机物有4种
D.从D中分离出盐酸的方法为过滤
10. 三位分别来自法国、美国、荷兰的科学家因研究“分子机器的设计与合成”而获得2016年诺贝尔化学奖。纳米分子机器日益受到关注,机器的“车轮”常用组件如下。下列说法正确的是( )
A.①③均能发生加成反应 B.①④互为同分异构体
C.①②③④均属于烃 D. ①②③④的一氯代物均只有1种
二、选做选择题(本题包括10小题,只有一个选项符合题意。每小题2分,共20分。请考生做答以下 21-30 小题。并在答题卡相应位置上填涂作答,多涂错涂均不得分。)
21. 下列有关认识正确的是( )
A.各能层含有的能级数为n - 1
B.各能层含有的电子数为2n2
C.各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7
D.各能层的能级都是从s能级开始至f能级结束
22.下列电子排布图所表示的元素原子中,其能量处于最低状态的是( )
23.下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ·mol-1)。
| I1 | I2 | I3 | I4 | …… |
R | 740 | 1 500 | 7 700 | 10 500 | …… |
下列关于元素R的判断中一定正确的是( )
A.R的最高正价为+3价
B.R元素位于元素周期表中第ⅡA族
C.R元素的原子最外层共有4个电子
D.R元素基态原子的电子排布式为1s22s2
24. 下表所列的是不同物质中氧氧键的键长和键能的数据,其中a和b未测出,根据一个原则可估计键能大小顺序为d>c>b>a,该原则是( )
| O | O | O2 | O |
键长(nm) | 149 | 128 | 121 | 112 |
键能(kJ/mol) | a | b | c=494 | d=628 |
A.成键电子数越多,键能越大 B.成键电子数越少,键能越大
C.键长越短的键,键能越大 D.以上都不是
25. 已知SO3、BF3、CCl4、PCl5、SF6都是非极性分子,而H2S、NH3、NO2、SF4、BrF5都是极性分子,由此可推出ABn型分子属于非极性分子的经验规律是( )
A.ABn型分子中A、B均不为氢原子
B.A元素的相对原子质量必小于B元素的相对原子质量
C.分子中所有原子都在同一平面上
D.分子中A原子最外层电子都已成键
26. 下列物质的熔沸点高低顺序中,正确的是( )
A.金刚石>晶体硅>二氧化硅>碳化硅 B.CI4>CBr4>CCl4>CH4 C.金刚石>生铁>纯铁>钠 D.MgO>H2O>N2>O2
27.在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是( )
A.sp,范德华力 B.sp2,氢键 C.sp2,范德华力 D.sp3,氢键
28. 某研究所发现了一种新的球形分子,它的分子式为C60Si60,其分子结构好似中国传统工艺品“镂雕”,经测定其中包含C60,也有Si60结构。下列叙述正确的是( )
A.该物质有很高的熔点、很大的硬度 B.该物质形成的晶体属分子晶体
C.该物质分子中Si60被包裹在C60里面 D.该物质的相对分子质量为1200
29. 有下列离子晶体立体结构示意图:
若以M代表阳离子,以N代表阴离子,则各离子晶体的组成表达式完全正确的组合是( )
A.①MN ②MN2 ③MN3 ④MN4 B.①MN ②MN2 ③MN2 ④MN
C.①MN2 ②MN2 ③MN2 ④MN D.①MN ②MN ③MN2 ④MN2
30. 钡在氧气中燃烧时得到一种钡的氧化物晶体, 结构如图所示,有关说法不正确的是( )
A.该晶体属于离子晶体
B.与每个Ba2+距离相等且最近的Ba2+共有12个
C.该晶体晶胞结构与NaCl相似
D.晶体的化学式为Ba2O2
第II部分(非选择题 共60分)
三、非选择题(本题包括4小题,共60分,请考生注意题目序号,在答题框中选择正确题号进行填涂并划线作答,选做题涂错做错均不得分。)
32.(请考生在答题卡上 31/32 题选做框内填涂 32题题号并划线作答,涂错做错均不得分,本题 15 分)
金属镍在电池、合金、催化剂等方面应用广泛。
(1)下列关于金属及金属键的说法正确的是________。
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是________。
(3) CO与N2结构相似,CO分子内σ键与π键个数之比为________。
(4)甲醛(H2CO)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内C原子的杂化方式为________。
(5)甲醇分子内的O—C—H键角________(填“大于”、“等于”或“小于”)甲醛分子内的O—C—H键角。
34.(请考生在答题卡上 33/34 题选做框内填涂 34题题号并划线作答,涂错做
错均不得分,本题 15 分)
M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为__________。
(2)元素Y的含氧酸中,酸性最强的是____________(写化学式)。
(3)与元素Y同周期元素中,第一电离能最大的是______(写元素符号)
(4)M与Y形成的一种化合物的立方晶胞如图所示。该化合物的化学式为_______。
(5)M与Y形成的另一种化合物易溶于氨水,在空气中呈深蓝色,深蓝色溶液中阳离子的化学式为__________。
36.(请考生在答题卡上 35/36 题选做框内填涂 36题题号并划线作答,涂错做
错均不得分,本题 15 分)
分子式为Pt(NH3)2Cl2的配位化合物有顺铂和反铂两种同分异构体。顺铂的结构简式为,具有抗癌作用;反铂的结构简式为,无抗癌作用。
请回答下列问题:
(1)C、N、O三种元素的电负性由大到小的顺序是________。
(2) Ni元素与Pt元素位于同一族,写出Ni元素基态原子的电子排布式:__________。
(3)顺铂和反铂的物理性质有很大差异,其中只有一种易溶于水,请你通过所学知识判断哪一种易溶于水,并说明理由: 。
(4)金属铂的原子堆积方式为铜型(面心立方堆积),一个金属铂的晶胞中含有__________个铂原子。
(5)NH3还能与很多化合物通过配位键发生相互作用。例如:科学家潜心研究的一种可作储氢材料的化合物X是NH3与第2周期中的另一种元素的氢化物相互作用的产物,X是乙烷的等电子体;加热化合物X会缓慢释放H2,转变为化合物Y,Y是乙烯的等电子体。则化合物X的结构式为__________(必须标明配位键)。
38.(请考生在答题卡上 37/38 题选做框内填涂 38题题号并划线作答,涂错做
错均不得分,本题 15 分)
氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应
可以得到BF3和BN,如下图所示:
请回答下列问题:
(1) BN中B元素的化合价为____________。
(2) 在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________________。
(3)由B2O3制备BF3的化学方程式是________________________________。
(4)BF3和过量NaF作用可生成NaBF4,BF的立体构型为__________________。
(5)六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。立方氮化硼的密度是_______________g·cm-3(只要求列算式,不必计算出数值。阿伏加德罗常数为NA)。
参考答案
一、选择题(本题包括20小题,每小题2分,共40分)
1-5 DAABB 6-10 DCCDA 21-25 CDBCD 26-30 BBBBD
二、非选择题(本题包括4小题,共60分) 各题叙述合理酌情给分。
32. (每空3分,共15 分)
(1)b (2)C(碳) (3)1∶2 (4)sp3 (5)小于
34. (每空3分,共15 分)
(1)金属晶体(2)HClO4 (3)Ar (4)CuCl (5) [Cu(NH3)4]2+
36. (每空3分,共15 分)
(1)O>N>C (写O、N、C顺序正确给2分) (2)1s22s22p63s23p63d84s2
(3) 顺铂易溶于水,因为它是极性分子,易溶于极性溶剂。 (4)4
(5)
38. (每空3分,共15 分)
(1)+3 (2)(极性)共价键 (皆给3分)
(3)
(物质错漏不给分,配平1分,加热1分,箭头不扣分)
(4)正四面体
(5)(结果正确,形式可异3分。分子项未×4给1分)








