

所属成套资源:2020王后雄猜题卷
【化学】河北省雄安新区博奥高级中学2019-2020学年高二上学期开学考试
展开
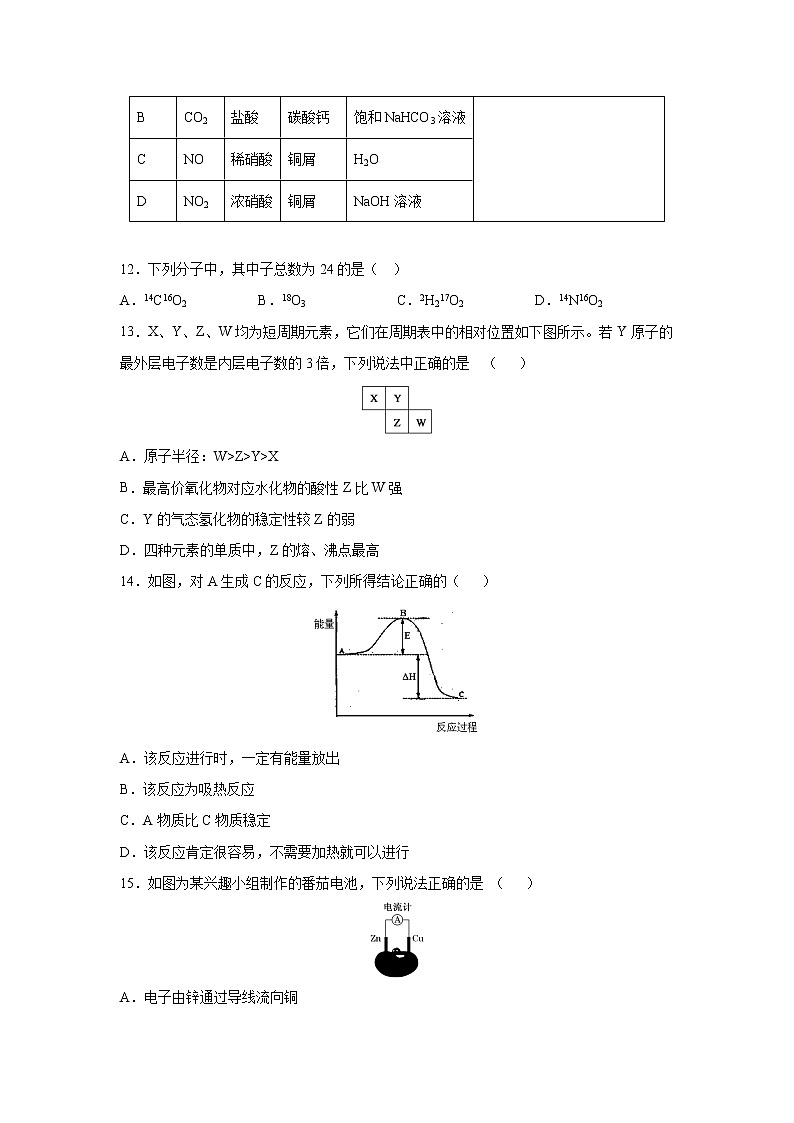
河北省雄安新区博奥高级中学2019-2020学年高二上学期开学考试一、单选题(本部分为选择题,每题3分)1.下列化合物依次属于氧化物、碱、盐的一组是( )A.Na2CO3、KOH、CaOB.CO、NaOH、KClC.H2O、H2SO4、NaClD.CuO、Cu2(OH)2CO3、CaCO32.下列关于摩尔质量的描述或应用正确的是( )A.1mol OH-的质量是17B.二氧化碳的摩尔质量是44 gC.铁原子的摩尔质量等于它的相对原子质量D.一个钠原子的质量约等于g3.现有三组溶液:①含有水分的植物油中除去水分;②回收碘的CCl4溶液中的CCl4;③用食用酒精浸泡中草药提取其中的有效成分。分离以上各混合液的正确方法依次是( )A.分液、萃取、蒸馏 B.萃取、蒸馏、分液C.分液、蒸馏、萃取 D.蒸馏、萃取、分液4.某无色透明溶液,在酸性环境下能大量共存的离子组是( )A.Na+、SO42-、HCO3-、C1-B.Mg2+、Cl-、Na+、NO3-C.K+、MnO4-、NO3-、Fe2+D.Cu2+、Cl-、NH4+、SO42-5.已知Na2S2O3(S的价态为+2价)可与氯气发生如下反应:4C12 +Na2S2O3 +5H2O= 2NaCl + 2H2SO4 + 6HCl,有关该反应的叙述正确的是( )A.Cl2在该反应中被还原B.H2SO4是还原产物C.反应中硫元素的化合价降低D.反应中H2O被氧化6.常温下,在溶液中可发生以下反应:①2Fe2++Br2=2Fe3++2Br-,②2Br-+Cl2=Br2+2Cl-,③2Fe3++2I-=2Fe2++I2。由此判断下列说法正确的是( )A.铁元素在反应①和③中均被氧化B.反应②中当有1 mol Cl2被还原时,有2 mol Br-被氧化C.氧化性强弱顺序:Cl2>Br2>I2> Fe3+D.还原性强弱顺序:I-> Br->Fe2+>Cl-7.24mL浓度为0.05mol·L-1的Na2SO3溶液恰好与20mL浓度为0.02mol·L-1的K2Cr2O7溶液完全反应。已知亚硫酸钠被氧化为硫酸钠,则铬元素在还原产物中的化合价为( )A.+3价 B.+4价 C.+5价 D.+6价8.为了验证NaHCO3固体中是否含有Na2CO3,下列实验及判断中,正确的( )A.加热,观察是否有气体放出B.溶于水后加BaCl2,看有无沉淀C.溶于水后加石灰水,看有无沉淀D.取固体试样加盐酸,看是否有气泡产生9.对于反应:2Na2O2 + 2H2O === 4NaOH + O2,下列说法中正确的是 ( )A.Na2O2是氧化剂,H2O是还原剂B.Na2O2既是氧化剂,又是还原剂C.该反应中电子转移的数目为4e-D.O2既是氧化产物,又是还原产物10.检验 SO2 气体中是否混有 CO2 气体,可采用的方法是( )A.通过品红溶液B.通过澄清石灰水C.先通过足量酸性 KMnO4 溶液,再通过澄清石灰水D.先通过 NaOH 溶液,再通过澄清石灰水11.下图中a、b、c表示相应仪器中加入的试剂,可用如图装置制取、净化、收集的气体是( )编号气体abcANH3浓氨水生石灰碱石灰BCO2盐酸碳酸钙饱和NaHCO3溶液CNO稀硝酸铜屑H2ODNO2浓硝酸铜屑NaOH溶液 12.下列分子中,其中子总数为24的是( )A.14C16O2 B.18O3 C.2H217O2 D.14N16O213.X、Y、Z、W均为短周期元素,它们在周期表中的相对位置如下图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法中正确的是 ( )A.原子半径:W>Z>Y>XB.最高价氧化物对应水化物的酸性Z比W强C.Y的气态氢化物的稳定性较Z的弱D.四种元素的单质中,Z的熔、沸点最高14.如图,对A生成C的反应,下列所得结论正确的( )A.该反应进行时,一定有能量放出B.该反应为吸热反应C.A物质比C物质稳定D.该反应肯定很容易,不需要加热就可以进行15.如图为某兴趣小组制作的番茄电池,下列说法正确的是 ( )A.电子由锌通过导线流向铜B.该装置将电能转化为化学能C.锌电极发生还原反应D.铜电极发生氧化反应16.将纯锌片和纯铜片按如图所示方式插入同浓度的稀硫酸中,以下叙述正确的是( )A.两烧杯中铜片表面均无气泡产生B.甲中铜片是正极,乙中铜片是负极C.甲、乙中SO42-都向铜片移动D.产生气泡的速率甲中比乙中快17.乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说法不正确的是( )A.和金属钠反应时键①断裂B.在铜催化共热下与O2反应时断裂①和③键C.在铜催化共热下与O2反应时断裂①和⑤键D.在空气中完全燃烧时断裂①②③④⑤键18.莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是( )A.分子式为C7H6O5B.分子中含有2种官能团C.可发生加成和取代反应D.在水溶液中羟基和羧基均能电离出氢离子19.下列关于苯的叙述正确的是( )A.反应①常温下不能进行B.反应②不发生,但是仍有分层现象,紫色层在上层C.反应③为取代反应,加热方式为酒精灯直接加热D.反应④能发生,生成的产物其二氯代物有4种二、非选择题20(14分)在25 ℃、101 kPa的条件下,断裂1 mol H—H键吸收436 kJ能量,断裂1 mol Cl—Cl键吸收243 kJ能量,形成1 mol H—Cl键放出431 kJ能量。H2+Cl2==2HCl的化学反应可用下图表示:请回答下列有关问题:(1)反应物断键吸收的总能量为____________________。(2)生成物成键放出的总能量为____________________。(3)判断H2+Cl2==2HCl反应________(填“吸收”或“放出”)能量。(4)反应物的总能量________(填“>”、“=”或“<”)生成物的总能量。三、综合题21(16分)I.某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据分析得:(8分钟时A为0.2mol 、B为0.5mol)(1)该反应的化学方程式为_________________________。(2)反应开始时至4min时,A的平均反应速率为________。(3)4min时,反应是否达平衡状态?________(填“是”或“否”), 8min时,V正________V逆(填“>” “<”或“=”)。II.在2L密闭容器中,800℃时反应2NO(g)+O2(g) →2NO2(g)体系中,n(NO)随时间的变化如表:时间/s012345n(NO)/mol0.0200.0100.0080.0070.0070.007 (1)上述反应________(填“是”或“不是”)可逆反应。(2)如图所示,表示NO2变化曲线的是________。(3)能说明该反应已达到平衡状态的是________(填序号)。a. v(NO2)=2v(O2) b.容器内压强保持不变c. v逆(NO)=2v正(O2) d. 容器内密度保持不变四、实验题22(13)实验室配制欲配置480mL4.0 mol·L-1的NaOH溶液。根据配置溶液的具体过程回答下列问题:(1)配制该溶液应选用______________mL容量瓶。 (2)用托盘天平称取_____________g固体NaOH。 (3)将称好的NaOH固体放至500mL的大烧杯中,倒入蒸馏水,用玻璃棒搅拌至完全溶解。待冷却至室温后,将烧杯中的溶液用玻璃棒引流转移至容量瓶。(4)用少量蒸馏水洗涤烧杯2-3次,并将每次洗涤的溶液都注入____________, 轻轻晃动容量瓶,使溶液混和均匀。 (5)向容量瓶中加入蒸馏水,直到液面离刻度线约1-2厘米时,改用________ 滴加蒸馏水至液面与刻度线相切。盖好瓶塞,摇匀。(6)配制好的溶液_____________(填“能”或“不能”)长期存放在容量瓶中。(7)以下因素会造成实验结果偏低的是____________A.定容时观察液面仰视 B.定容时观察液面俯视C.有少量NaOH溶液残留在烧杯中 D.容量瓶中原来有少量蒸馏水
【参考答案】1.B 2.D 3.C 4.B 5.A 6.B 7.A 8.B 9.B 10.C11.B 12.A 13.D 14.A 15.A 16.D 17.C 18.C 19.D20.(1)679 kJ (2)862 kJ (3)放出 (4)>21.2A⇌B 0.05mol·(L·min)-1 否 = 是 b bc 22.500 80 容量瓶 胶头滴管 不能 AC




