
所属成套资源:人教版初中化学中考重点专题训练
人教版初中化学中考重点专题5——金属活动性顺序的应用
展开
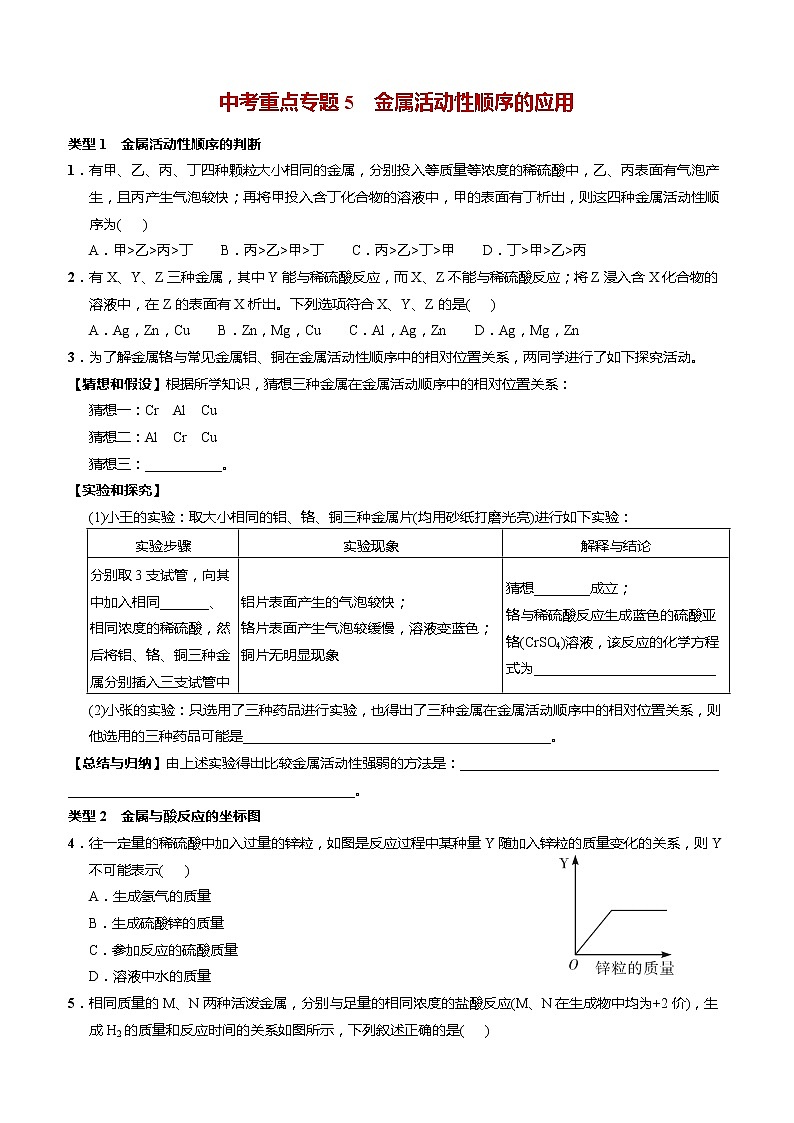
中考重点专题5 金属活动性顺序的应用类型1 金属活动性顺序的判断1.有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快;再将甲投入含丁化合物的溶液中,甲的表面有丁析出,则这四种金属活动性顺序为( )A.甲>乙>丙>丁 B.丙>乙>甲>丁 C.丙>乙>丁>甲 D.丁>甲>乙>丙2.有X、Y、Z三种金属,其中Y能与稀硫酸反应,而X、Z不能与稀硫酸反应;将Z浸入含X化合物的溶液中,在Z的表面有X析出。下列选项符合X、Y、Z的是( )A.Ag,Zn,Cu B.Zn,Mg,Cu C.Al,Ag,Zn D.Ag,Mg,Zn3.为了解金属铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,两同学进行了如下探究活动。【猜想和假设】根据所学知识,猜想三种金属在金属活动顺序中的相对位置关系:猜想一:Cr Al Cu猜想二:Al Cr Cu猜想三:___________。【实验和探究】(1)小王的实验:取大小相同的铝、铬、铜三种金属片(均用砂纸打磨光亮)进行如下实验:实验步骤实验现象解释与结论分别取3支试管,向其中加入相同_______、相同浓度的稀硫酸,然后将铝、铬、铜三种金属分别插入三支试管中铝片表面产生的气泡较快;铬片表面产生气泡较缓慢,溶液变蓝色;铜片无明显现象猜想________成立;铬与稀硫酸反应生成蓝色的硫酸亚铬(CrSO4)溶液,该反应的化学方程式为__________________________(2)小张的实验:只选用了三种药品进行实验,也得出了三种金属在金属活动顺序中的相对位置关系,则他选用的三种药品可能是____________________________________________。【总结与归纳】由上述实验得出比较金属活动性强弱的方法是:______________________________________________________________________________。类型2 金属与酸反应的坐标图4.往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量Y随加入锌粒的质量变化的关系,则Y不可能表示( )A.生成氢气的质量B.生成硫酸锌的质量C.参加反应的硫酸质量D.溶液中水的质量5.相同质量的M、N两种活泼金属,分别与足量的相同浓度的盐酸反应(M、N在生成物中均为+2价),生成H2的质量和反应时间的关系如图所示,下列叙述正确的是( )A.相对原子质量N>MB.两个反应生成H2的质量相等C.金属的活泼性N>MD.两个反应消耗盐酸的质量一定相等6.如图所示的四个图象与对应实验相符的是( )A.等质量的Mg和Zn中加入等质量、等浓度且过量的稀硫酸B.等质量且足量的Mg和Zn中加入等质量、等浓度的稀硫酸C.等质量且足量的Mg和Zn中加入等质量、等浓度的稀硫酸D.等质量的Mg和Zn中加入等质量、等浓度且过量的稀硫酸7.下列图象分别与选项中的操作相对应,其中不合理的是( )A.甲:向等质量、等浓度的稀H2SO4中分别加入足量的Zn粉和Fe粉B.乙:向一定量石灰石中加入过量的稀盐酸C.丙:向一定量CuCl2溶液中加入AlD.丁:向装有一定量Fe粉的试管中滴加CuSO4溶液类型3 金属与某化合物溶液反应后,滤液、滤渣成分的判断8.某化学小组向一定量AgNO3和Cu(NO3)2混合溶液中加入一定量的Zn粉,充分反应后过滤得溶液A和固体B,滤液A中所含的物质不可能的情况是( )A.Zn(NO3)2、AgNO3 B.Zn(NO3)2、Cu(NO3)2、AgNO3C.Zn(NO3)2、Cu(NO3)2 D.Zn(NO3)29.在CuCl2和ZnCl2的混合溶液中加入铁粉,充分反应后过滤,所得滤渣与盐酸反应放出气体。则所得滤液中含有的物质是( )A.CuCl2 ZnCl2 FeCl2 B.只有FeCl2 C.FeCl2 ZnCl2 D.CuCl2 ZnCl210.同学们到实验室去进行“探究金属的性质”实验。将锌粉和铁粉的混合物加入到盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,得到滤渣和滤液。请你填空:(1)若将所得滤渣放入稀盐酸中,有气泡产生,则:①滤液里一定含有__________(填写化学式,下同),可能含有__________;②滤渣中一定含有__________,可能含有__________。(2)若反应后所得滤液呈无色,则滤渣中一定含有__________(填写化学式)。类型4 金属的分离和有关物质的回收11.填写下列表格(“混合物”栏中括号内为杂质)。混合物除杂质的化学方程式主要操作步骤铜粉(Fe) FeCl2溶液(CuCl2) 12.某工厂欲从只含有CuSO4的废液中回收金属铜,并得到工业原料硫酸亚铁,其工业流程如图:(1)操作a的名称是________。(2)加入过量A的目的是_________________。(3)写出流程中有关反应的化学方程式:________________________;__________________________。
参考答案1.B 2.A3.Al Cu Cr(1)质量 二 Cr+H2SO4==CrSO4+H2↑(2)Al、CrSO4溶液、Cu[或Cr、Al2(SO4)3溶液、CuSO4溶液]通过金属与酸反应比较(或通过金属与金属化合物溶液反应比较,其他合理答案也可)4.D 5.A 6.C 7.D8.A 9.C10.(1)①Zn(NO3)2 Fe(NO3)2 ②Ag、Fe Zn(2)Ag、Fe11.Fe+2HCl===FeCl2+H2↑ 加盐酸至不再产生气泡,过滤,洗涤,干燥Fe+CuCl2===FeCl2+Cu 加过量铁粉,反应完全后过滤12.(1)过滤(2)使CuSO4全部反应(3)Fe+CuSO4===FeSO4+Cu Fe+H2SO4===FeSO4+H2↑





