




化学人教版课题4 化学式与化合价教课内容课件ppt
展开1、能根据物质的组成书写化学式,能描述化学式的意义。 2、能根据化学式对物质进行命名。 3、能根据名称书写化学式。
◆试写出下列物质的符号(1)氧气 ,氮气 ,氢气 ,红磷 ,(2)二氧化硫 ,水 , 四氧化三铁 ,过氧化氢 。
这些物质的符号由什么组成的?
用元素符号和数字的组合
来表示物质组成的式子。
①任何物质都有化学式吗?
②同种物质可以有不同的化学式吗?
③化学式可以任意的书写吗?
只有纯净物有化学式 ,混合物没有化学式;
◆下列物质中属于纯净物的是 。 A.蒸馏水 B.清洁的空气 C.冰水混合物 D.铜丝 E.二氧化硫 F.海水 G.五氧化二磷 H.氯化钠
A. C. D. E. G. H.
一种纯净物只能用一个化学式来表示
◆指出下列符号的意义: (1)H: 。 (2)Fe: 。 (3)2H: 。
粒子(分子、原子、离子)符号前面的数字,只表示粒子(分子、原子、离子)的个数。
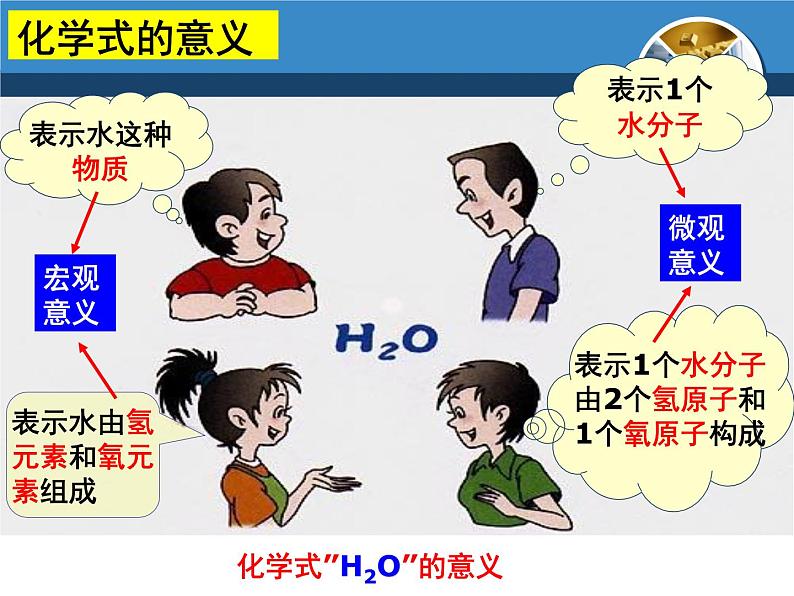
化学式”H2O”的意义
表示水由氢元素和氧元素组成
表示1个水分子由2个氢原子和1个氧原子构成
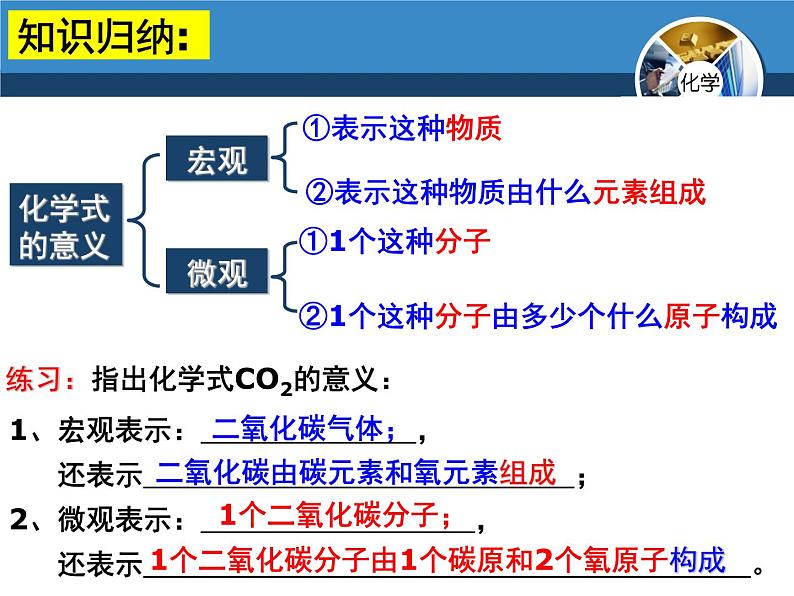
②表示这种物质由什么元素组成
②1个这种分子由多少个什么原子构成
练习:指出化学式CO2的意义:
1、宏观表示: , 还表示 ;2、微观表示: , 还表示 。
二氧化碳由碳元素和氧元素组成
1个二氧化碳分子由1个碳原和2个氧原子构成
(1)N2: ; ; ; 。 (2)SO2: ; ; ; 。
1个氮分子由2个氮原子构成
二氧化硫由硫元素和氧元素组成
1个二氧化硫分子由1个硫原子和2个氧原子构成
◆指出下列化学式的意义:
◆指出下列符号所表示的意义:
H: ; (2) 2H: ;(3) H2: ;(4) 2H2 : ;(5) H+ : ; (6) 2H+: 。
1个氢分子由2个氢原子构成;
化学符号中数字的意义:
1、符号前面的数字:2、符号右下角的数字:
H 2H 2H2 2H+ H2
表示1个分子中原子的个数
表示微粒(分子、原子、离子)的个数。
表示1个分子中原子的个数。
1个水分子中含有2个氢原子
◆指出下列数字“2”所表示的意义:
2H: ; (2) 2H+: ;(3) H2: ;(4) 2H2 : 前面的“2” ; 后面的“2” 。
1个氢分子含有2个氢原子
说出下列符号各具什么意义?
1个氧分子由2个氧原子构成
◆写出下列物质的化学式:
氯化钠 ;氯化钾 ;高锰酸钾 ; 五氧化二磷 ;二氧化碳 ;水 ;氮气 ;氦气 ;红磷 ;汞 。
1、由金属和非金属组成的物质:
氧元素在右,另一种元素在左
金属在左,非金属在右。
3、当某组成元素原子个数是”1”时,1可省略。
1、由原子构成的物质:
直接用元素符号表示该物质。
2、由多个原子构成的物质:
在元素符号右下角标出原子个数。
、O2、H2、O3、P4等
由4个磷原子构成的磷分子
◆读出下列物质的名称:
NaCl KCl P2O5 Fe3O4
2、由2种元素组成的物质读作:
●非金属氧化物中,氧原子数为1时,数字“1”要读出来;
●金属氧化物中,氧原子数为1时,省略不读。
N2O MgO
4、含有OH(氢氧根)的物质,读作:
NaOH KOH Ca(OH)2 Al(OH)3
5、含有SO4(硫酸根)的物质,读作:
CuSO4 K2SO4 CaSO4 Na2SO4
6、含有CO3(碳酸根)的物质,读作:
Na2CO3 K2CO3 CaCO3 CuCO3
7、含有NO3(硝酸根)的物质,读作:
NaNO3 KNO3 Ca(NO3)2 Cu(NO3)2
8、有些物质的化学式要读它的俗称:
H2O NH3
MgO CuO CO2 SO2 Fe3O4 P2O5 MnO2
氧在右,另一种元素在左
金属和非金属元素组成的物质
1、保持氢气化学性质的粒子是: A、H B、H2O C、H2 D、2H2、下列符号只有微观意义的是: A、Cl2 B、2N2 C、Cu D、CO23、地壳中,含量最多的金属与非金属形成的化合物的化学式: A、CaO B、SiO2 C、Fe2O3 D、Al2O3
4、“H2SO4”含“1”“2”“3”“4”的意义,叙述不正确的是 A、“1”表示每个硫酸分子中含1个硫原子 B、“2”表示硫酸中含有一个氢气分子 C、“3”表示硫酸由三种元素组成 D、“4”表示每个硫酸分子中含有4个氧原子
5、请写出下列物质的化学式或名称(1)铜丝 ;二氧化碳 ;五氧化二磷 ; 2个氯分子 ;4个汞原子 ;3个氧离子 ; 每个硫化氢分子中含有1个硫原子和2个氢原子 ;(2)NaCl ;KBr ;CaCl2 ; ClO2 ;Al2O3 ;SiO2 ; CaO ;ZnS ;
找 主 语
6、请写出下列符号表示的意义(1)N ; (2)2N ;(3) 2SO2 ;(4) N2 ;
1、记住一些常见元素和根的化合价,初步学会应用 化合价推求化学式,根据化学式推算化合价。2、知道相对分子质量的概念,初步学会利用相对原 子质量、相对分子质量进行物质组成的简单计算。3、能看懂某些商品标签上标示的物质成分及其含量。
◆写出下列物质的化学式 氯化钾 ; 水 ; 二氧化碳 ;
通常元素之间相互化合时,各元素的原子数目是一定的。
◆观察上述物质组成元素的原子个数比
化合价的成因及表示形式
元素符号正上方的正数或负数。
常见元素和根的化合价的规律及应用
1、金属和非金属化合时,
请计算出下列化合物中元素的正负化合价之和,你发现什么规律?
正价 + 负价 = 0
判断化学式是否正确的唯一标准!
例题:(15年天河一模)我省境内有许多温泉,经检测分析,该温泉属于硅酸盐温泉,对心脏、高血压等有良好的医疗保健作用。已知硅酸盐中硅元素的化合价为+4价,则硅酸的化学式为 A.H2SiO3 B.H4SiO3 C.H2SiO4 D.H3SiO3
3、一些元素有可变化合价:
在不同物质中可显不同的化合价。
如何读出下列物质的化学式?
遇到“破铜烂铁”要小心
例题:写出下列物质的名称(Cl为-1价,O为-2价)
先标出已知化合价,再计算未知的化合价。
请写出下列物质的化学式。
氧化铁 ; 氧化亚铁 。
根据名称写化学式步骤:
(金属在左,非金属在右)
作为一个整体参加反应的一些原子集团。
氢氧根 硝酸根 硫酸根 碳酸根 铵根
试求下列原子团中硫元素和氮元素的化合价。
正价 + 负价 = 根的化合价
常见元素和根的化合价的规律
4、单质中元素的化合价为0。
化合价是元素原子在形成化合物时表现出来的性质。
请标出出下列物质的化合价。
1价:K、Na、Cl、H、Ag2价:O、 S 、Ca、Ba、Mg、Zn3Al、4Si、5价P1、2 Cu; 2、3 Fe;-1氢氧硝酸根;-2硫酸碳酸根只有铵根是+1
1、写出下列物质的名称。
;
;
;
K Cl H Cl O4 Cl2 K Cl O3
2、写出下列物质氯元素的化合价。
先要标出已知元素的化合价
[ ]
3、写出下列物质的化学式。
氢氧化钾氢氧化钙氢氧化铁
化合价与离子所带电荷的关系
◆你发现化合价与离子所带电荷数之间的关系了吗?
1、离子所带电荷数与化合价在数值上完全相同,但数字和符号位置对调。
2、化合价在符号正上方,离子符号在符号右上角。
化合价与离子符号表示方法的区别
“+”“-”和数字整体的位置
“+”“-”和数字的相对位置
写在元素符号的正上方
写在元素符号的右上角
“+”“-”在前数字在后
“+”“-”在后数字在前
3、元素显正几价,则元素的离子带几个单位正电荷;元素显负几价,则元素的离子带几个单位负电荷。
氢离子: 钡离子:钙离子: 银离子:铁离子: 亚铁离子:锌离子: 按根根离子:
练习:写出下列离子符号
表示镁元素的化合价为+2
表示每个镁离子带两个单位的正电荷
化合价与离子符号表示意义的区别
(数字在前,符号在后)
(符号在前,数字在后)
AgCl2 Na CO3 CuSO4 K2O Mg NO3 K2SO4 Ba OH Na O2
◆判断下列化学式的书写是否正确,并改正。
判断化学式是否正确的唯一标准:
AgCl Na CO3 CuSO4 K2O Mg NO3 K2SO4 Ba OH Na O
根据化学式的计算
1、化学式相对分子质量的计算;
2、化学式中各元素的质量比;
3、化学式中元素的质量分数计算;
4、计算物质中某元素的质量;
求“NH4HCO3”的相对分子质量(式量)
解:NH4HCO3的式量
各个原子相对原子质量的总和
化学式相对分子质量的计算
【可能用到的原子质量:C-12; N-14;O-16;H-1】
氢氧化钙【Ca(OH)2】
( )
若化学式中出现带括号的原子团时,要先将括号中的原子团计算出来,再进行运算。
【可能用到的原子质量: 】
S:32 Ca:40 Cl:35.5 O:16 H:1
N2NH4NO3(NH4)2SO4 C6H12O6
14 × 2 = 28
14 + 1×4 + 14 + 16×3 = 80
练习:计算下列物质的相对分子质量
【可能用到的原子质量:C:12 H:1 O:16 N:14 S:32 】
(14 + 1×4) ×2 + 32 + 16×4 = 132
12×6 + 1 ×12 + 16 × 6= 180
1×m+32 +16× (2n+1)
2N2 3CO 2 2Ca(OH) 2
(12 + 16 ×2 )
[40 +(16 + 1) ×2 ]
【例1】计算二氧化硫(化学式为SO2)中硫元素和氧元素的质量比是: 。
化学式中各元素质量比的计算
【例2】蛋白质是机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应,生成氨基酸,蛋氨酸(化学式为C5H11O2NS)就是其中的一种。求蛋氨酸中各元素的质量比是: 。
解:mC:mH:mO:mN:mS
=60 : 11 : 32 : 14 : 32
mc:mH:mO:mN:mS=
60 : 11 : 32 : 14 : 32
前面没有“指名道姓”,后面要“后缀”
练习:求CO(NH2)2(尿素)中各元素的质量比?
【注意】: 若化学式中有括号,计算原子总数时,应乘以括号外的数。
解:mC:mO:mN:mH
(14 ) :
=3 : 4 : 7 : 1
【可能用到的原子质量:C:12 H:1 O:16 N:14】
H2O CO2NH4NO3
(1× 2) : 16 =
12 :(16 × 2) =
(14×2): (1×4): (16×3)
mN : mH : mO =
= 7 : 1 : 12
练习:计算下列物质中各元素的质量比。
【例1】Fe2O3中氧元素的质量分数各为多少?
化学式中元素的质量分数的计算
【可能用到的原子质量:C:12 H:1 O:16 N:14 Fe:56 】
所有原子的相对原子质量
练习: 计算化肥尿素CO(NH2)2中氮元素的质量分数?
( )
计算结果保留1位小数!
【可能用到的原子质量:C:12 H:1 O:16 N:14 】
60千克NH4NO3中含氮元素多少千克?
计算百分比数据时,不要直接算出来,列分式并约分更科学。
物质中某元素的质量的计算
设氮元素的质量为X,则有:
同分式分子、分母可同时约分,不同分式的分子和分子、分母和分母可同时约分!
先约分,后对角线相乘。
18g水中含有多少克氢元素?
千万别直接计算出结果!否则产生小数。
直接用分式的形式比较好!
多少千克CO2中含13.2千克碳元素?
设X千克CO2中含13.2千克碳元素,则有:
多少千克CO中含有的碳元素与13.2千克CO2中含有的碳元素相等?
解:设有X千克CO,根据题意有:
解:设相对分子量为R,则有:
计算时,要把百分比数写成分数的形式,使得计算更方便!
1、某物质的一个分子中含有2个N原子,此物质的氮元素质量分数为35%,求此物质的相对分子质量?
【可能用到的原子质量:N:14 】
2、蛋白质是机体生长及修补受损组织的主要原料,人体通过食物获得的蛋白质在胃肠中与水反应,生成氨基酸,蛋氨酸(化学式为C5H11O2NS)就是其中的一种。求蛋氨酸中N元素的质量分数?
3、合格奶粉每100克中含蛋白质约18克,蛋白质中氮元素的平均质量分数为16%,则每100克合格奶粉中含N元素的质量为 克;现测定某奶粉每100克中含有氮元素的质量为0.5克。则这种奶粉属于 产品(填“合格”或“不合格”)。
4、现有硫(S)、氧(O)、氢(H)、铁(Fe)四种元素,按表内题设要求把有关的化学式和相对分子质量填入空格中。
5、(1)计算氮肥NH4NO3中氮元素的质量分数。 (2)若测得某种NH4HCO3的含氮量为18%,判断该物质是否纯净?
(2)NH4HCO3中N%=
因为17.7%<18%, 所以该物质不纯净
6、某化合物的化学式为RO2 ,其中氧元素的质量分数为50%,求R的相对原子质量并确定R为何元素?
1.下列符号中能正确表示+3价铝元素的是 ( ) A、Al B、Al C、3Al D、Al2.下列化学式中,书写错误的是 ( ) A、氧化钙(OCa) B、氧化镁(MgO) C、三氯化铁(FeCl3) D、三氧化硫(SO3)3.化学式Fe2O3的读法是 ( ) A、铁二氧三 B、二铁化三氧 C、三氧化二铁 D、二氧化二铁 E、氧化铁
4.Mg(OH)2相对分子质量的计算式为 ( ) A、24+16+1×2 B、24×(16+1)×2 C、24×16+1×2 D、24+(16+1)×25.2H2O相对分子质量的计算式为 ( ) A、2+1×2+16 B、2×1×2×16 C、2 ×(1×2+16) D、2×1×2+16 6.H2SO4的相对分子质量为 ,在H2SO4中氢、硫、 氧三种元素的质量是 。氢、硫、氧三种元 素的原子个数比是 。
【可能用到的原子质量:H:1 O:16 N:14 S:32 Mg:24 】
7.用数字和化学式表示出:(1)五个氧分子 (2)2个水分子 (3)4个硫酸根离子 (4)10个氢氧化钠分子 8.下列化学符号表示两个氢分子的是 ( ) A、2H B、H2 C、2H2 D、H2O
化学九年级上册课题4 化学式与化合价授课ppt课件: 这是一份化学九年级上册课题4 化学式与化合价授课ppt课件,共60页。PPT课件主要包含了宏观意义,微观意义,动动脑,知识巩固,7Fe,化合价的运用,化合价的应用,相对原子质量的总和等内容,欢迎下载使用。
九年级上册课题4 化学式与化合价教课课件ppt: 这是一份九年级上册课题4 化学式与化合价教课课件ppt,共60页。PPT课件主要包含了化学式,化学式知识概况,H2O,化学式的意义,四化学式的读法,化合价,简介化合价的发展史,表示方法,化合价的发展史,原子的核外电子排布等内容,欢迎下载使用。
化学九年级上册第四单元 自然界的水课题4 化学式与化合价课堂教学课件ppt: 这是一份化学九年级上册第四单元 自然界的水课题4 化学式与化合价课堂教学课件ppt,共19页。PPT课件主要包含了教材分析,教材的地位和作用,教材内容的地位和作用,利用化合价推求化学式,教学重点,教学难点,学情分析,教学方法,教法学法,敢思会思等内容,欢迎下载使用。













