






初中化学人教版九年级下册第九单元 溶液课题2 溶解度教案配套课件ppt
展开教学目标1. 了解饱和溶液的含义。2. 能举例说明结晶现象。3. 了解溶解度的含义。4. 初步学习绘制和分析溶解度曲线,体验数据处理的过程,学习数据处理的方法。5. 通过实验探究培养学生对实验现象的观察、分析和推理归纳能力。
实验9-5 在室温下,向盛有20 mL水的烧杯中加入5 g 氯化钠,搅拌;等溶解后,再加 5 g 氯化钠,搅拌,观察现象。然后再加入15 mL水,搅拌,观察现象。
20 mL水能完全溶解5 g 氯化钠
烧杯中溶液底部有未溶解的固体
20 mL水不能完全溶解10 g 氯化钠
增加溶剂的量,可将未溶物质溶解
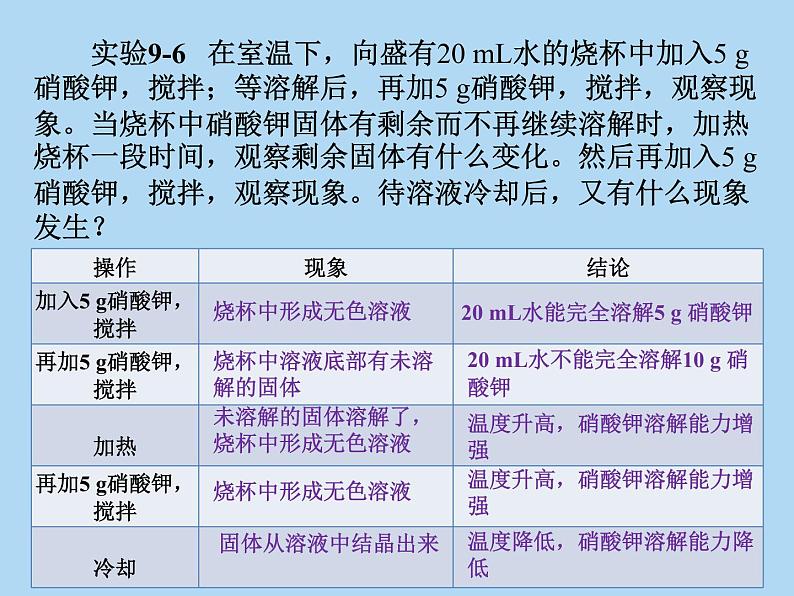
实验9-6 在室温下,向盛有20 mL水的烧杯中加入5 g硝酸钾,搅拌;等溶解后,再加5 g硝酸钾,搅拌,观察现象。当烧杯中硝酸钾固体有剩余而不再继续溶解时,加热烧杯一段时间,观察剩余固体有什么变化。然后再加入5 g 硝酸钾,搅拌,观察现象。待溶液冷却后,又有什么现象发生?
未溶解的固体溶解了,烧杯中形成无色溶液
20 mL水能完全溶解5 g 硝酸钾
20 mL水不能完全溶解10 g 硝酸钾
温度升高,硝酸钾溶解能力增强
温度降低,硝酸钾溶解能力降低
在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做这种溶质的饱和溶液;还能继续溶解的溶液,叫做这种溶质的不饱和溶液。 在实验9-5 中,当氯化钠能继续溶解时,溶液是不饱和的;当氯化钠固体不能继续溶解而有剩余时,溶液就变成了饱和的。当再加入水,剩余的氯化钠固体继续溶解,溶液又从饱和变成不饱和。 在实验9-6 中,第二次加入的硝酸钾不能全部溶解,但加热烧杯时,剩余的硝酸钾固体继续溶解,且再次加入的硝酸钾能全部溶解。这说明,当温度升高时,室温下的硝酸钾饱和溶液变成了较高温度下的不饱和溶液,因而能继续溶解硝酸钾。
上述实验说明,在增加溶剂或升高温度的情况下,饱和溶液可以变成不饱和溶液。因此,只有指明“在一定量溶剂里”和“在一定温度下”,溶液的“饱和”和“不饱和”才有确定的意义。 在实验9-6 中还可以看到,当热的硝酸钾溶液冷却以后,烧杯底部出现了固体。这是因为在冷却过程中,硝酸钾不饱和溶液变成了饱和溶液;温度继续降低,过多的硝酸钾会从溶液中以晶体的形式析出,这一过程叫做结晶(如下图)。
冷却热的饱和溶液时,硝酸钾晶体从溶液中析出
讨论 你知道用海水晒盐吗?上网查阅资料,了解用海水晒盐的过程,与同学交流。
海水晒盐是通过蒸发减少溶剂的量,使海水由不饱和溶液变成饱和溶液,然后使粗盐结晶析出。
除了冷却热的饱和溶液的方法以外,蒸发溶剂也是一种获得晶体的常用方法。例如,用海水晒盐,就是利用涨潮将海水引入贮水池,待海水澄清后,先引入蒸发池,经过风吹和日晒使水分部分蒸发;到一定程度后再引入到结晶池中,继续风吹和日晒,海水就会慢慢成为食盐的饱和溶液;再晒,食盐晶体就会逐渐从海水中析出,得到粗盐,同时得到含有大量化工原料的母液(叫做苦卤)。其大致过程如下:
综上所述,在一般情况下,不饱和溶液与饱和溶液之间的转化关系及结晶的方法可以表示如下:
通过上述实验,我们大致可以得出以下结论:在室温下,20 mL 水中所能溶解的氯化钠或硝酸钾的质量都有一个最大值,这个最大质量就是形成它的饱和溶液时所能溶解的质量。这说明,在一定温度下,在一定量溶剂里溶质的溶解量是有一定限度的。化学上用溶解度表示这种溶解的限度。
固体的溶解度表示在一定温度下,某固态物质在100 g 溶剂里达到饱和状态时所溶解的质量。如果不指明溶剂,通常所说的溶解度是指物质在水里的溶解度。例如,在20℃时,100 g 水里最多能溶解36 g 氯化钠(这时溶液达到饱和状态),我们就说在20℃时,氯化钠在水里的溶解度是36 g。
用实验的方法可以测出物质在不同温度时的溶解度,如下表。
1. 用纵坐标表示溶解度,横坐标表示温度,根据上表所提供的数据,在下图的坐标纸上绘制几种物质的溶解度随温度变化的曲线——溶解度曲线。 2. 从绘制的溶解度曲线上,查出上述几种物质在25℃和85 ℃时的溶解度。
几种固体物质的溶解度曲线
3. 以上二图 给出了几种固体物质的溶解度曲线。请与你所绘制的溶解度曲线进行比较,并讨论: (1)根据以上二图分析,这些固体物质的溶解度随温度的变化有什么规律?举例说明。 (2)从溶解度曲线中,你还能获得哪些信息? (3)溶解度数据表(如上表)和溶解度曲线都可以表示物质在不同温度时的溶解度,二者有什么区别?通过溶解度数据表和溶解度曲线所提供的不同信息,你能否由此体会到:不同的数据处理方法,作用不同。与同学交流。
利用溶解度曲线,我们可以查出某物质在不同温度时的溶解度;可以比较不同物质在同一温度时溶解度的大小;可以比较不同物质的溶解度受温度变化影响的大小;可以看出物质的溶解度随温度变化的规律;等等。
从以上二图可以看出,多数固体物质的溶解度随温度的升高而增大,如硝酸钾、氯化铵等;少数固体物质的溶解度受温度变化的影响很小,如氯化钠;极少数固体物质的溶解度随温度的升高而减小,如氢氧化钙。
由于称量气体的质量比较困难,所以气体的溶解度常用体积来表示。通常用的气体的溶解度,是指该气体的压强为101 kPa和一定温度时,在 1 体积水里溶解达到饱和状态时的气体体积。如氮气的压强为 101 kPa和温度为0 ℃时,1体积水里最多能溶解0.024体积的氮气,则在0 ℃时,氮气的溶解度为0.024。
讨论 1. 打开汽水(或某些含有二氧化碳气体的饮料)瓶盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关? 2. 喝了汽水以后,常常会打嗝。这说明气体的溶解度还与什么有关?
汽水中含有大量二氧化碳
如何增加养鱼池水中的含氧量
海水、河水或湖水中,都溶解了一定量的氧气,但养鱼池中常常由于鱼多而缺氧, 因此要设法增加水中的氧气含量。最常见的办法是在鱼池中设立几个水泵,把水喷向空中(或把水搅动起来),这样,可以增大空气与水的接触面积,增加水中氧气的溶解量。你见过类似的事例吗?在寒冷的冬季,北方养鱼池的冰面上总要打很多洞,你知道这是为什么吗?如果用鱼缸养鱼,又如何增加水中的含氧量呢?
在干净的玻璃杯中加入约20 mL开水,然后加入白糖,用筷子搅拌,直到有少量白糖不再溶解为止。将一根细线的一端浸入白糖溶液中,另一端留在玻璃杯外,用硬纸片盖住玻璃杯(防止灰尘进入溶液),静置。过4~5天或更长时间,拿掉硬纸片,观察溶液表面、玻璃杯壁和细线上白糖晶体的生成。
60 ℃时,100 g水中最多溶解110 g硝酸钾。或60 ℃时,100 g水中溶解110 g硝酸钾恰好达到饱和
初中化学人教版九年级下册第九单元 溶液课题2 溶解度示范课课件ppt: 这是一份初中化学人教版九年级下册第九单元 溶液课题2 溶解度示范课课件ppt,共24页。PPT课件主要包含了一饱和溶液,实验探究,想一想,溶液是否饱和的判断,概念上,外观上,饱和溶液,不饱和溶液,蒸发结晶,二溶解度等内容,欢迎下载使用。
人教版九年级下册第九单元 溶液课题2 溶解度授课ppt课件: 这是一份人教版九年级下册第九单元 溶液课题2 溶解度授课ppt课件,共60页。PPT课件主要包含了归纳总结一,归纳总结二,归纳总结三,归纳总结四,溶解度第一课时,溶解度,应该在同一温度下,这样行吗,应该溶剂的量相同,应该达到饱和状态等内容,欢迎下载使用。
初中人教版课题2 溶解度背景图课件ppt: 这是一份初中人教版课题2 溶解度背景图课件ppt,共37页。PPT课件主要包含了饱和溶液,浓溶液与稀溶液,不一定,注结晶的方法,蒸发结晶蒸发溶剂,贮水池,蒸发池,结晶池,氯化钠,多种化工原料等内容,欢迎下载使用。













