





初中化学课题2 溶解度教课内容ppt课件
展开一.饱和溶液与不饱和溶液
在 ,向 里加入某种溶质,当溶质不能继续溶解时所得到的溶液叫做饱和溶液
1、什么叫饱和溶液、不饱和溶液
在 ,向 里加入某种溶质,当溶质还能继续溶解时所得到的溶液叫做不饱和溶液
?如何判断一种溶液是否饱和呢?
一般地说,要确定某一溶液是否饱和,只要看在一定温度下,有没有不能继续溶解的剩余溶质存在。如有,且溶质的量不再减少,那么这种溶液就是饱和溶液。
2、饱和溶液与不饱和溶液的转化
在同量的溶液中,含溶质较多的溶液——浓溶液; 含溶质较少的溶液——稀溶液
不同的溶质:饱和溶液不一定是浓溶液, 不饱和溶液不一定 是稀溶液。相同溶质、相同温度:饱和溶液一定比不饱和溶液浓。
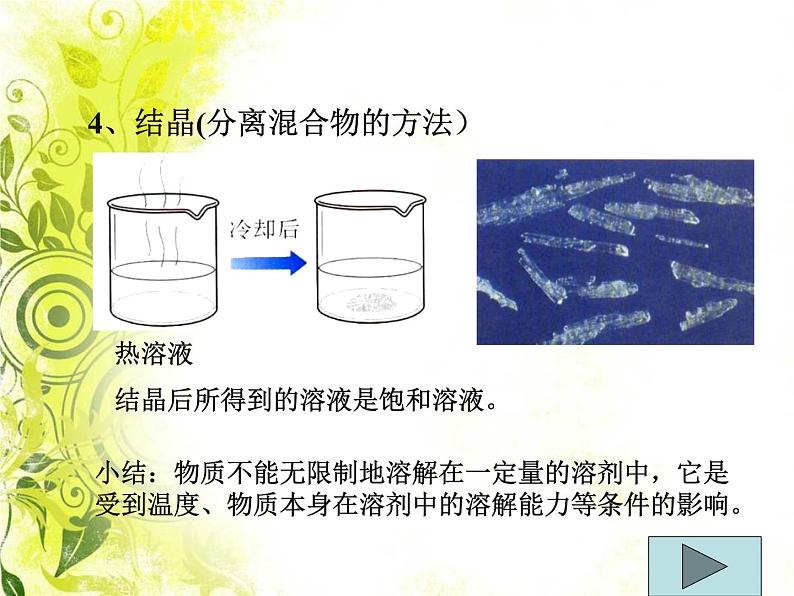
4、结晶(分离混合物的方法)
结晶后所得到的溶液是饱和溶液。
小结:物质不能无限制地溶解在一定量的溶剂中,它是受到温度、物质本身在溶剂中的溶解能力等条件的影响。
讨论:在上面的活动与探究中,用的水都是20mL,其中溶解氯化钠和硝酸钾的质量是否相同?
在同一条件下,(相同温度,一定量的水),它们在水中溶解的最多量接近相同,但是随着温度的上升,水中溶解的硝酸钾的质量比氯化钠的质量要大得多。
在 下,某固体物质在 里达到 状态时所溶解的的质量。
100g溶剂(一般指水)
讨论:200c时硝酸钾的溶解度为31.6g,这句话的含义
用纵坐标表示溶解度,用横坐标表示温度.
通过绘制、观察氯化钠溶解度曲线,你得到什么信息?
图9-12 几种固体物质溶解度曲线
1:同一物质在不同温度下 的溶解度不同(点)
5:曲线的交点表示这两 种物质在该温度下的 溶解度(相同)
4:曲线越陡,该物质的 溶解度受温度影响越大
找一找50度各物质的溶解度
3:查阅某物质在某一温度下的溶解度(点)
2:不同一物质在同一温度下 的溶解度不同(点)
6:曲线上的点,曲线上方的点,曲线下方的点表示的意义
图9-13 熟石灰的溶解度随温度升高而降低
1: 大多数固体物质的溶解度随温度升高而增大。
溶解度随温度变化的规律
2: 少数固体物质的溶解度受温度影响较小, 如NaCl
3: 极少数物质的溶解度随温度升高而减小, 如Ca(OH)2
1、加热盛饱和氢氧化钙溶液的试管,会看到 。
有白色固体析出/溶液变浑浊
3、右图分别表示A、B、C三种物质的溶解度曲线,则t20C时,其溶解度由大小的顺序是: A.A、B、C B. B、A、C C.B、C 、A D.C 、A、B
如图是A、B、C三种物质在水中的溶解度曲线,请回答:(1)M点的含义是_________________________ (2)当温度为t1 ℃,三种物质溶解度由小到大依次为_______,当温度为t3 ℃时,溶解度最大的是___;(3)C可能表示哪种物质: 。(4)从B溶液中得到晶体宜采用的方法是 。(5)除去A中混有的少量B的方法是 。
t2ºC时,A和C两种物质的溶解度相等
你发现溶解度曲线的线型有几种类型?
(6)当A、B、C三种物质的溶液接近饱和时,采用增加溶质、恒温蒸发溶剂、降低温度的方法均可以达到饱和的是 物质溶液。
气体在压强为101KPa和一定温度时溶解在1体积水里达到饱和状态时的气体体积。
如:在00C时,氮气的溶解度为0.024。
即:在101KPa和温度为00C时,1体积水里最多能溶解0.024体积氮气。
气体的溶解度与什么有关系呢?回答以下问题找出答案。
(1)打开汽水盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关?
(2)喝了汽水以后,常常会打嗝。这说明气体的溶解度还与什么有关?
气体的溶解度与温度、压强有关,温度越高,溶解度越小;压强越大溶解度越大。
下列关于硝酸钾的溶解度的说法,正确的是: A 200C时,20g硝酸钾溶解在100g水里,所以200C时硝酸钾的溶解度是20g。 B 200C时,20g硝酸钾溶解在水里制成饱和溶液,所以200C时硝酸钾的溶解度是20g。 C 把31.6g硝酸钾溶解在100g水里,形成饱和溶液,所以200C时硝酸钾的溶解度是31.6g。 D 200C时,31.6g硝酸钾溶解在100g水水里,形成饱和溶液,所以200C时硝酸钾的溶解度是31.6g。
硝酸钾在600C时的溶解度是110g,则此温度下配制得的饱和溶液中,溶质、溶剂、溶液三者间的质量比为____________________________________。
在200C时,氯化钾的溶解度是33g,则在200C时,100克水溶解氯化钾_______g可达到饱和。
溶质 溶剂 溶液
110g 100g 210g
剩余的氯化钠晶体继续溶解最后消失
20ml水能完全溶解5克氯化钠
20ml水不能完全溶解10克氯化钠
加水可使饱和的氯化钠溶液变不饱和
加入硝酸钾晶体完全溶解
改变条件时,饱和溶液与不饱和溶液可以互相转变。
1.1000C硝酸钾饱和溶液冷却至300C,滤去晶体后,所得溶液是________溶液(饱和、不饱和)。 2.把600C时的氯化铵饱和溶液冷却到100C,有氯化铵晶体析出,剩余溶液是: A.浓溶液 B.稀溶液 C.饱和溶液 D.不饱和溶液 3.200C时,要使硝酸钾不饱和溶液,变为饱和溶液,可采取下列措施中的: A.温度升高至600C B.加入硝酸钾 C.加入水 D.加入200C硝酸钾饱和溶液
4.某物质的溶解度随温度升高而增大。现有一瓶常温时该物质的饱和溶液,要使它变成不饱和溶液而又保持其溶剂的质量不变,可采用的方法是 。
5.室温时,在各盛有10ml水的两个小烧杯中,分别缓缓地加入氯化钠和硝酸钾的固体,边加入边搅拌,到烧杯里有剩余固体,不能再溶解为止。这个实验说明 。
在一定温度下物质不能无限制地溶解到一定量的溶剂中
6、A、B、C、D四个烧杯里分别盛有质量相等的同种溶剂,向四个烧杯加入某溶质,且固体溶质质量依次减少(温度相同),充分溶解,(如下图所示)回答下列各问(填序号)(1)_____________中盛的一定是饱和溶液;(2)_____________中盛的可能是饱和溶液;(3)_____________中盛的一定是不饱和溶液;
【基础巩固】1.用什么方法可以使接近饱和的硝酸钾溶液 变为饱和溶液?2.硝酸钾在60 ℃时的溶解度是110g,这说明在 ℃时, g 硝酸钾溶解在 g水中恰好形成饱好溶液。3.在提到某种物质的溶解度时,为什么要特别指明温度?答:溶解度与温度有关。不同温度下同一种物质的溶解度 不同。4.分析溶解度曲线,从中可以看出固体的溶解度与温度有 什么关系?答:大多数物质的溶解度随温度的升高而增大如KNO3 ; 少数物质的溶解度随温度的升高变化不大如NaCl; 极少数物质的溶解度随温度升高而减小如Ca(OH)2 。
5.为什么汗水带有咸味?被汗水浸湿的衣服晾干后,常出 现白色的斑迹,这是为什么?答:汗水中含有盐。水分蒸发后,盐留在衣服上形成白斑6.现有一瓶蒸馏水和一瓶氯化钾溶液,可用什么简单的办 法把它们鉴别开?答:用玻璃被各蘸液体少量于酒精灯上灼烧,无斑迹的是 蒸馏水,有斑迹的是氯化钾。7.加热冷水时,当温度尚未达到沸点时,为什么水中常有 气泡冒出?天气闷热时,鱼塘里的鱼为什么总是接近水 面游动?答:温度升高,气体的溶解度减小,溶解在水中的气体逸出; 水温升高、水中溶解的氧气减少,而水面与空气接触溶解的氧气多,所以--------。
8.氨在常温下是一种气体,它易溶于水,溶于水后就形成 氨水,当温度升高时氨又会逸出。氨水是一种常用的化 学肥料,平时贮存在氨水罐中。试设想在保存氨水时应 注意什么?答:放在阴凉处、密封保存在氨水罐中。9.下图是a、b两种固体物质的溶解度曲线。从图中你能得 到哪些信息?开放题
t ℃时,a、b两种物质的溶解度相等;小于t ℃时, a溶解度< b物质溶解度;大于t ℃时, a溶解度> b物质溶解度.
【能力提高】 1.10℃时硝酸钾的溶解度是20.9g,20℃时食盐的溶解度是25g,70℃时氯化铵的溶解度是60g,则( )A. 硝酸钾的溶解度最小 B. 食盐的溶解度的最大C. 氯化铵的溶解度最大 D. 无法比较溶解的的大小2.将60℃时的硝酸钾饱和溶液冷却到20℃,溶液中保持不变的是( )A. 溶质质量 B. 溶剂质量 C. 溶液质量 D. 质的溶解度
初中化学人教版九年级下册第九单元 溶液课题2 溶解度评课课件ppt: 这是一份初中化学人教版九年级下册第九单元 溶液课题2 溶解度评课课件ppt,共27页。PPT课件主要包含了活动探究,课堂练习,影响因素,想一想等内容,欢迎下载使用。
化学课题2 溶解度教课内容课件ppt: 这是一份化学课题2 溶解度教课内容课件ppt,共60页。PPT课件主要包含了溶剂水,实验2,固体溶解,固体有剩余,想一想,应该在同一温度下,溶剂量应该相同,应该达到饱和状态,固体溶解度的概念,饱和状态等内容,欢迎下载使用。
初中化学人教版九年级下册第九单元 溶液课题2 溶解度教学演示课件ppt: 这是一份初中化学人教版九年级下册第九单元 溶液课题2 溶解度教学演示课件ppt,共25页。PPT课件主要包含了混合物分离的方法,过滤法,应用粗盐提纯,①溶解,②过滤,③蒸发,④转移,玻璃棒转移,结晶法,1冷却热饱和溶液等内容,欢迎下载使用。













