



初中化学人教版九年级下册课题2 溶解度评课ppt课件
展开在一定的温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的质量,称为该物质在这种溶剂里的溶解度。
100g溶剂 (一般指水)
思考:如何比较不同物质在水中的溶解能力大小呢?
查一查:教材P36表9-1,给出了几种物质在不同温度时的溶解度,请大家查一查20 ℃时NaCl的溶解度。在20 ℃时,NaCl的溶解度为36.0 g。影响溶解度的因素:
20℃氯化钠的溶解度是36g,从中你能获取哪些信息?①20℃,100g水中最多能够溶解36g氯化钠;②20℃,100g水中溶解36g氯化钠,恰好形成饱和溶液
(1)20℃时,将36g氯化钠溶解在100g水中,所得的溶液是_____________。(2)20℃时从足量的氯化钠饱和溶液中蒸发掉100g水,析出氯化钠晶体的质量为_________。(3) 20℃的氯化钠饱和溶液中,溶液、水、溶质的质量比为_______________。
1、判断:20℃向100g水中加入40g氯化钠,得到氯化钠饱和溶液,则20℃时氯化钠溶解度是40g。
2、在20℃时,50g水中最多可溶解15.8g硝酸钾,则20℃时硝酸钾溶解度是____g。
3、30℃时硝酸钾的溶解度是45.8g,这句话的含义是什么?将其关系代入下表:
30℃时,100g水中最多能够溶解45.8g硝酸钾;30℃时,100g水中溶解45.8g硝酸钾,溶液达到饱和状态。
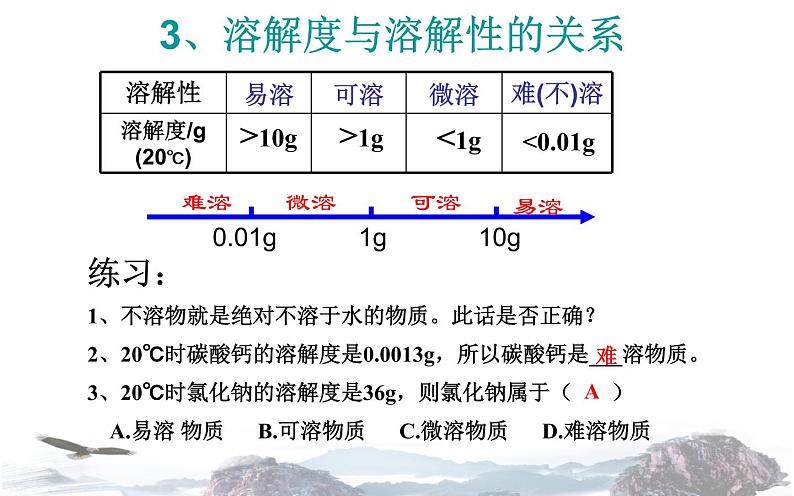
练习:1、不溶物就是绝对不溶于水的物质。此话是否正确?2、20℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是___溶物质。3、20℃时氯化钠的溶解度是36g,则氯化钠属于( ) A.易溶 物质 B.可溶物质 C.微溶物质 D.难溶物质
3、溶解度与溶解性的关系
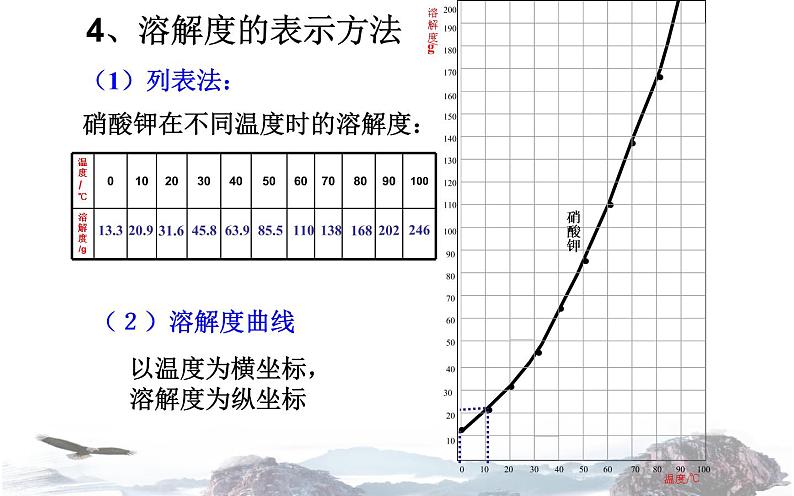
硝酸钾在不同温度时的溶解度:
以温度为横坐标,溶解度为纵坐标
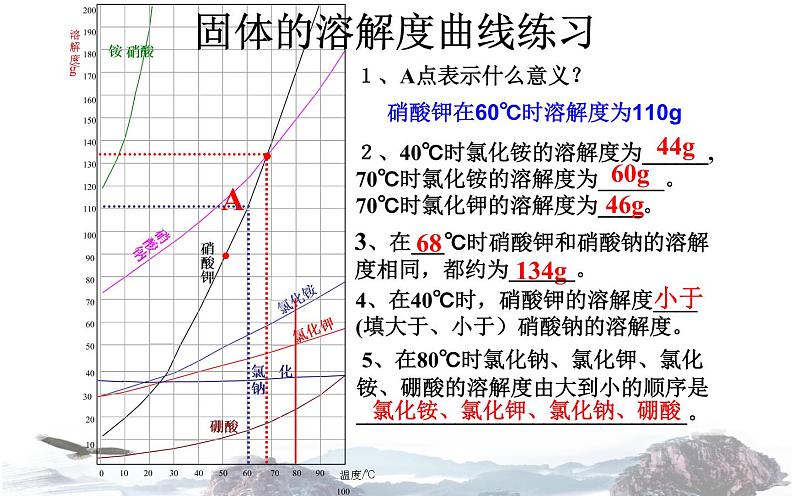
1、A点表示什么意义?
2、40℃时氯化铵的溶解度为______, 70℃时氯化铵的溶解度为______。 70℃时氯化钾的溶解度为____。
4、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。
3、在___℃时硝酸钾和硝酸钠的溶解度相同,都约为______。
氯化铵、氯化钾、氯化钠、硼酸
5、在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是______________________________。
硝酸钾在60℃时溶解度为110g
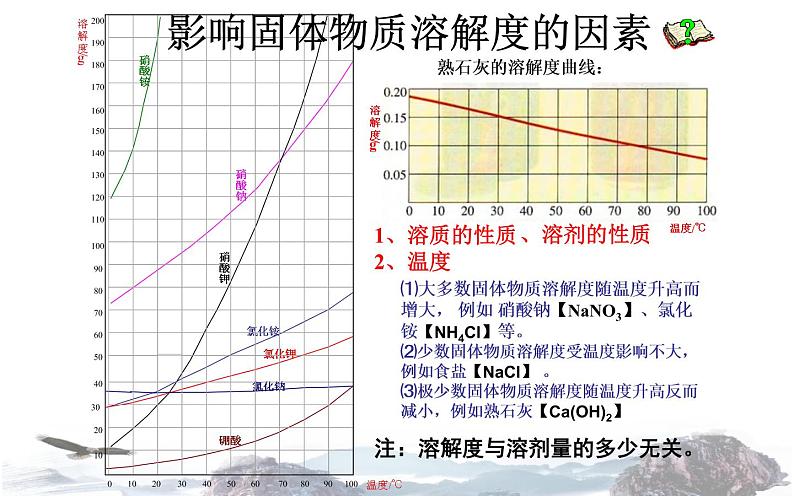
1、溶质的性质2、温度注:溶解度与溶剂量的多少无关。
⑴大多数固体物质溶解度随温度升高而增大, 例如 硝酸钠【NaNO3】、氯化铵【NH4Cl】等。 ⑵少数固体物质溶解度受温度影响不大,例如食盐【NaCl】 。⑶极少数固体物质溶解度随温度升高反而减小,例如熟石灰【Ca(OH)2】
影响固体物质溶解度的因素
1、表示溶解度随温度变化而变化的趋势;2、曲线上任一点表示该物质在该温度下的溶解度;3、交点表示几种物质在交点所示的温度下的溶解度相同;4、溶解度曲线下方的点表示的溶液是不饱和溶液。
1、甲、乙两种固体的溶解度曲线如右图所示。⑴ ℃时,甲和乙的溶解度相等;⑵40℃时,若将40g乙(不含结晶水)放入160g水中充分溶解,所得溶液的溶质质量与溶液质量之比 ,该溶液是 溶液(填“饱和”或“不饱和”);(3)40℃时,将甲、乙两物质的饱和溶液各100g降温至20℃,析出晶体(均不含结晶水)的质量关系是:m(甲) m(乙) (填“﹥”、“﹦”或“﹤”)。
1、定义:气体溶解度是指这种气体在压强为101KPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
0℃时,氧气的溶解度为0.049的含义是什么?
如氮气压强为101kPa和温度为0℃时,1体积水最多能溶解0. 024体积氮气,则在0℃时氮气的溶解度为0.024。
氧气在压强为101kPa和温度为0℃时,1体积水最多能溶解0. 049体积氧气
2、影响气体溶解度的因素
思考:1、天气闷热时,鱼儿为什么总爱在水面上进行呼吸?天气闷热,温度升高,氧气的溶解度减小;2、深海中CO2气体的溶解度为什么比海面要大?因为深海中的压强比海面大。
⑴气体溶解度一般随压强增大而增大,压强减小而减小。
⑵气体溶解度一般随温度升高而减小,温度降低而增大。
相同溶质在不同的溶 剂中的溶解能力不同
不同的溶质在相同溶 剂中的溶解能力不同
易溶 、可溶 、 微溶 、难(不)溶
影响因素(温度、压强)
1.右图为氯化钠、碳酸钠(俗称纯碱)在水中的溶解度曲线。(1)当温度为10℃时,碳酸钠的溶解度为 ;(2)当温度 时,氯化钠的溶解度大于碳酸钠的溶解度;(3)生活在盐湖附近的人们习惯“夏天晒盐,冬天捞碱”。请你解释原因: “夏天晒盐”“冬天捞碱”
氯化钠的溶解度受温度影响不大,夏天温度高水分蒸发快,氯化钠易结晶析出;碳酸钠的溶解度受温度影响大,冬天温度低,碳酸钠易结晶析出。
练习:⑴温度,温度越高,溶解速率越快;搅拌,搅拌能加快食盐的溶解;颗粒大小,食盐颗粒越小,溶解越快。⑵在两个烧杯中各放入50mL水,分别取2g颗粒大小相同的食盐,同时放进烧杯中,在一个烧杯中搅拌,观察记录两个烧杯中的食盐完全溶解所需要的时间。11、⑴加速固体物质的溶解;⑵NaOH,NaOH溶于水放热;⑶硝酸铵溶解吸热,使空气中的水蒸气凝结成水珠。
初中化学人教版九年级下册课题2 溶解度优秀教学课件ppt: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9866_t3/?tag_id=26" target="_blank">课题2 溶解度优秀教学课件ppt</a>,共23页。PPT课件主要包含了温度不同,溶剂量不同,固体溶解度,四要素,条件一定温度,状态饱和状态,单位g,概念的理解,刚好形成饱和溶液,溶解性与溶解度的关系等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度多媒体教学ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度多媒体教学ppt课件,共8页。PPT课件主要包含了课题二溶解度,固体的溶解度,快速计算溶解度,溶解度的表示方法,溶解度的相对大小等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度优秀课件ppt: 这是一份初中化学人教版九年级下册课题2 溶解度优秀课件ppt













