


化学人教版课题2 溶解度示范课课件ppt
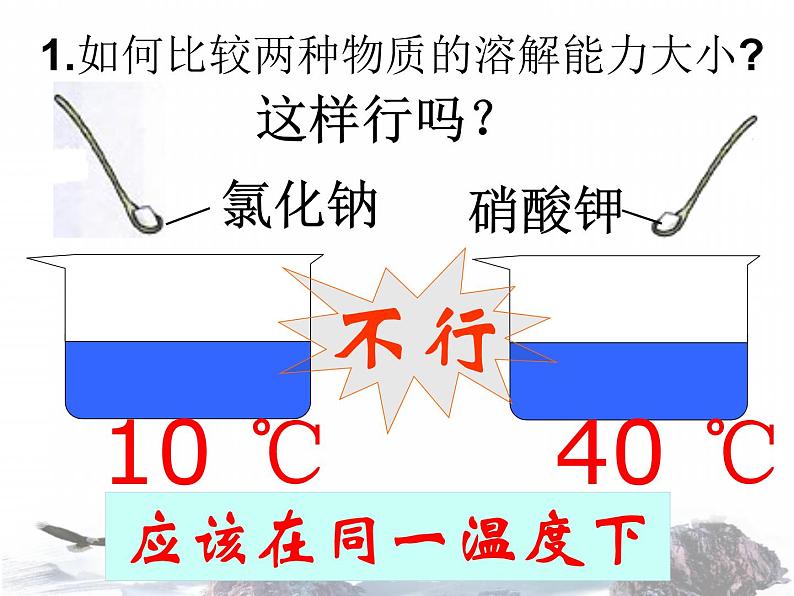
展开1.如何比较两种物质的溶解能力大小?
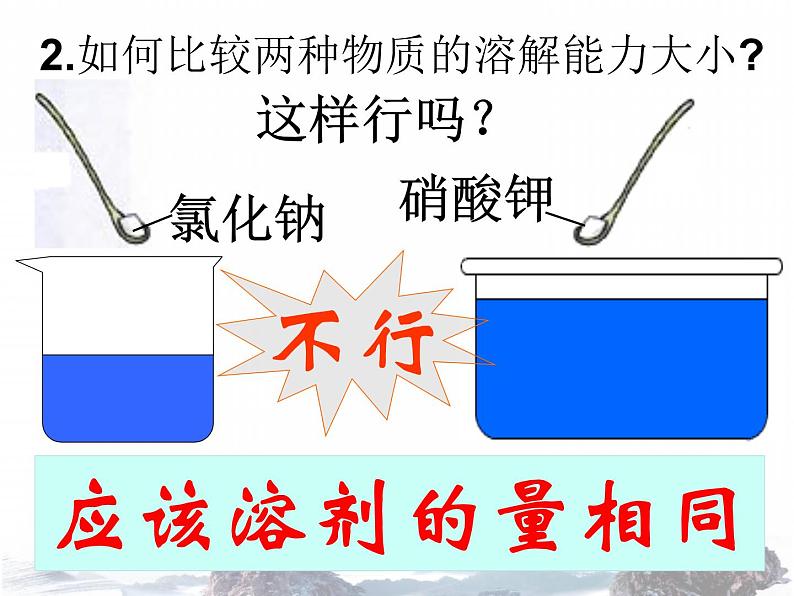
2.如何比较两种物质的溶解能力大小?
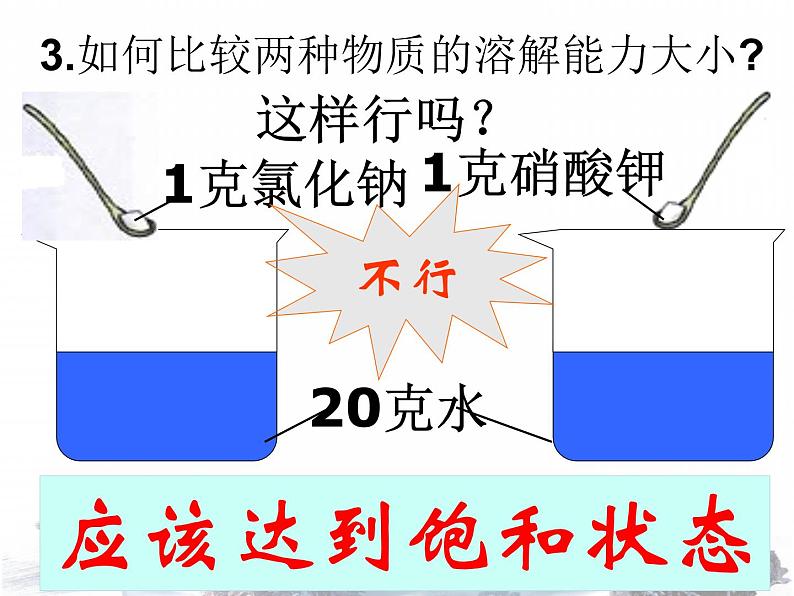
3.如何比较两种物质的溶解能力大小?
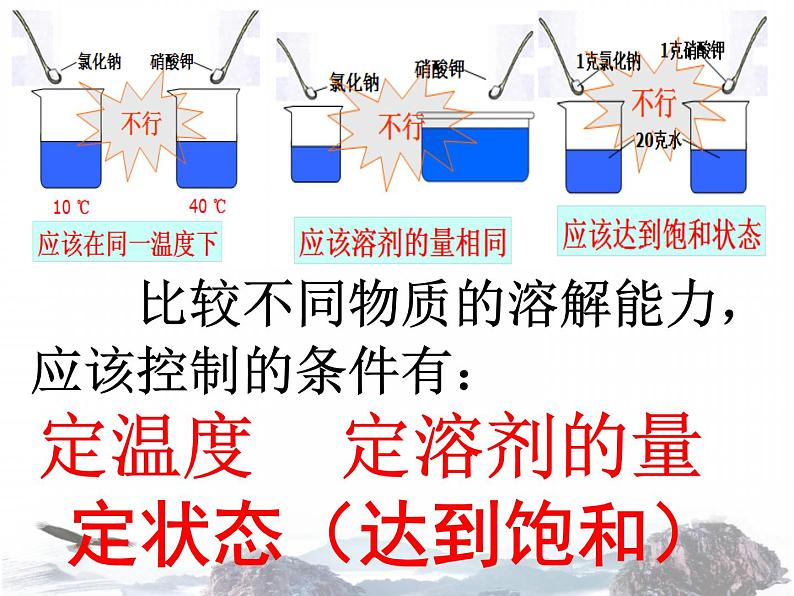
比较不同物质的溶解能力,应该控制的条件有:
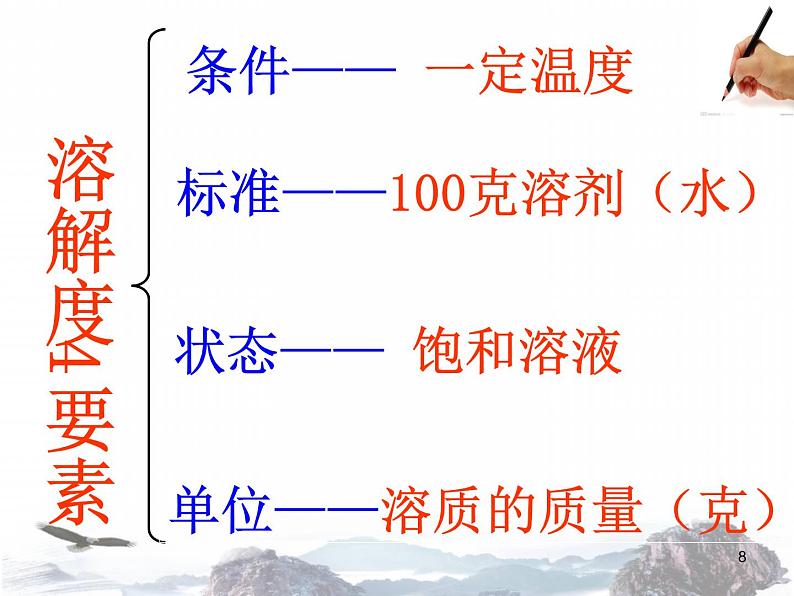
在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。
标准——100克溶剂(水)
单位——溶质的质量(克)
三.小 组 讨 论 1:
20℃时,氯化钠的溶解度是36g。
2.在20℃时,100g水中溶解36g氯化钠达到饱和;
1.在20℃时,100g水中最多能溶解氯化钠固体36.0g;
3.在20℃时, 36.0g氯化钠固体全部溶解至少需要100g水;
4.在20℃时, 从足量的氯化钠饱和溶液中蒸发掉100g水,能析出36.0g氯化钠晶体;
5.在20℃时,氯化钠的饱和溶液中水与溶质的质量比为100:36(或25:9)
6、在20℃时,将氯化钠与水以36:100的质量比混合,可得该温度下氯化钠的饱和溶液;
7.在20℃时,从氯化钠的饱和溶液中蒸发水与析出晶体的质量比为100:36(或25:9)
(1)50gA物质溶于100g水中刚好形成饱和溶液,则该物质溶解度为50g。( )
(2)20 ℃ 50gB物质溶于水中,刚好形成100g饱和溶液,则20 ℃时该物质溶解度为50g。 ( )
(3)20 ℃ 50gC物质溶于100g水中,形成150g溶液,则20 ℃时该物质溶解度为50g。 ( )
(4)20 ℃ 50gD物质溶于100g水中恰好形成饱和溶液,则20 ℃时该物质溶解度为50。 ( )
在20℃时,100g水中溶解36g氯化钠溶液达到饱和,则20℃时氯化钠溶解度是____。20 ℃时50g水中最多可溶解氯化钠___g,形成____g氯化钠溶液。
在40℃时,200g水中溶解80g氯化钾溶液达到饱和,则40℃时氯化钾的溶解度是____。40 ℃时将40g氯化钾加入50g水中,充分溶解后,形成了氯化钾的______(填“饱和”或“不饱和”)溶液___g 。
五.溶解度的表示方法:
A.几种固体物质在不同温度时的溶解度(克)
从表中你能得到哪些信息?
同一物质在不同温度的溶解度;不同物质在同一温度的溶解度。
缺点是:温度变化不连续
用纵坐标表示溶解度,用横坐标表示温度.
小组活动与探究( 36页)
1.用纵坐标表示溶解度,横坐标表示温度.根据表9—1所提供的数据,在图9—11的坐标纸上绘制几种物质的溶解度随温度变化的曲线—溶解度曲线。2.从绘制的溶解度曲线上,查出上述几种物质在25 ℃和85℃时的溶解度。
B.几种物质的溶解度曲线
点:曲线上的点均表示某物质在该温度下的溶解度。
两曲线交点:表示这两种物质在该温度下的溶解度相同。
曲线:曲线越陡,该物质的溶解度受温度影响越大。
大多数固体物质溶解度随温度升高而增大。例如硝酸钾、氯化铵等。
少数固体物质溶解度受温度影响不大。例如食盐。
极少数固体物质溶解度随温度升高反而减小。例如熟石灰。
讨论2:从这些溶解度曲线的走向和陡峭程度我们能获得哪些信息?
C.从溶解度曲线分析结晶情况
A、冷却热饱和溶液法(降温结晶法)
适用于溶解度随温度变化较小的物质如NaCl
适用于溶解度随温度变化较大的物质如KNO3
1、横坐标60,纵坐标110 的交点表示什么意义?2、40℃时氯化铵的溶解度为_____, 70℃时氯化铵的溶解度为______。 70℃时氯化钾的溶解度为____。3、在__℃时硝酸钾和硝酸钠的溶解度相同,都约为____。
六、巩固练一练:看课本P37图9-12,回答问题
4、在40℃时,硝酸钾的溶解度____ (填大于、小于)硝酸钠的溶解度。5、在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是
氯化铵、氯化钾、氯化钠、硼酸
1.从氯化钠和碳酸钠的溶解度表你获得的信息是:
, 。
NaCl的溶解度随温度变化较小
碳酸钠的溶解度随温度变化较大
2、如图,A、B是两种物质的溶解度曲线图,(1)A物质的溶解度曲线表明A物质的溶解度____________________(2)M点表示在____ºC时,A和B的溶解度_____,在_____时A物质的溶解度大于B物质的溶解度。在______时A物质的溶解度小于B物质的溶解度。
3. 右图是甲、乙两种物质的溶解度曲线,下列说法正确的是( ) A.甲的溶解度受温度影响比乙小 B.15℃时甲、乙的溶解度相等C.30℃时乙的溶解度为30g D.升高温度可使接近饱和的甲溶液变为饱和
4.上图是A.B.C三种固体物质的溶解度曲线,回答下列问题:(1)从B溶液中得到晶体宜采用的方法是(2)分离B与C混合物采用的方法是(3)除去A中混有的少量B的方法是
先溶解,再过滤,最后蒸发结晶
配成A的热饱和溶液,降温结晶,过滤
同学们,通过本节课的学习,你都学到了什么?
1.在一定温度下,某固态物质在100克溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里的溶解度。2.溶解度的表示法:列表法、溶解度曲线法3.物质的溶解度随温度的变化情况可用溶解度曲线来表示
学习目标3.知道影响气体溶解度的一些因素。会利用有关气体溶解度的知识解释身边的一些现象。
气体的溶解度与什么有关系呢?
(1)打开汽水盖时,汽水会自动喷出来。这说明气体在水中的溶解度与什么有关?
(2)喝了汽水以后,常常会打嗝。这说明气体的溶解度还与什么有关?
气体溶解度一般随压强增大而增大,随压强减小而减小气体溶解度一般随温度升高而减小,随温度降低而增大。
总结:气体溶解度的影响因素
请解释:天气闷热时,鱼儿为什么总爱在水面上进行呼吸?
知识点一、溶解度与饱和溶液
【典例1】t℃时,向10 g水中逐渐加入硝酸钾晶体至饱和,则此过程中该溶液满足下图a、b两个变量的变化关系的是( )A.a -溶解度,b-溶质质量 B.a -溶质的质量分数,b-溶质质量C.a -溶质质量,b-溶剂质量 D.a -溶解度,b-溶剂质量
4、加热饱和氢氧化钙溶液,会看到:________________________________;如果把二氧化碳气体通入澄清石灰水中,也会看到二者原理一样吗?
有白色固体析出/溶液变浑浊
3、某物质的溶解度随温度升高而增大。现有一瓶常温时该物质的饱和溶液,要使它变成不饱和溶液而又保持其溶剂的质量不变,可采用的方法是 。
不同,前者是物理变化,后者是化学变化
5、下图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )A.在t1℃时,三种物质的溶解度由大到小的顺序是甲>乙>丙B.在t2℃时,甲、乙两物质的溶解度相等 C.甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液D.当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙
6、根据下列几种物质溶解度曲线图,得到的结论正确的是( )
A.硝酸钾中混有少量氯化钠,采用蒸发结晶进行提纯 B.氢氧化钙饱和溶液降低温度后有晶体析出 C.80℃时,氯化钾与硫酸镁的溶解度相等 D.所有物质的溶解度均随温度的升高而增大或 随温度的降低而减小
7.甲、乙两种固体的溶解度曲线如下图。现将两试管分别装入甲、乙两种物质的饱和溶液(试管底部均有未溶解的固体),再放进盛有冰水的烧杯里, 则下列说法正确的是( ) A.甲溶液中溶质增大 B.乙溶液中剩余的固体减少 C.试管里甲、乙物质的溶解度都增大 D.试管里甲、乙两溶液中的溶质都减少
8.下图是A.B两种物质的溶解度曲线,试回答下列问题(1)t1ºC时,A 的溶解度 B 的溶解度.(填< > 或=)(2)当A、B两物质的溶液接近饱和时,采用增加溶质、蒸发溶剂、降低温度的方法可以达到饱和的是 物质的溶液?
1、将20℃的硝酸钾饱和溶液升温至80℃时,下列说法正确的是( ) A.溶液的浓度不变 B.溶液质量减少 C.溶液中溶质的溶解度减少D.溶液仍为饱和溶液
2.要使KNO3溶解度增大采用的方法( )A增加水 B增加KNO3 C不断振荡搅拌 D升高温度
3.25 ℃时50g水最多溶解5gA;60 ℃时,100g水最多溶解10gB,则比较A,B溶解度大小为( )
A.不能比较 B. A=B C. A>B D. A
5、将氯化钠和硝酸钾的混合物用结晶法分离,对于滤液(母液)来说,下列说法能够成立的是( )A.滤液中不含硝酸钾 B.滤液中不含氯化钠C.滤液是硝酸钾不饱和溶液 D.滤液是硝酸钾饱和溶液
(1)A点的意义是(2)t2时,1,2,3,4四种物质溶解度由大到小的顺序是(3)物质 的溶解度受温度影响最大,物质 的溶解度随温度的升高而增大,物质 的溶解度随温度的升高而减小。
t1℃时,物质1、 3的溶解度相等
8.在80℃时,将110g硝酸钾加入到100g水中,充分溶解后,形成的溶液为该温度下硝酸钾的____溶液。欲使其刚好形成饱和溶液,可采用的方法有:
若再降温到10℃,会怎样?
会析出89g硝酸钾晶体
9.在90℃时,将36g氯化钠加入到100g水中,充分溶解后,形成的溶液为该温度下氯化钠的______溶液。欲使其刚好形成饱和溶液,可采用的方法有:
若仅将题中“36g”换成“30g”,会怎样?
1.NaCl和KNO3在不同温度时的溶解度如下:
下列说法正确的是( )A.10℃时,将40g NaCl固体加入l00g水中,可得到l40gNaCl溶液B.KNO3和NaCl的溶解度受温度的影响都很大C.将30℃的KNO3饱和溶液升温至60℃,会变成不饱和溶液D.20℃时,NaCl饱和溶液的溶质质量分数为36%
2.在闷热的夏天,池塘里的鱼大多浮在水面上,导致这一现象发生的原因是( )A、夏天的鱼特别喜欢在水面上B、夏天水温高,鱼到水面上可以凉快一些C、夏天水温高,水中溶解的氧气少,鱼就浮在水面上D、夏天,水面上营养特别丰富,鱼就游到水面上
3.右图表示M、N两种固体物质的溶解度曲线,下列对图示信息的描述正确的是( )A.30℃时M的溶解度小于N的溶解度B.P点表示t℃时M、N的溶解度相等C.M、N都是难溶物质 D.阴影处各点对应的溶液(不包含曲线上的点)是M的不饱和溶液,N的饱和溶液
4.20℃时,碳酸氢钠的溶解度为9.7g,其含义是在20℃___________________ ;工业上用氨碱法制纯碱时,向饱和氨盐水中不断通入CO2,同时生成碳酸氢钠和氯化铵,但却只有碳酸氢钠结晶析出,原因是________________________ 。
100g水中最多溶解9.7g碳酸氢钠
相同温度下,氯化铵的溶解度比碳酸氢钠大
人教版九年级下册课题2 溶解度教课内容ppt课件: 这是一份人教版九年级下册课题2 溶解度教课内容ppt课件,共16页。PPT课件主要包含了试试身手,不饱和溶液,饱和溶液,①增加溶剂,②升高温度,①增加溶质,③蒸发溶剂,②降低温度,晶体的定义,结晶的方法等内容,欢迎下载使用。
初中化学人教版九年级下册课题2 溶解度评课ppt课件: 这是一份初中化学人教版九年级下册课题2 溶解度评课ppt课件,共16页。PPT课件主要包含了溶解度的表示方法,想一想等内容,欢迎下载使用。
初中人教版第九单元 溶液课题2 溶解度教学演示ppt课件: 这是一份初中人教版第九单元 溶液课题2 溶解度教学演示ppt课件,共16页。PPT课件主要包含了初识溶解度,不饱和溶液,饱和溶液,物质的溶解性,影响因素,溶质的质量,一定温度,饱和状态,克质量的单位g,记忆温饱百克等内容,欢迎下载使用。













