






人教版第九单元 溶液课题3 溶液的浓度评课ppt课件
展开
这是一份人教版第九单元 溶液课题3 溶液的浓度评课ppt课件,共25页。PPT课件主要包含了我们来观察,我们会分析,颜色越深浓度越大,一溶质的质量分数,溶质质量,溶液质量,溶质的质量分数,我们会观察,我们会应用,计算溶液的质量等内容,欢迎下载使用。
在两杯同样多的水中分别加入1匙、2匙蔗糖,完全溶解后,哪一杯更甜?哪一杯更浓?
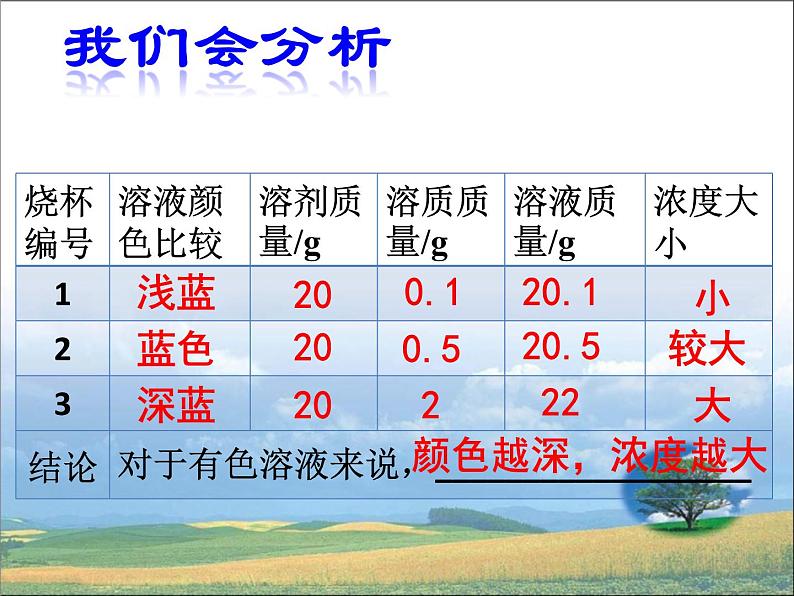
实验 9-7在室温下,向三个小烧杯中各加入20 mL水,然后分别加入0.1 g、0.5 g、2 g无水硫酸铜,振荡,使硫酸铜全部溶解,比较三种硫酸铜溶液的颜色。在这三种溶液中,哪种最浓?哪种溶液最稀?你判断的依据是什么?
溶液的浓与稀只能粗略地表明一定量的溶液里所含溶质的多少,但在实际应用中,常常要准确知道一定量溶液里含有溶质的质量。因此需要准确知道溶液的组成。那如何表明溶液的组成呢?
是_________和_________之比。
溶质的质量 =溶液质量 ×溶质质量分数
注意:①溶质的质量:被溶解的那部分质量,没有被溶解的那部分不能计入溶质质量和溶液质量。②溶液的质量 = 溶质的质量 + 溶剂的质量③溶质质量、溶剂质量、溶液质量的单位要统一。④溶质的质量分数用百分数表示。
固体全部溶解,形成无色溶液
两杯溶液都是无色透明,怎样比较溶液的稀浓?
例题1、在农业生产上,常需要用质量分数为16%的氯化钠溶液选种。现要配制150 kg这种溶液,需要氯化钠和水的质量各是多少?
二、有关溶质的质量分数的计算
1、计算所需溶质和溶剂的质量
解:溶质的质量分数= ×100%
溶质质量=溶液质量×溶质的质量分数 =150 kg×16% =24 kg
溶剂质量=溶液质量—溶质质量 =150 kg—24 kg =126 kg
答:配制150 kg质量分数为16%的氯化钠溶液需24 kg氯化钠和126 kg水。
例题2、现有12g硝酸钾,要配制成15%的硝酸钾溶液,①溶液质量是多少?②需要水的质量为多少?
溶质质量=溶液质量=溶剂质量=
溶液质量×溶质的质量分数溶质质量÷溶质的质量分数溶液质量-溶质质量
在实验里常常要用到稀硫酸和稀盐酸,通常用浓硫酸或浓盐酸来稀释。细心的同学会发现,浓硫酸和浓盐酸的质量分数相差很大。1、为什么浓硫酸的质量分数是98%,而浓盐酸的质量分数才36.5%?2、怎样将浓酸稀释为稀酸呢?
盐酸的最大浓度是36.5%,在大的话HCl就挥发了。98.3%的浓硫酸是常用的浓度。
浓酸具有强腐蚀性,所以要稀释为稀酸,增加使用酸的安全性。
一、溶解度与溶质的质量分数
在一定温度下的某物质的饱和溶液中
注意:1、适用范围:___________2、在一定温度下,饱和溶液的溶质质量分数_____3、固体的溶解度只与_____有关,所以饱和溶液的溶质质量分数只与______有关
例1:已知20℃时食盐的溶解度为36g,求20 ℃时食盐溶液的溶质质量分数最大是多少?
例题2(溶液的稀释:溶质的质量不变)化学实验室现有质量分数为98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把50 g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
解:设稀释后溶液的质量为x。 50 g×98%=x×20%
需要水的质量=245 g—50 g=195 g
答:要把50 g质量分数为98%的浓硫酸稀释为20%的硫酸,需要水195 g。
三、溶质质量分数应用于化学方程式的计算
例3:100g某硫酸溶液恰好与13g锌完全反应,试计算这种硫酸中溶质的质量分数。
分析:参加化学反应的是______,因此先根据化学方程式求参加化学反应的_______的质量。
一、配制一定溶质质量分数的溶液。
【实验探究】配制50g质量分数为6%的氯化钠溶液。步骤如下:
①计算:需要氯化钠的质量为___g,水的体积为____mL(水的密度近似看做1g/cm 3);
②称量:在托盘天平两边各放一张同样大小的滤纸,调节托盘天平平衡后,将游码拨到______处,最后添加氯化钠固体,直至天平平衡;
③量取:用量筒量取所需的水,倒入装有氯化钠固体的烧杯里;④溶解:用玻璃棒________,使氯化钠完全溶解。
⑤贮存:把配好的溶液装入 试剂瓶,盖好瓶塞,并贴上写有______和______________的标签,放到指定的地方,标签向________。
哪些因素可造成配制的溶质质量分数偏低?
(1) ______偏多了,可能是用了____视方法量取所需要的溶剂
(2) 天平没有调节平衡,且向____偏
(2)用已配好的质量分数为6%的氯化钠溶液(密度约为1.04g/cm 3),配制50g质量分数为3%的氯化钠溶液,需要量取6%的氯化钠溶液_____mL,水_____mL
相关课件
这是一份化学九年级下册课题3 溶液的浓度教课免费ppt课件,共49页。PPT课件主要包含了实验9-7,分析实验结论,溶质质量,溶液质量,100%,溶质质量分数,实验9-8,溶质质量溶剂质量,实验用品,实验步骤等内容,欢迎下载使用。
这是一份初中化学第九单元 溶液课题3 溶液的浓度课文内容ppt课件,共20页。PPT课件主要包含了教材核心练,溶质质量,溶液质量,基础达标练,巩固提升练等内容,欢迎下载使用。
这是一份初中化学人教版九年级下册课题3 溶液的浓度课堂教学课件ppt,共16页。PPT课件主要包含了溶质的质量分数,推导公式,观看演示实验,实验误差分析等内容,欢迎下载使用。









