




初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构授课ppt课件
展开1、初步了解核外电子是分层排布的。2、了解原子结构示意图的涵义。3、了解核外电子的排布特点与元素性质的关系。
1、核外电子是怎样绕原子核运动的?有规律吗?2、电子经常出现的区域,科学家们把它叫什么?3、电子在核外的排布有什么特点?4、原子结构示意图各部分的涵义是什么?
原子是怎样构成的?
核外电子是怎样绕原子核运动的呢?有规律吗?
电子不像行星绕太阳旋转有固定的轨道,但有经常出现的区域,科学家把这样的区域称为电子层。
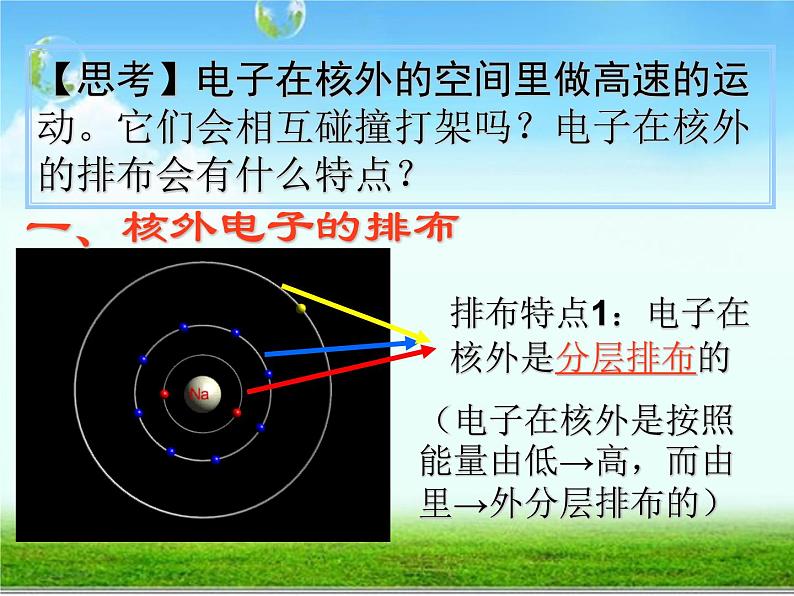
【思考】电子在核外的空间里做高速的运动。它们会相互碰撞打架吗?电子在核外的排布会有什么特点?
排布特点1:电子在核外是分层排布的
(电子在核外是按照能量由低→高,而由里→外分层排布的)
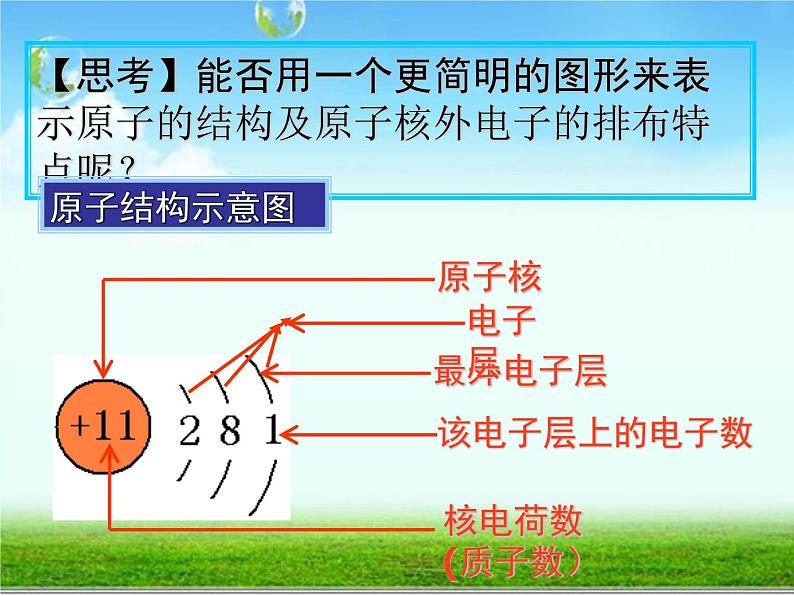
【思考】能否用一个更简明的图形来表示原子的结构及原子核外电子的排布特点呢?
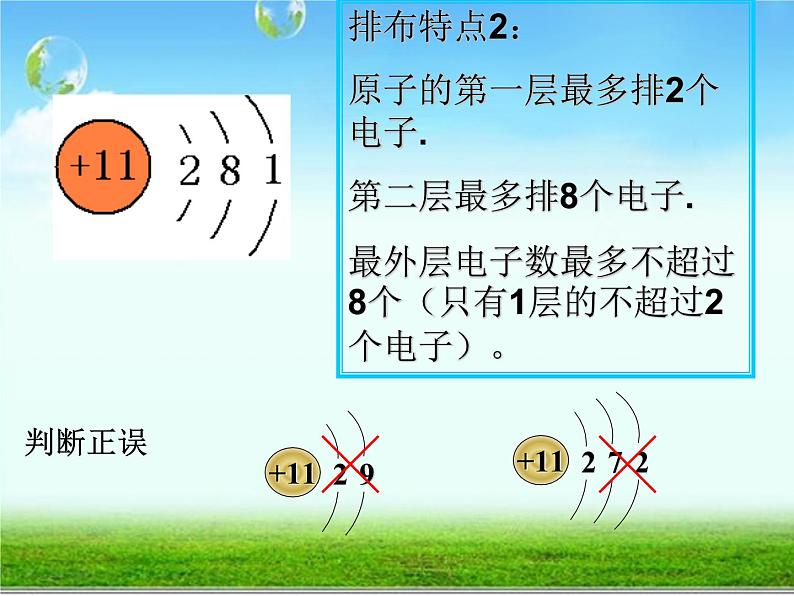
排布特点2: 原子的第一层最多排2个电子.第二层最多排8个电子.最外层电子数最多不超过8个(只有1层的不超过2个电子)。
写出下列元素的符号,画出其原子结构示意图。 硫(16 ) 镁(12) 氯(17) 氟(9)
1、原子结构在什么样的情况下属于相对稳定结构?2、稀有气体元素的原子、金属元素的原子、非金属元素的原子最外层电子各有什么特点?在化学反应中是易得到电子还是易失去电子?3、元素的化学性质主要与原子的什么有关?
【小知识】物质都有趋向于稳定状态的特点(如:水往低处流;树上的苹果往下掉)。
【稳定结构】像稀有气体元素原子这样的结构叫8电子稳定结构。
若只有一个电子层,则2电子也是稳定结构(如: He)。
原子也不例外,也有趋向于稳定结构的特点。那么,什么样的结构才是原子的稳定结构呢?
金属元素:最外层电子数<4个,易失去电子;达到稳定结构
【思考】分析下列原子核外电子排布有什么特点?
非金属元素:最外层电子数≥4个,易得到电子;达到稳定结构
稀有气体:最外层电子数等于8个(He2个)。(稳定结构)
归纳 :各元素原子最外电子数目的特点
最外层电子数决定了元素的化学性质。
最外层电子数决定了元素的化学性质
1、 决定元素的种类。是区分不同元素的依据。2、 决定着元素的化学性质。
1.离子:带电荷的原子或原子团叫做离子。
2.阴离子:带负电荷的原子叫做阴离子。如: O2- F- 阳离子:带正电荷的原子叫做阳离子。如: Na+Mg2+
3.离子符号的书写:电荷数标注在元素符号的右上角(先写数字后写“+”“-”号)。
4.离子所带电荷数由该元素原子的最外层电子数决定。
右上角的数字表示每个离子带多少个单位的电荷
Mg2+---每个镁离子带两个单位的正电荷
练习:说出下列符号中的数字的含义Al3+ O2- Zn2+
离子符号前加数字只表示离子的个数
3Ca2+ 表示三个钙离子
排布特点1:电子在核外是分层排布的。
排布特点2: 原子的第一层最多排2个电子,第二层最多排8个电子,最外层电子数最多不超过8个(只有1层的不超过2个电子)。
原子中:质子数=电子数(原子不带电)
阳离子中:质子数>电子数(带正电) 阴离子中:质子数<电子数(带负电)
原子和离子的联系和区别
1.属于原子结构示意图的是 、属于离子结构示意图的是 2.要能够根据示意图写出对应的符号
原子:核电荷数=核外电子数
离子:核电荷数≠核外电子数
2.判断下列原子结构示意图是否正确?
请写出下列示意图的名称
3.某离子带3个单位的正电荷,质子数为13,该离子的核外电子数为_____,该离子的名称是______,符号是____,该离子的结构示意图是:
4.下列五种微粒中最易失去电子的是 ,最易得到电子的是 , 属于同种元素的是————,原子化学性质相似的是————.。
A B C
D E
初中人教版课题2 原子的结构多媒体教学ppt课件: 这是一份初中人教版课题2 原子的结构多媒体教学ppt课件,共27页。PPT课件主要包含了原子的构成,α粒子束,交流共享,原子构成示意图,方便使用,钻石质量的计量,相对质量,◆表达式,◆符号,◆单位SI等内容,欢迎下载使用。
初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构教案配套ppt课件: 这是一份初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构教案配套ppt课件,共36页。PPT课件主要包含了原子的构成示意图,中子不带电,原子的构成,带正电,核电荷数,质子数,电子数,质子和中子,12Mx,原子结构规律等内容,欢迎下载使用。
九年级上册课题2 原子的结构图文课件ppt: 这是一份九年级上册课题2 原子的结构图文课件ppt,共25页。PPT课件主要包含了原子的结构,重走科学之路,原子的体积,我真棒,我能行,分组讨论,《原子的构成》,开心辞典练习题,电子的自白,作业二等内容,欢迎下载使用。













