




高中人教版 (2019)实验活动2 强酸与强域的中和滴定课堂教学ppt课件
展开
这是一份高中人教版 (2019)实验活动2 强酸与强域的中和滴定课堂教学ppt课件,共24页。PPT课件主要包含了图S2-1,图S2-2,图S2-3,80mL,图S2-4,酸式滴定管等内容,欢迎下载使用。
【实验目的】1.练习中和滴定的实验操作;理解中和滴定的原理;探究酸碱中和反应过程中pH的变化特点。2.通对实验进一步掌握数据分析的方法,体会定量实验在化学实验研究中的作用。【实验用品】酸式滴定管、碱式滴定管、滴定管夹、烧杯、锥形瓶、铁架台。0.100 0 ml·L-1 HCl溶液、0.100 0 ml·L-1左右的NaOH溶液、酚酞溶液、蒸馏水。
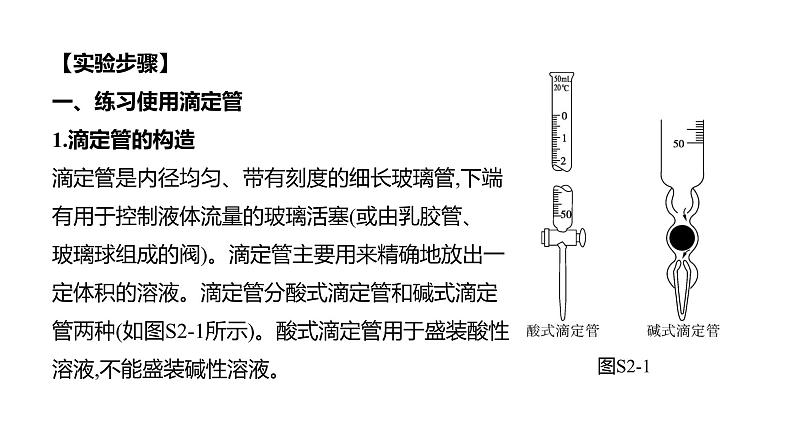
【实验步骤】一、练习使用滴定管1.滴定管的构造滴定管是内径均匀、带有刻度的细长玻璃管,下端有用于控制液体流量的玻璃活塞(或由乳胶管、玻璃球组成的阀)。滴定管主要用来精确地放出一定体积的溶液。滴定管分酸式滴定管和碱式滴定管两种(如图S2-1所示)。酸式滴定管用于盛装酸性溶液,不能盛装碱性溶液。
2.滴定管的使用方法(1)检查仪器:在使用滴定管前,首先要检查活塞是否漏水,在确保不漏水后方可使用。(2)润洗仪器:在加入酸、碱之前,洁净的酸式滴定管和碱式滴定管要分别用所要盛装的酸、碱润洗2~3次。方法是:从滴定管上口加入3~5 mL所要盛装的酸溶液或碱溶液,倾斜着转动滴定管,使液体润湿全部滴定管内壁。然后,一手控制活塞(轻轻转动酸式滴定管的活塞;或者轻轻挤压碱式滴定管中的玻璃球),将液体从滴定管下部放入预置的烧杯中。
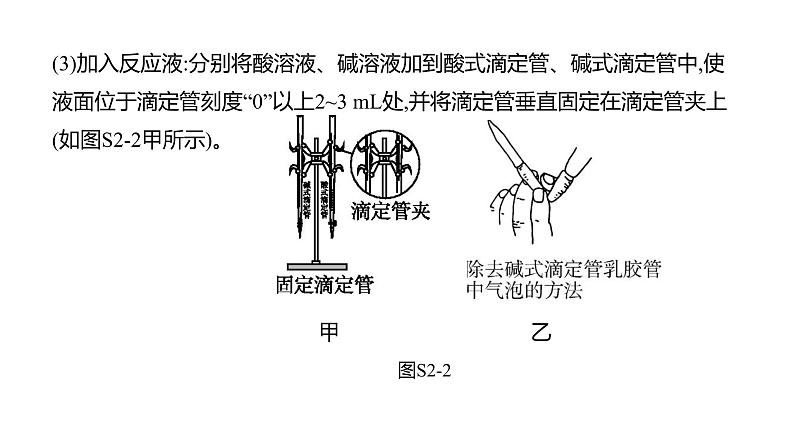
(3)加入反应液:分别将酸溶液、碱溶液加到酸式滴定管、碱式滴定管中,使液面位于滴定管刻度“0”以上2~3 mL处,并将滴定管垂直固定在滴定管夹上(如图S2-2甲所示)。
甲 乙
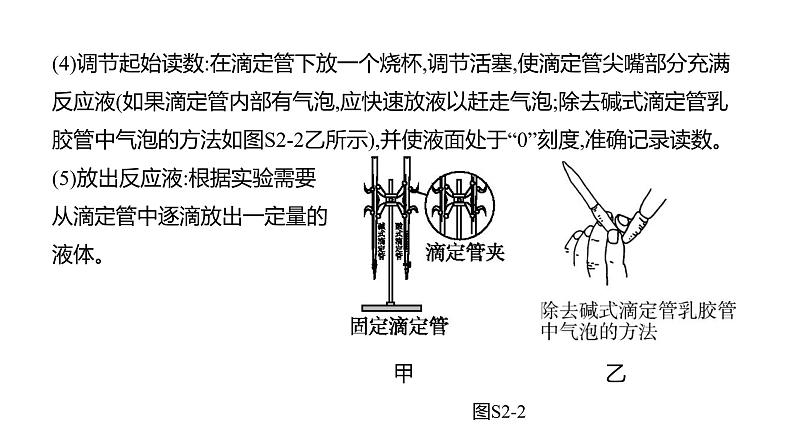
(4)调节起始读数:在滴定管下放一个烧杯,调节活塞,使滴定管尖嘴部分充满反应液(如果滴定管内部有气泡,应快速放液以赶走气泡;除去碱式滴定管乳胶管中气泡的方法如图S2-2乙所示),并使液面处于“0”刻度,准确记录读数。(5)放出反应液:根据实验需要从滴定管中逐滴放出一定量的液体。
二、用已知浓度的强酸滴定未知浓度的强碱1.向润洗过的酸式滴定管中加入0.100 0 ml·L-1 HCl溶液,赶气泡、调节液面至“0”刻度后记录准确读数。2.向润洗过的碱式滴定管中加入待测浓度的NaOH溶液,赶气泡、调节液面至“0”刻度后,用碱式滴定管向锥形瓶中滴入25.00 mL待测溶液,再向其中滴入2滴酚酞溶液,这时溶液呈红色。
3.把锥形瓶放在酸式滴定管的下方,瓶下垫一张白纸,小心地滴入酸。边滴边摇动锥形瓶,接近终点时,改为滴加半滴酸,直到因加入半滴酸后,溶液颜色从粉红色刚好变为无色,且半分钟内不变色为止。这表示已经到达滴定终点。记录滴定管液面的读数,并填入表中。4.重复实验两次,并记录相关数据。5. 计算待测NaOH溶液中NaOH的物质的量浓度。
【问题和讨论】1.在进行中和滴定时,为什么要用酸(或碱)润洗酸式(或碱式)滴定管2~3次?2.滴定用的锥形瓶是否也要用待测的碱(或酸)润洗?锥形瓶装待测液前是否需要保持干燥?为什么?
提示:1.因为酸式(或碱式)滴定管在实验前会先用水清洗,若不用待装液润洗,会降低标准溶液的浓度,最终影响实验的精确度。2.滴定用的锥形瓶不能用待测的碱(或酸)润洗,否则会导致待测液浓度偏大;锥形瓶是用来盛装一定体积待测溶液,装待测液前无需干燥,对实验结果无影响。
【实验评价】1.欲测定某HCl溶液的物质的量浓度,可用0.100 0 ml·L-1NaOH标准溶液进行中和滴定(用酚酞作指示剂)。请回答下列问题:(1)若甲学生在实验过程中,记录滴定前滴定管内液面读数为1.10 mL,滴定后液面如图S2-3,则此时消耗标准溶液的体积为 。
[解析]滴定前滴定管内液面读数为1.10 mL,滴定后液面读数是24.90 mL,此时消耗标准溶液的体积为24.90 mL-1.10 mL=23.80 mL;
(2)乙学生做了三组平行实验,数据记录如下:
选取上述合理数据,计算出HCl待测溶液的物质的量浓度为 ml·L-1(小数点后保留四位)。
(3)滴定时的正确操作是 。 滴定达到终点的现象是 ; 此时锥形瓶内溶液的pH的范围是 。
左手控制活塞,右手不断摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化
当滴入最后一滴NaOH溶液时,溶液颜色恰好由无色变为浅红色,且半分钟内不变色
[解析]中和滴定时,左手控制活塞,右手不断摇动锥形瓶,眼睛注视锥形瓶中溶液颜色的变化;滴定过程中,溶液pH升高,所以滴定达到终点的现象是:当滴入最后一滴NaOH溶液时,溶液颜色恰好由无色变为浅红色,且半分钟内不变色;指示剂酚酞的变色范围是8.2~10.0,此时锥形瓶内溶液的pH的范围是8.2~10.0;
(4)下列哪些操作会使测定结果偏高 (填序号)。 A.锥形瓶用蒸馏水洗净后再用待测液润洗B.酸式滴定管用蒸馏水洗净后再用标准液润洗C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失D.滴定前读数正确,滴定后俯视滴定管读数
[解析]锥形瓶用蒸馏水洗净后再用待测液润洗,HCl物质的量增多,消耗氢氧化钠溶液体积偏大,测定结果偏高,选A;酸式滴定管用蒸馏水洗净后再用标准液润洗,无影响,不选B;滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失,消耗氢氧化钠溶液的体积偏大,测定结果偏高,选C;滴定前读数正确,滴定后俯视滴定管读数,氢氧化钠溶液的体积偏小,测定结果偏低,不选D。
2.滴定实验是化学学科中重要的定量实验。请回答下列问题:Ⅰ.酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液。(1)该学生的实验操作如下:a.用碱式滴定管取稀NaOH溶液 25.00 mL,注入锥形瓶中,加入甲基橙作指示剂。b.用待测定的溶液润洗碱式滴定管。c.用蒸馏水洗干净滴定管。d.取下酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3 cm处,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下。
e.检查滴定管是否漏水。f.另取锥形瓶,再重复操作一次。g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。①滴定操作的正确顺序是(用序号填写) →c→ → →d→ → 。
e b a g f
[解析]中和滴定有检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等操作,所以滴定操作的正确顺序是ecbadgf;
②某次滴定前、后的盛放盐酸滴定管中液面的位置如图S2-4。请回答:仪器A的名称是 ;盐酸的体积读数:滴定前读数为 mL,滴定后读数为 mL;
[解析]仪器A为酸式滴定管,滴定前读数为0.80 mL,滴定后读数为22.80 mL;
③在G操作中如何确定终点 。
当滴入最后一滴溶液,锥形瓶内溶液由黄色变为橙色且半分钟内不褪色
[解析]用甲基橙作指示剂时,溶液由黄色变橙色,且半分钟内不变色,则到达滴定终点;
(2)下列操作造成测定结果偏高的是 (填选项字母) A.滴定终点时,俯视滴定管溶液液面B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
Ⅱ.氧化还原滴定——用标准KMnO4溶液滴定草酸溶液取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.100 0 ml·L-1的高锰酸钾溶液滴定,发生的反应为2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
(1)滴定时,KMnO4溶液应装在 (“酸”或“碱”)式滴定管中,滴定终点时滴定现象是 。 (2)该草酸溶液的物质的量浓度为 。
锥形瓶内由无色变为浅紫色,且半分钟内不褪色
0.200 0 ml·L-1
相关课件
这是一份人教版 (2019)选择性必修1实验活动2 强酸与强域的中和滴定教学演示课件ppt,共29页。PPT课件主要包含了玻璃活塞,氧化性,是否漏水,~3mL,红色刚好变为无色,半分钟内,数据记录等内容,欢迎下载使用。
这是一份人教版 (2019)选择性必修1实验活动2 强酸与强域的中和滴定评课课件ppt,共27页。
这是一份高中化学人教版 (2019)选择性必修1第三章 水溶液中的离子反应与平衡实验活动2 强酸与强域的中和滴定课前预习课件ppt,文件包含第三章水溶液中的离子反应与平衡_实验活动2强酸与强碱的中和滴定-课件ppt、第三章水溶液中的离子反应与平衡_实验活动2强酸与强碱的中和滴定-教案docx等2份课件配套教学资源,其中PPT共39页, 欢迎下载使用。










