






初中化学人教版九年级下册课题3 溶液的浓度课文内容ppt课件
展开1. 在t2时A物质的溶解度是_________,在该温度下把50克的物质溶解在100克的水中充分搅拌,则所得的溶液中溶质的质量分数是_________________
(可列出计算式子即可)
2、把100克质量分数是90%的浓硫酸稀释为质量分数20%的稀硫酸溶液,需加水多少克?
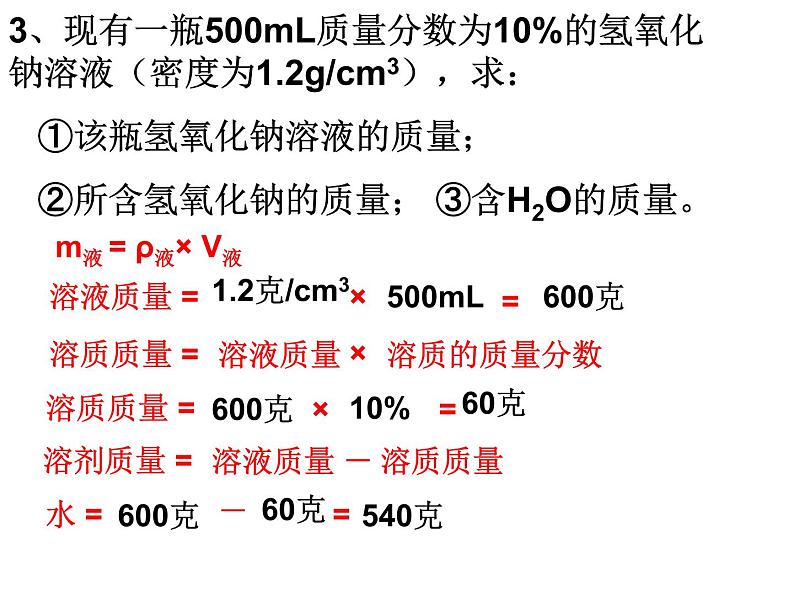
3、现有一瓶500mL质量分数为10%的氢氧化钠溶液(密度为1.2g/cm3),求: ①该瓶氢氧化钠溶液的质量; ②所含氢氧化钠的质量; ③含H2O的质量。
1. 在t2时A物质的溶解度是_________,在该温度下把50克的物质溶解在100克的水中充分搅拌,则所得的溶液中溶质的质量分数是__________
(100g + X) ×20%
X = 450g-100g
m液 = ρ液× V液
3、现有一瓶500mL质量分数为10%的氢氧化钠溶液(密度为1.2g/cm3),求: ①该瓶氢氧化钠溶液的质量; ②所含氢氧化钠的质量; ③含H2O的质量。
四、在化学方程式中涉及溶质质量分数的计算
基本思路:按化学方程式计算的方法进行计算
即:溶质质量 = 溶液质量 × 溶质的质量分数
把溶液的质量转化成溶质的质量,再去计其它质量
给出某溶液及其溶质的质量分数,求其它质量
(2)给出其它质量,求某溶液中溶质的质量分数
一般先利用化学方程式先计溶质的质量,再求溶质的质量分数
解:设生成氢气的质量为X
2 ×(1+35.5)
例1. 100克质量分数是14.6 %的稀盐酸和足量的锌完全反应,则完全反应生成氢气多少克?
Zn + HCl =
Zn 65 H 1 Cl 35.5
【练习】H=1,O=16,CI=35.5 C=12 100g质量分数是7.3%的稀盐酸和足量的大理石混合,完全反应,能制得多少克的CO2?
解:设制得二氧化碳的质量为X
这些气体的体积是多少升?(二氧化碳的密度在标准状况下约是2克/升)
例2、100g的某硫酸和足量的锌粒混合,完全反应后,能制得0.2g H2,求该硫酸中溶质的质量分数。
解:设硫酸溶液中溶质的质量为X
(1+32+16×4)
ZnSO4 + H2↑
解:设盐酸溶液中溶质的质量为X
练习2. 100克的稀盐酸和13克的锌刚好完全反应,则这盐酸中溶质的质量分数是多少?
H2 +ZnCl2
练2 100 g的某过氧化氢溶液和二氧化锰混合,完全反应后制得3.2g的O2,求过氧化氢溶液中溶质的质量分数。
练4、50g的某过氧化氢溶液和4g二氧化锰混合,完全反应后,得到50.8g的剩余物,求(1)生成氧气多少克?(2)过氧化 氢溶液中溶质的质量分数。
【练3】 100g的某硫酸和足量的锌粒混合,完全反应后,能制得0.2g H2,求该硫酸中溶质的质量分数。
H=1 O=16 S=32 Zn=65
解:设过氧化氢溶液中溶质的质量为X
2 ×(1×2+16×2)
50g+4g-50.8g
练4、50g的某过氧化氢溶液和4g二氧化锰混合,完全反应后,得到50.8g的剩余物,求(1)生成氧气多少克?,(2)过氧化 氢溶液中溶质的质量分数。
练4、50g的某过氧化氢溶液和4g二氧化锰混合,完全反应后,得到50.8g的剩余物,(2)过氧化 氢溶液中溶质的质量分数。
1、配制50克质量分数是20 %的稀硫酸,需要质量分数是80%的浓硫酸(1)_____克和水(2)_____克。实际所需的浓硫酸是(3)_____ mL(该硫酸的密度是1.5克/mL)(要列式、计数,精确到0.1)
2、 100 g质量分数是9.8%的稀硫酸和足量的锌粒混合完全反应后,能制得多少克H2?H=1,O=16 S=32 Cl=35.5 C=12
3. 50g质量分数是14.6%的稀盐酸和足量的大理石混合,完全反应,能制得多少克的CO2?
例1 100 g质量分数是6.8%的过氧化氢溶液和足 量的二氧化锰混合完全反应后,能制得多少 克O2?H=1,O=16
解:设制得氧气的质量为X
2×(1×2+16×2)
16、在一定温度下,向一定量的氯化钠溶液(未饱和) 中不断加入氯化钠固体,并搅拌,在此过程中溶液 里溶质的质量分数(w)与加入氯化钠质量(m)的 变化关系如图所示,其中图像正确的是( )
17、在一定温度下,向一定量的饱和氯化钠溶液 中不断加入氯化钠固体,并搅拌,在此过程中溶液 里溶质的质量分数(w)与加入氯化钠质量(m)的 变化关系如图所示,其中图像正确的是( )
18、在一定温度下,向一定量的水 中不断加入氯化钠固体,并搅拌,在此过程中溶液 里溶质的质量分数(w)与加入氯化钠质量(m)的 变化关系如图所示,其中图像正确的是( )
1 、 H=1,O=16,CI=35.5 C=12 100g质量分数是7.3%的稀盐酸和足量的大理石混合,完全反应,能制得多少克的CO2?
2 100 g的某过氧化氢溶液和二氧化锰混合,完全反应后制得3.2g的O2,求过氧化氢溶液中溶质的质量分数。
1H=1,O=16,CI=35.5 C=12 100g质量分数是7.3%的稀盐酸和足量的大理石混合,完全反应,能制得多少克的CO2?
初中化学人教版九年级下册课题3 溶液的浓度教学ppt课件: 这是一份初中化学人教版九年级下册课题3 溶液的浓度教学ppt课件,共20页。PPT课件主要包含了硫酸铜溶液,溶液的浓度,一溶质质量分数,合作探究1,合作探究2,谈体会说收获,练一练等内容,欢迎下载使用。
初中化学人教版九年级下册第九单元 溶液课题3 溶液的浓度优秀课件ppt: 这是一份初中化学人教版九年级下册第九单元 溶液课题3 溶液的浓度优秀课件ppt,共20页。PPT课件主要包含了学习目标,新课学习,飞机喷洒农药,喷洒药水,溶质的质量分数,×100%,05%,44%,比一比算一算,09%等内容,欢迎下载使用。
初中化学人教版九年级下册课题3 溶液的浓度精品课件ppt: 这是一份初中化学人教版九年级下册课题3 溶液的浓度精品课件ppt,共35页。PPT课件主要包含了导入新课,学习目标,讲授新知,躬行实践,溶质的质量分数,知识小结,溶质的稀释与浓缩,计算时的注意事项,知识总结,学以致用等内容,欢迎下载使用。











