- 专题:氧化还原反应同步练习 学案 16 次下载
- 专题:氧化还原反应 学案 21 次下载
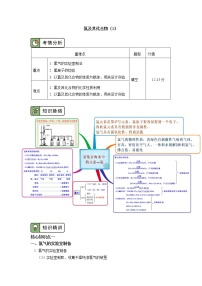
- 必修1 第二章 第二节 氯及其化合物(1)同步练习 学案 12 次下载
- 必修1 第二章 第二节 氯及其化合物(2) 学案 学案 25 次下载
- 必修1 第二章 第二节 氯及其化合物(2)同步练习 学案 14 次下载
高中化学人教版 (2019)必修 第一册第二节 氯及其化合物优秀导学案
展开核心知识点一:
一、氯气的性质
1. 氯元素的概述
(1)氯元素的存在
在自然界中只以化合物的形式存在;以NaCl、MgCl2、CaCl2等形式大量存在与海水中,还存在与陆地的盐湖和盐矿中。
(2)氯的原子结构
氯原子最外层有7个电子,在化学反应中容易得到一个电子,使最外层达到8个电子的稳定结构。因此,氯气是很活泼的非金属单质,具有强氧化性。
2. 氯气的物理性质
[注意]实验室里闻有毒气体及未知气体气味的方法是用手在瓶口轻轻扇动,仅使极少量气体飘进鼻孔即可。
3. 氯气与单质反应
(1)与金属反应
①与钠反应:2Na+Cl2eq \(=====,\s\up7(点燃))2NaCl。钠在氯气中剧烈燃烧,火焰呈黄色,生成白烟
②与铁反应:2Fe+3Cl2eq \(=====,\s\up7(点燃))2FeCl3。剧烈燃烧,产生棕褐色的烟
③与铜反应:Cu+Cl2eq \(=====,\s\up7(点燃))CuCl2。剧烈燃烧,产生棕黄色的烟,加少量的水,溶液呈绿色,加较多的水,溶液呈黄色
(2)与非金属反应与H2反应:H2+Cl2eq \(=====,\s\up7(点燃))2HCl。
核心知识点二
二、氯气与化合物反应
1. 与水反应:溶于水的氯气部分与水反应,离子方程式为Cl2+H2O=H++Cl-+HClO。
2. 与碱反应 Cl2+2NaOH===NaCl+NaClO+H2O。
3. 与还原性无机化合物反应(书写离子方程式)
①与碘化钾溶液反应:2I-+Cl2===I2+2Cl-。
②与SO2水溶液反应:Cl2+SO2+2H2O===4H++2Cl-+SO42-。
③与FeCl2溶液反应:2Fe2++Cl2===2Fe3++2Cl-。
4. 次氯酸
(1)不稳定性见光易分解,化学方程式为2HClOeq \(=====,\s\up7(光照))2HCl+O2↑。
(2)强氧化性①能将有色物质氧化为无色物质,作漂白剂。②杀菌、消毒。
(3)弱酸性比碳酸酸性弱,电离方程式为 HClO H++ClO-。
5. 次氯酸盐
(1)漂白液有效成分:NaClO,漂白原理NaClO+CO2+H2O===NaHCO3+HClO。
(2)漂白粉
①成分:漂白粉的主要成分是Ca(ClO)2、CaCl2,其中有效成分是Ca(ClO)2。
②制备原理:化学方程式为2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O。
③漂白原理:化学方程式为Ca(ClO)2+H2O+CO2===CaCO3↓+2HClO。
6. 氯水的成分和多重性质
(1)氯水的成分分析
(2)新制氯水的多重性质
①氯气具有强氧化性,与变价金属反应时均生成高价态的金属氯化物,如FeCl2不能由两种单质化合生成。
②氯气没有漂白性,不能使干燥的有色布条褪色,但可使湿润的有色布条褪色,起漂白作用的物质是HClO。
③ClO-不论是在酸性、碱性条件下都能跟亚铁盐、碘化物、硫化物、亚硫酸盐等发生氧化还原反应,即ClO-与I-、Fe2+、S2-、SO不论是在酸性环境还是在碱性环境中均不能大量共存。
④氯水中因HClO见光分解,随着HClO的消耗,最后成为盐酸,故久置氯水酸性增强,无漂白性。因此,氯水要现用现配,通常保存在棕色试剂瓶中并置于阴暗处。
核心知识点一:
下列说法正确的是( )
A. Cl2具有很强的氧化性,在化学反应中只能做氧化剂
B. 红热的铜丝在Cl2中燃烧,生成蓝色固体CuCl2
C. 有Cl2参加的化学反应必须在溶液中进行
D. Fe在Cl2中燃烧生成FeCl3
【考点】氯气的化学性质
【答案】D
【解析】A. Cl2的化合价为0价,处于中间价态,在化学反应中既能做氧化剂也能做还原剂。
B. 红热的铜丝在Cl2中剧烈燃烧,产生棕黄色的烟
C. 不一定,比如氯气与金属钠反应
下列化合物能用金属与氯气反应制备,又能用金属与盐酸反应制备的是( )
A. MgCl2
B. CuCl2
C. FeCl2
D. FeCl3
【考点】氯气与金属反应
【答案】A
【解析】A. Mg与Cl2反应可以生成MgCl2;Mg与盐酸反应可以生成MgCl2
B. Cu与盐酸不反应
C. Fe与Cl2反应生成FeCl3;与盐酸反应生成FeCl2;
D. Fe与Cl2反应生成FeCl3;与盐酸反应生成FeCl2;
核心知识点二:
下列说法中不正确的( )
A. 氯水的pH小于7
B. 燃烧一定有氧气参加
C. 紫色的石蕊试液中滴加氯水,先变红后褪色
D. 用氯气消毒自来水的原因是:氯气与水反应生成的HCl有强氧化性,可杀灭水中的细菌
【考点】氯水的性质
【答案】BD
【解析】A. 氯与水反应生成盐酸和次氯酸,显酸性,固pH小于7
B. 不一定吗,比如金属钠与氯气反应,属于燃烧,但是没有氧气参与反应
C. 紫色的石蕊试液中滴加氯水,溶液显酸性,所以紫色石蕊变红。因为有次氯酸,有强氧化性,故褪色
D. 氯气与水反应生成的HClO有强氧化性,可杀灭水中的细菌
新制的氯水与久置的氯水相比较,下列说法不正确的是( )
A. 都呈酸性
B. 前者能使有色布条褪色
C. 光照新制氯水有气体逸出,该气体是Cl2
D. 加AgNO3溶液都能生成白色沉淀
【考点】考查氯水的性质
【答案】B
【解析】新制的氯水中含有分子Cl2、HClO、H2O,离子H+、Cl-、ClO-、OH-,次氯酸光照时发生反应生成盐酸与氧气。所以久置的氯水实际上已经是盐酸。
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 下列关于氯及其化合物说法正确的是( )
A. 漂白粉是混合物,有效成分是Ca(ClO)2
B. 光照氯水有气泡逸出,该气体是Cl2
C. Cl2能使湿润的有色布条褪色,说明Cl2具有漂白性
D. 实验室用二氧化锰与稀盐酸反应制取Cl2
2. 关于氯水中存在的各种成分,下列说法中可能错误的是( )
A. 加入含有NaOH的酚酞试液,红色褪去,说明有H+存在
B. 加入有色布条后,有色布条褪色,说明有HClO分子存在
C. 氯水呈浅黄色,且有刺激性气味,说明有Cl2分子存在
D. 加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl-存在
3. 在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用以鉴别的一种试剂是( )
A. 氢氧化钠溶液 B. 酚酞试液 C. 硝酸银溶液 D. 氯化钡溶液
4. 下列关于漂粉精在空气中容易失效原因的准确表述是( )
①次氯酸不稳定,易分解 ②CaCl2易潮解
③Ca(ClO)2易和盐酸反应 ④Ca(ClO)2易和空气中的CO2和H2O反应
A. 只有① B. 只有② C. ①和② D. ①④
5. 下列物质中含有Cl-的是( )
A. 液氯 B. KClO3 C. HCl气体 D. 氯水
6. (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是_______________。
(2)为防止氯气尾气污染空气,根据氯水显酸性的性质,可用_______________溶液吸收多余的氯气,原理是(用化学方程式表示)_________________________________。根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,漂白粉的有效成分是__________(化学式),长期露置于空气中的漂白粉,加稀盐酸后产生的气体是__________(字母代号填)。
A. O2 B. Cl2 C. CO2 D. HClO
(3)据报道,某化工总厂最近相继发生氯气泄漏和爆炸事故,当人们逃离爆炸现场时,可以用浸有一定浓度的某种物质的水溶液的毛巾捂住鼻子,最适宜采用的该物质是___________。
A. NaOH B. NaCl C. KBr D. Na2CO3
7. 有X、Y、Z三种元素:
(1)X、Y、Z的单质在常温下均为气体;
(2)X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;
(3)XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;
(4)每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;
(5)Z单质溶于X2Y中,所得溶液具有漂白性。
试写出其元素符号:
(1)X_______,Y_______, Z_______,以及化合物的分子式:XZ_______,X2Y_________。
(2)写出Z单质与X2Y反应的化学反应方程式:____________________________。
1. 答案:A
【解析】B、气体是O2,故错;C、应是HClO具有漂白性,故错;D、应是浓盐酸,故错。故选A。
2. 答案:A
【解析】碱遇酚酞变红,氢离子与碱反应使颜色消失,但次氯酸具有漂白性,也能使颜色褪去,则不能说明氢离子存在,A错误;次氯酸具有强氧化性,能够漂白有色物质,则加入有色布条后,有色布条褪色,则说明氯水中有HClO分子存在,B正确;氯气为黄绿色气体,具有刺激性气味,说明氯气分子存在C正确;加入硝酸酸化的硝酸银溶液产生白色沉淀,该沉淀为AgCl,说明氯水中有氯离子存在D正确
3. 答案:C
【解析】硝酸银与氯离子反应能生成氯化银白色沉淀。
4. 答案:D
【解析】漂粉精在空气中容易失效原因是Ca(ClO)2易和空气中的CO2和H2O反应生成次氯酸,次氯酸不稳定,易分解
5. 答案:B
【解析】A. 液氯中只含有氯分子
B. KClO3存在的是氯酸根,没有氯离子
C. HCl气体含有氯化氢分子
D. 氯水中氯气与水反应生成氯化氢,氯化氢在水中能电离生成氯离子
6. 答案:(1)潮湿有色布条褪色而干燥有色布条不褪色(2)氢氧化钠(NaOH)2NaOH+Cl2=NaClO+NaCl+H2O
Ca(ClO)2; C
(3)D
7. 答案:(1)H O Cl HCl H2O
(2)Cl2+ H2O==HCl+HClO
【解析】X、Y、Z的单质在常温下均为气体;
X单质可以在Z的单质中燃烧,生成物为XZ,火焰呈苍白色;且XZ极易溶于水,在水溶液中电离出X+和Z-,其水溶液能使蓝色石蕊试纸变红;证明XZ是HCl,其中X是氢气,Z是氯气
每2个X2分子能与1个Y2分子化合成2个X2Y分子,X2Y常温下为液体;且Z单质溶于X2Y中,所得溶液具有漂白性。所以X2Y为H2O。重难点
题型
分值
重点
1. 氯气的物理性质
2. 氯气与单质反应
3. 氯气与化合物反应
选择、
填空
12-15分
难点
1. 氯气与单质的反应
2. 氯气与化合物的反应
颜色
状态
气味
密度
毒性
溶解性
黄绿色
气体
刺激性气味
比空气大
有毒
1体积水溶解约2体积Cl2
三分子
四离子
H2O、Cl2、HClO
H+、Cl-、ClO-、OH-
化学第二节 氯及其化合物第1课时导学案: 这是一份化学第二节 氯及其化合物第1课时导学案,共9页。
化学选择性必修1第二节 化学平衡精品第1课时学案及答案: 这是一份化学选择性必修1第二节 化学平衡精品第1课时学案及答案,共7页。学案主要包含了学习目标,学习过程,思维模型,深入研究,学以致用,学习效果等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 氯及其化合物导学案: 这是一份高中化学人教版 (2019)必修 第一册第二节 氯及其化合物导学案,共14页。学案主要包含了学习目标,基础知识,考点剖析等内容,欢迎下载使用。