






备战2021广东中考化学课堂教本第一部分 考点十一 盐 化肥
展开一、生活中常见的盐1.常见的盐及其用途
2.化学性质(1)盐溶液的酸碱性:大多数盐溶液显中性,少部分盐溶液显碱性,如K2CO3、Na2CO3、NaHCO3等的溶液显碱性。(2)与某些金属反应生成新盐和新金属①条件:盐必须可溶,金属单质(除K、Ca、Na)的活动性要强于盐中的金属。
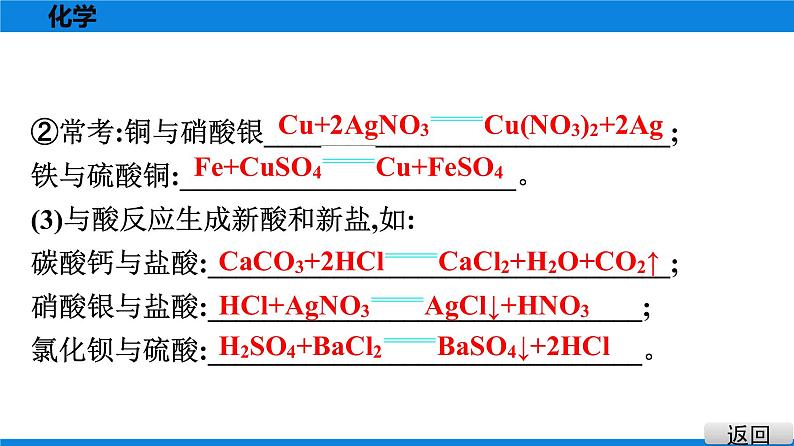
②常考:铜与硝酸银_____________________________; 铁与硫酸铜:________________________。 (3)与酸反应生成新酸和新盐,如:碳酸钙与盐酸:_________________________________; 硝酸银与盐酸:_______________________________; 氯化钡与硫酸:_______________________________。
(4)与碱反应生成新盐和新碱,如:碳酸钠与氢氧化钙:__________________________; 硫酸铜与氢氧化钠:__________________________; (5)与某些盐反应生成新盐和新盐①条件:两种盐必须可溶,生成物有沉淀或气体或水。
②常考:氯化钙与碳酸钠:__________________________; 硫酸铜与氯化钡:_________________________________。 3.粗盐提纯(详见实验突破)4.复分解反应(1)概念:两种化合物互相交换成分,生成另外两种化合物的反应。
(2)复分解反应发生的条件:反应物有酸可不溶,无酸必都溶;生成物中有沉淀或有气体或有水生成,满足一个条件即可。(3)常见难溶化合物①难溶性碱: (蓝色)、 (白色)、 (红褐色)等。 ②难溶性盐:AgCl、BaSO4、CaCO3、BaCO3等。
二、化学肥料1.化肥的简易鉴别(一看二闻三溶四加碱)
点拨:(1)氮肥中的 呈液态,碳酸氢铵有强烈的氨味,这是因为碳酸氢铵在常温下不稳定,分解生成氨气;
(2)检验铵盐的方法:铵盐都能与碱反应,放出有刺激性气味的 ,其能使湿润的红色石蕊试纸变 ,据此可以检验铵盐;
2.化肥的作用(1)氮肥:促进植物茎、叶生长茂盛,叶色浓绿,提高植物蛋白质的含量(壮叶)。(2)磷肥:促进作物生长,增强作物抗寒、抗旱能力(壮果)。(3)钾肥:促进植物生长、增强抗病虫害和抗倒伏能力(壮茎)。(4)复合肥:同时均匀地供给作物几种养分,充分发挥营养元素间的作用,有效成分高。
1.(全国视野:科普)下列含氮化合物中不属于盐的是( )A.NH4NO3 B.NH3·H2O C.NH4HCO3 D.(NH4)2SO4
2.(粤教P249)在以下有关纯碱的描述中,不正确的是( )A.“纯碱”其实不是碱,属于盐类B.可用纯碱代替洗涤剂洗涤餐具表面的油污C.用纯碱可除去面团发酵产生的酸D.用加水溶解的方法检验纯碱中是否混入了食盐
A.a处产生白色物质B.b处生成蓝色沉淀C.c处发生复分解反应D.d处产生气泡
3.(粤教P258)铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象。下列说法中错误的是( )
A.碳酸氢铵 B.碳酸氢钾C.尿素 D.磷酸二氢铵
4.(人教P81改编)小华家住农村,他和父亲一起下地,见到自家的大豆出现了易倒伏的缺钾现象。他建议可以适当补充的化肥是( )
5.(人教P81改编)今年夏粮又获丰收,再显中国饭碗自信,其中化肥功不可没。下列说法错误的是( )A.尿素[CO(NH2)2]能使作物枝叶繁茂、叶色浓绿B.磷酸二氢铵(NH4H2PO4)属于复合肥C.含氮量为31.5%的硝酸铵(NH4NO3)化肥样品为纯净物D.化肥虽好不能滥用,过度施肥会造成土壤退化和水体污染
【易错点总结】1.盐不一定是由金属离子和酸根离子构成,如铵盐就不含金属离子。2.盐与碱相遇或盐与盐相遇时必须符合复分解反应的条件才能产生。即生成的盐至少有一种是沉淀(不溶于水),且反应物中的盐和碱必须全部溶于水。3.农作物必需的营养元素有多种,不仅仅是氮、磷、钾,这三者的需要量较大。
1.以碳酸钠为核心的转化(“—”表示两种物质间可以发生反应,“→”表示两种物质间可以实现转化,化学方程式填写一个即可,下同):
①__________________________; ②____________________________; ③________________________; ④__________________________; ⑤___________________________。
2. 以碳酸钙为核心的转化
①___________________________; ②_____________________________; ③______________________________; ④________________________________; ⑤______________________________。
考点1 常见盐的性质和用途课标母题(课标提供素材:侯德榜对我国制碱工业的贡献)1.(2020越秀区二模)碳酸钠用途非常广泛,侯德榜先生发明了将制碱与制氨结合起来的联合制碱法(侯氏制碱法)。下列说法不正确的是( )
A.生产:常用钠单质与二氧化碳通过化合反应制得B.性质:碳酸钠水溶液呈碱性C.用途:碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产D.组成:碳酸钠由钠离子和碳酸根离子构成
中考母题2. (2020广东)Na2CO3俗称纯碱,侯德榜为纯碱工业的发展做出了杰出贡献。Na2CO3属于( )A.氧化物 B.盐C.有机物 D.混合物
3. (2014广东)下列物质的名称和俗名相对应的是( )A.碳酸钙—纯碱B.氯化钠—食盐C.碳酸钙—小苏打D.氧化钙—熟石灰
A.碳酸氢钠俗称小苏打B.泡打粉可以随意放置C.加入泡打粉制作的蛋糕更松软D.面粉是有机物,碳酸盐是无机物
4.(2017广东)图为××泡打粉的标签如图所示,下列说法错误的是( )
5.(2020深圳)小深同学用思维导图梳理了Na2CO3的相关知识,其中描述错误的是( )
6.(2018广东)学习了单质、氧化物、酸、碱、盐的性质后,可以发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为_______________________________。 (2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有 (选填序号)。 (3)若盐是硝酸铜,由⑦来实现的化学方程式为_________________________________________________。 (4)图中⑤处应补充的文字是 (写一种,不能与图中已有信息重复)。
全国视野7.下列图象能正确反映对应的实验操作的是( )
考点2 化学肥料课标母题(课标提供素材:常见铵态氮肥的性质特点及使用注意事项)1.(2019广东)化学肥料是农作物的“粮食”,下列关于化学肥料的说法正确的是( )A.尿素[CO(NH2)2]属于复合肥料 B.大量施用化肥以提高农作物产量C.铵态氮肥与草木灰混用,会降低肥效 D.棉花叶片枯黄,应施用硫酸钾等钾肥
2.(2016广东)公园里部分植物的枝叶枯黄,茎也比较纤细。建议工作人员最好给这些植物施用的一种化肥是( )A.NH4HCO3 B.KNO3 C.Ca(H2PO4)2 D.(NH4)3PO4
中考母题3.(2018广州)下列关于化肥的说法不正确的是( )A.化肥对提高农作物的产量具有重要作用B.氯化钾(KCl)和磷酸氢二铵[(NH4)2HPO4]都属于复合肥料C.铵态氮肥与熟石灰混合研磨后能嗅到刺激性气味D.化肥的过度使用会造成土壤酸化,可用熟石灰改良
(1)此包化肥中含氮的质量为 kg。 (2)该化肥的化学性质为:①与碱性物质混用会因放出 气而损失肥效;② 。 (3)该化肥的物理性质为 。
4.(2015广东)某化肥说明书的一部分如图。
全国视野5.(2020本溪)下列化学肥料中能促进植物生长,增强抗病虫害和抗倒伏能力的是( )A.K2SO4 B.CO(NH2)2 C.NaNO3 D.NH4H2PO4
(1)步骤①中通过观察到 现象,可以鉴别出碳酸氢铵。 (2)步骤②的试剂可以选用两种不同类别(按酸、碱、盐、氧化物进行分类)的物质,其化学式分别为 、 。
6.如图是某同学鉴别碳酸氢铵、硫酸铵、硝酸铵三种化肥的过程(反应条件未标出),请回答下列问题:
请写出硫酸铵分别与这两种试剂发生反应的化学方程式:__________________________________________;_____________________________________。
粗盐中难溶性杂质的去除
1.实验用品:托盘天平、蒸发皿、坩埚钳、酒精灯、漏斗、药匙、量筒、烧杯、玻璃棒、铁架台、滤纸、火柴、蒸馏水、粗盐。2.实验装置及步骤
(1)用托盘天平称取一定质量的粗盐,称量时要在托盘天平的两个托盘上各放一张干净的称量纸,防止 。 (2)用药匙将该粗盐逐渐加入盛有适量水的烧杯里,边加边 ,直到粗盐不再溶解为止。 (3)过滤:将粗盐水用玻璃棒 到过滤器。
药品污染和腐蚀托盘
(4)蒸发:将过滤后的澄清滤液倒入蒸发皿中,边加热边搅拌,防止 。 当蒸发皿 时,停止加热,利用蒸发皿余热将滤液蒸干。
液体受热不均导致液滴飞溅
3.误差分析(1)产率偏低:①粗盐未完全溶解就进行过滤;②溶解搅拌时溶液溅出;③蒸发时未用玻璃棒搅拌,导致液滴飞溅;④转移时有部分精盐残留在蒸发皿上或有部分精盐洒落。(2)产率偏高:①砝码锈蚀使实际称得的粗盐质量偏大;②提纯后的精盐尚未完全干燥就称其质量;③过滤时滤纸破损,滤液中进入部分难溶性固体杂质。
4.粗盐中可溶性杂质的去除:加入试剂的顺序及操作
5.所加试剂的作用及反应的化学方程式(1)加入过量的BaCl2溶液——除去__________,————————————————。 (2)加入过量的NaOH溶液——除去________,——————————————————。 (3)加入过量的Na2CO3溶液——除去___________________;________________________________。
CaCl2和过量的BaCl2
(4)加入过量的稀盐酸——除去_______________________;___________________________,_________________________________。
过量的NaOH和Na2CO3
6.实验分析(1)操作①与操作③的顺序能否颠倒?理由是 。 (2)在第④步操作中,加入的盐酸过量,对所得到的氯化钠纯度 影响(填“有”或“无”)。 (3)提纯后发现所得的氯化钠的质量大于粗盐中氯化钠的质量,原因是 。
在除杂过程中生成了NaCl
不能,若二者颠倒,无法除去加入过量的Ba2+
例1 实验课上,老师指导某兴趣小组利用10.0 g粗盐进行粗盐提纯的实验,邀请你帮助他们完成下面的实验报告。【查阅资料】1.粗盐中含有泥沙及少量可溶性的MgCl2、CaCl2、Na2SO4等杂质。2.Ba(OH)2是一种易溶于水的强碱。
【主要玻璃仪器】量筒、烧杯、漏斗、玻璃棒、胶头滴管、酒精灯。【主要试剂】粗盐样品、稀盐酸、BaCl2溶液、NaOH溶液、Na2CO3溶液、蒸馏水。
搅拌,防止局部温度过高,造成液滴飞溅
稀盐酸逐滴加入至刚好不再产生气泡
【结果与反思】(1)实验操作、试剂和装置均不存在问题,老师却指出该样品中氯化钠的质量分数不是94%,原因是 。 (2)小明提出,如果步骤Ⅱ中只调换“过量的NaOH溶液”与“过量的BaCl2溶液”的加入顺序,对除杂结果也不会产生影响,你 (填“同意”或“不同意”)小明的观点。
提纯过程中反应生成了氯化钠
复分解反应及其应用【难点讲解】对复分解反应的三种考向:1.判断复分解反应能否发生,根据前面考点过关中的“复分解反应发生的条件”可做解答。
2.判断物质之间能否发生转化:主要分析被转化物质能否与其他物质发生反应或自身能否发生分解反应,直接转化为题目要求的物质,需熟记常见物质的性质。一般情况下AgCl、BaSO4、KNO3、NaNO3等不能通过一步反应转化为其他物质。3.判断物质或离子是否共存:主要看物质间相互交换成分或阴、阳离子相互结合是否有沉淀、气体或水生成,若有则不能共存。解题时还应注意题目中的附加条件,如溶液的酸碱性、溶液的颜色等。
例2 (2020德州)下列物质间能够发生反应,但没有出现明显现象的是( )A.将稀盐酸滴入盛石灰石的试管中B.将CO2通入NaOH溶液中C.将碳酸钠溶液滴入澄清石灰水中D.将稀硫酸滴入NaCl溶液中
例3 (2020鸡西)下列各组物质在同一溶液中可以大量共存的是( )A.NaOH、FeCl3、K2SO4B.NaCl、HNO3、AgNO3C.NaCl、K2CO3、Ca(OH)2D.KNO3、NaCl、Ba(OH)2
例4 (2020镇江)下列各组溶液,不用其他试剂就能鉴别出来的是( )A.FeCl3、KOH、NaCl、Ba(NO3)2B.Na2CO3、BaCl2、NaNO3、稀HClC.Na2SO4、Ba(OH)2、NaOH、稀HNO3D.BaCl2、NaOH、MgSO4、KNO3
(数字化实验)某小组同学利用pH传感器对碳酸氢钠、碳酸钠的某些性质进行以下探究。
25 ℃时,向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入相同浓度的盐酸,用pH传感器测得pH变化与时间的关系如图1、图2所示。将图1与图2的阴影部分进行叠加,发现两者基本重合。回答下列问题:(1)含等碳原子数的碳酸氢钠和碳酸钠溶液均呈碱性,两种溶液碱性较强的是 。
备战2021广东中考化学课堂教本第一部分 考点二 碳与一氧化碳: 这是一份备战2021广东中考化学课堂教本第一部分 考点二 碳与一氧化碳,共21页。PPT课件主要包含了教材考点归纳,疏松多孔,吸附性,难溶于水,血红蛋白,教材母题变式拓展,变浑浊,防止石灰水倒,使反应更充分,使试管炸裂等内容,欢迎下载使用。
备战2021广东中考化学课堂教本第一部分 考点四 常见气体的制取: 这是一份备战2021广东中考化学课堂教本第一部分 考点四 常见气体的制取,共21页。PPT课件主要包含了伸入液面以下,气体沿长颈漏斗口逸出,浓硫酸,NaOH,饱和碳酸氢钠等内容,欢迎下载使用。
备战2021广东中考化学课堂教本第一部分 考点三 二氧化碳: 这是一份备战2021广东中考化学课堂教本第一部分 考点三 二氧化碳,共21页。PPT课件主要包含了教材考点归纳,变浑浊,化学性质,气体肥料,制冷剂,人工降雨,温室效应,固体变红色,NaOH,CuO等内容,欢迎下载使用。












