






高中化学人教版 (新课标)必修2第二节 来自石油和煤的两种基本化工原料背景图课件ppt
展开
这是一份高中化学人教版 (新课标)必修2第二节 来自石油和煤的两种基本化工原料背景图课件ppt,共38页。PPT课件主要包含了C6H6,苯的发现,科学史话P71,现代理论,苯分子的结构,苯的一取代物只有一种,苯的物理性质,有特殊,取代反应,实验小结等内容,欢迎下载使用。
有人说我笨,其实并不笨, 脱去竹笠换草帽,化工生产逞英豪。(打一有机化合物)
江西省鹰潭市第一中学 桂耀荣
Michael Faraday (1791-1867)
1825年,英国科学家法拉第在煤气灯中首先发现苯,并测得其含碳量,确定其最简式为CH; 1834年,德国科学家米希尔里希制得苯,并将其命名为苯; 之后,法国化学家日拉尔等确定其分子量为78,苯分子式为 。
(一)分子式:C6H6
1.根据分子式C6H6,它属于饱和烃还是不饱和 烃?
2.根据饱和链烃的通式,苯分子中可能含有的双键数目?
3.写出C6H6分子的可能链状结构简式。
1、CH2=C=CH—CH=C=CH2
2、CH2 =C=C = C=CH—CH3
3、CH2 =C=C = CH—CH=CH2
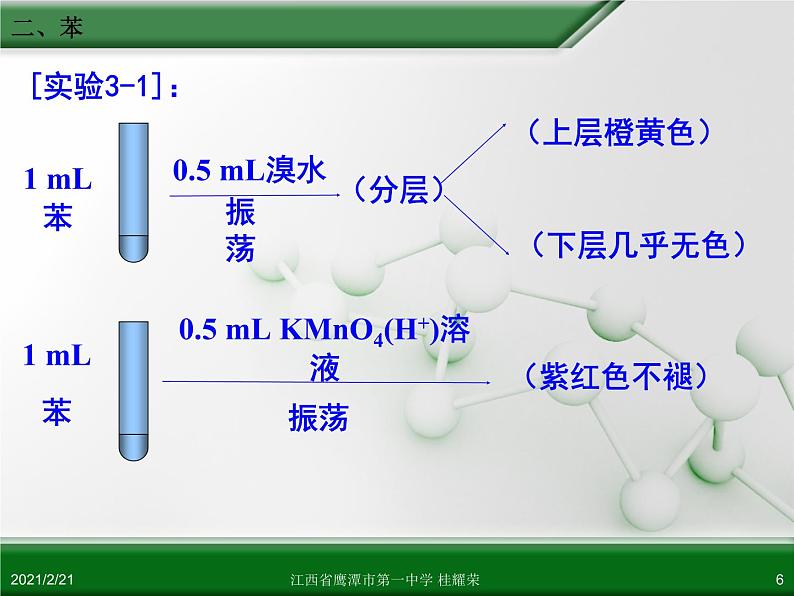
现象:溴的四氯化碳溶液和酸性KMnO4溶液都不褪色。
实验:向盛有1 mL苯的两支试管中分别滴加0.5 mL溴的四氯化碳溶液或酸性KMnO4溶液,振荡静置,观察现象。
实验结论1:苯与不饱和烃有很大区别,苯分子中没有双键。
实验结论2:苯分子中6个氢原子处于等同的地位。
设问:苯分子中有没有双键?
1.根据分子式推测出苯分子可能具有不饱和烃的结构;
2.根据实验结论1,否定苯分子具有不饱和链烃的结构;
3.根据实验结论2,推测苯分子可能是环状结构。
设问:C6H6中6个H处于同等地位,6个C能否形成直链?能否形成环状?
苯的发现和苯分子结构学说19世纪60年代,德国化学家凯库勒已经知道苯的分子式为C6H6,但它们是如何排列、连接的呢?他提出多种可能的排法,但经过推敲后都放弃了,他被这件工作弄得疲惫不堪。一天,他搁下写满字的厚厚一叠纸便朦胧地睡了。他在梦中看见6个碳原子组成了古怪的形状。6个碳原子组成的“蛇”不断“弯弯曲曲地蠕动着”。突然这条蛇似乎被什么东西所激怒,它狠狠地咬着自己的尾巴,后来牢牢地衔在尾巴尖,就此不动了。凯库勒哆嗦一下,醒了过来。多么奇怪的梦啊,总共只有一瞬间的梦,但是在他眼前的原子和分子却没有消失,他记住了在梦中看见的分子中原子的排列顺序,也许这就是答案吧?他匆匆地在纸上写下了他所能够回想的一切,后来凯库勒提出了两点假设。
凯库勒在1866年提出三点假设:(1)苯的六个碳原子形成闭合环状,即平面六边形(2)每个碳原子均连接一个氢原子(3)各碳原子间存在着单、双键交替形式
但若按照凯库勒的观点依旧不能解释:
①苯不能使溴水和酸性高锰酸钾溶液褪色
②邻二氯苯只有一种结构
结论:苯分子结构中不存在碳碳单键和双键交替结构
苯的分子结构:①平面正六边形结构(6个碳、6个氢在同一平面上,对角线位置的碳和氢在同一直线上)②键角是120°③碳碳键是一种介于单键和双键之间的独特的键(大π键)
(2)苯环上的碳碳键是介于单键和双键之间的 独特的键(六个键完全相同)
(1)苯分子中所有原子在同一平面, 为平面正六边形结构
(一)分子式 C6H6
C─C 1.54×10-10m
C=C 1.33×10-10m
苯中的6个C原子和H原子位置等同
苯通常是 、 气味的 毒 体, 溶于水,密度比水 , 熔点为5.5℃ ,沸点80.1℃, 易挥发。
注意:苯易燃烧,但不能被酸性KMnO4溶液氧化
⑴ 苯与溴的取代反应:
反应条件:纯溴、催化剂
苯环上的 H 原子还可被其它卤素原子所代替
①、溴水不与苯发生反应②、只发生单取代反应③、溴苯是不溶于水,密度比水大的无色,油状液体,能溶解溴,溴苯溶解了溴时呈褐色
互溶、不反应、深红棕色
烧杯底部有褐色油状物、不溶于水
1.苯、溴、Fe屑等试剂加入烧瓶的顺序是怎样的?
2.Fe屑的作用是什么?
3.将Fe屑加入烧瓶后,烧瓶内有什么现象?这说明什么?
4.长导管的作用是什么?
剧烈反应,烧瓶中充满红棕色蒸气。反应放热。
用于导气和冷凝回流(或冷凝器)
5.为什么导管末端不插入液面下?
6.哪些现象说明发生了取代反应而不是加成反应?
7.纯净的溴苯应是无色的,为什么所得溴苯为褐色?怎样使之恢复本来的面目?
溴化氢易溶于水,防止倒吸。
苯与溴反应生成溴苯的同时有溴化氢生成,说明它们发生了取代反应而非加成反应。因加成反应不会生成溴化氢。
因为未发生反应的溴溶解在生成的溴苯中。用水和碱溶液反复洗涤可以使褐色褪去,还溴苯以本来的面目。
①. 硝基苯是无色有苦杏仁味的油状液体,不溶 于水,密度比水大,有毒。
②. 混合时,要将浓硫酸缓缓注入浓硝酸中,并不 断振荡。
③. 条件: 50-60C 水浴加热
④. 浓H2SO4的作用 : 催化剂 脱水剂
请你写出苯与Cl2 加成 反应的方程式
苯比烯、炔烃难进行加成反应
苯的化学反应特点:易取代、难加成、难氧化
不被 酸性KMnO4溶液 氧化
易被酸性KMnO4溶液 氧化
苯不被酸性 KMnO4溶液氧化
苯环的碳碳键完全相同。
溶液分层;上层显橙色,下层近无色
Fe(或 FeBr3)
1、下列说法正确的是 ( )A.从苯的分子组成来看远没有达到饱和, 所以它能使溴水褪色B.由于苯分子组成的含碳量高,所以在空气 中燃烧时,会产生明亮并带浓烟的火焰C.苯的一氯取代物只有一种 D.苯是单、双键交替组成的环状结构
2、能说明苯分子中碳碳键不是单双键相间交替的事实是 ①苯不能使KMnO4溶液褪色;②苯环中碳碳键的键长均相等;③邻二氯苯只有一种;④在一定条件下苯与H2发生加成反应生成环己烷。 ( ) A. ①②③④ B.①②③ C. ②③④ D.①②④ 3、下列各组物质中可以用分液漏斗分离的( ) A. 酒精与碘 B.溴与四氯化碳 C. 硝基苯与水 D.苯与溴苯
总结:苯的化学性质(较稳定): 1、难氧化(但可燃); 2、易取代,难加成。
相关课件
这是一份人教版 (新课标)必修2第二节 来自石油和煤的两种基本化工原料图文ppt课件,共28页。PPT课件主要包含了小资料,空间结构,平面结构,乙烯的结构,乙烯的物理性质,排水法收集,乙烯的化学性质,溴分子,加成反应,科学视野P70等内容,欢迎下载使用。
这是一份高中化学第二节 化学能与电能背景图ppt课件,共20页。PPT课件主要包含了化学电池,一次性电池如干电池,总反应,充电电池,优点可反复使用,燃料电池,改变燃料,其他电池,废电池对环境的危害等内容,欢迎下载使用。
这是一份高中化学人教版 (新课标)选修2 化学与技术课题2 金属材料评课ppt课件,共28页。PPT课件主要包含了金属的广泛应用,从矿石中获得金属,电解法,热还原法,热分解法,活泼金属,较活泼金属,不活泼金属,1炼铁,钢铁的冶炼等内容,欢迎下载使用。









