



人教版 (新课标)选修5 有机化学基础第二节 有机化合物的结构特点背景图ppt课件
展开本节课以有机物分布广、种类多的小影片导入新课,使学生认识到有机化合物种类繁多的主要原因是碳原子的成键方式较多。再从最简单的有机化合物——甲烷开始,介绍碳原子的成键特点、成键方式与空间构型的关系并总结规律。然后在此基础上创设情境,通过观察思考,引出同分异构体的概念,并通过探究分析进一步归纳出同分异构体的判断方法。
选取了两道例题,每题均配有动画,借助有机物分子“拉”、“转”、“翻”的动态模拟演示,使学生对同分异构体的认识从感性上升到理性,完成对同分异构体知识的内化。
该微课(有机化合物的结构特征导入)简单介绍生活中的有机化合物种类繁多及其主要原因。可以增强学生对生活中有机物的认识,使学生感受到化学与人类生活的紧密联系,在激发学生的学习兴趣的同时又明确了学习的内容。
一、回忆:甲烷分子的表示式
一、有机物中碳原子的成键特点
在有机物分子中碳呈 价。
碳原子既可与其他原子形成 共价键,碳原子之间也可相互形成单键,也可以形成 或 ;碳碳之间可以形成长长的 ,也可以形成 。
有机物种类繁多的主要原因是什么?
碳原子既可与其他原子形成4个共价键;同时碳原子之间也可相互形成单键、双键或三键;碳碳之间既可以形成较长的碳链,又可以形成碳环。
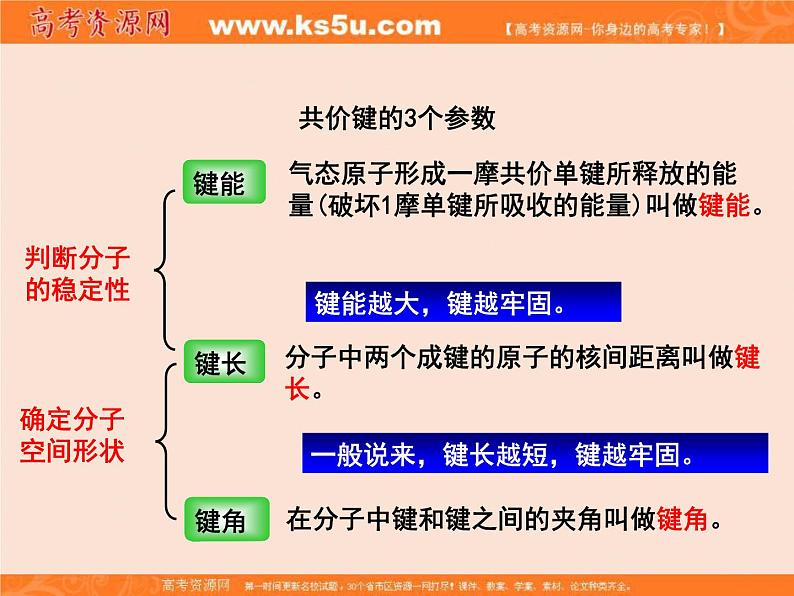
分子中两个成键的原子的核间距离叫做键长。
一般说来,键长越短,键越牢固。
气态原子形成一摩共价单键所释放的能量(破坏1摩单键所吸收的能量)叫做键能。
在分子中键和键之间的夹角叫做键角。
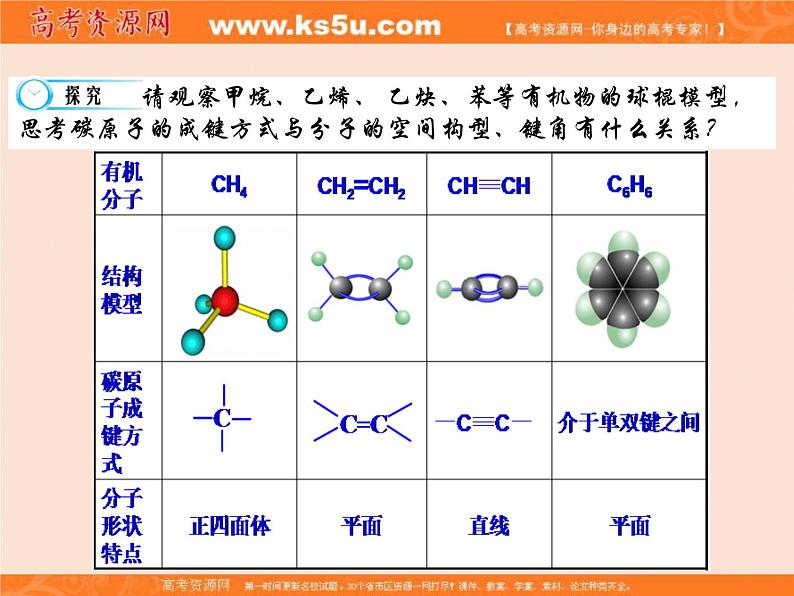
请观察甲烷、乙烯、 乙炔、苯等有机物的球棍模型,思考碳原子的成键方式与分子的空间构型、键角有什么关系?
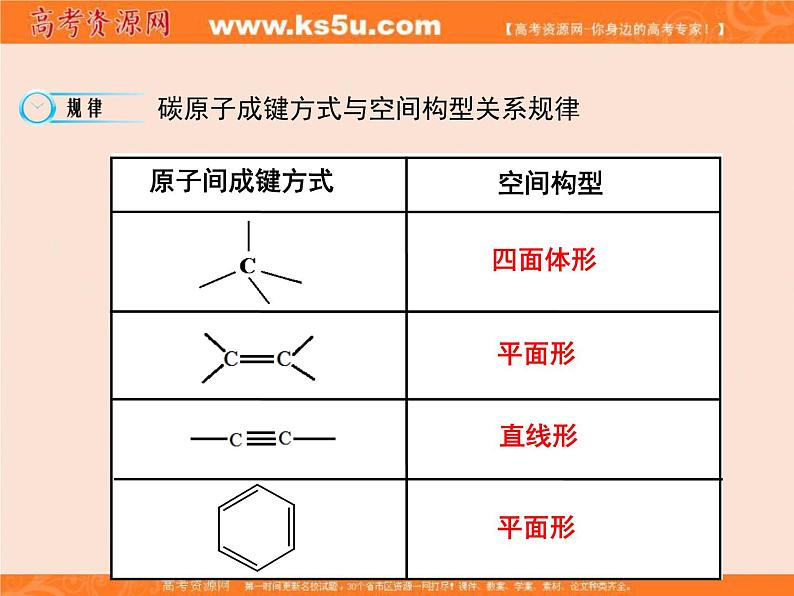
碳原子成键方式与空间构型关系规律
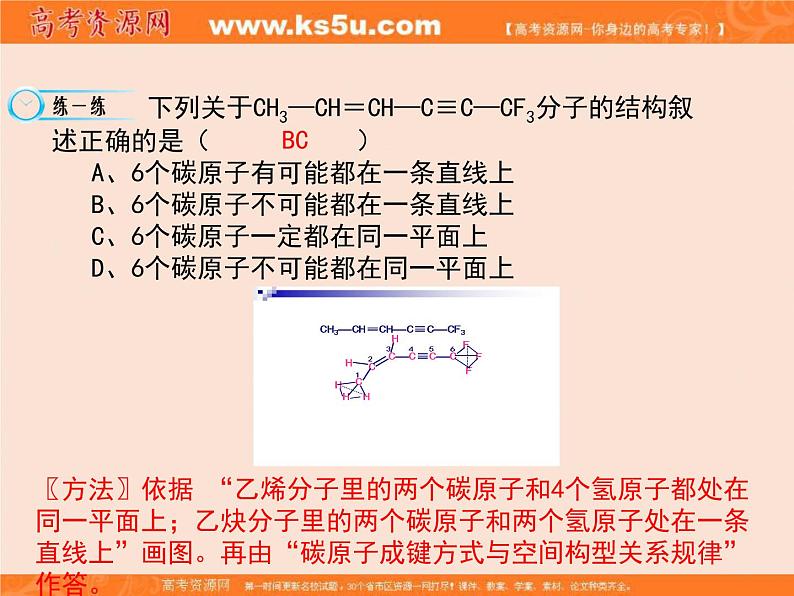
下列关于CH3—CH=CH—C≡C—CF3分子的结构叙述正确的是( ) A、6个碳原子有可能都在一条直线上 B、6个碳原子不可能都在一条直线上 C、6个碳原子一定都在同一平面上 D、6个碳原子不可能都在同一平面上
〖方法〗依据 “乙烯分子里的两个碳原子和4个氢原子都处在同一平面上;乙炔分子里的两个碳原子和两个氢原子处在一条直线上”画图。再由“碳原子成键方式与空间构型关系规律”作答。
碳原子不仅能与氢原子或其他原子形成4个共价键,碳原子之间也能相互以共价键结合。
(1)碳原子之间可以形成稳定的单键、双键、三键;
(2)多个碳原子可以相互结合成长短不一的碳链,碳链可带有支链;
(3)多个碳原子还可以相互结合成环,碳环和碳链还可以相互结合。
(1)根据图形,写出这三种物质的结构简式:
(2)从结构简式中,我们发现它们的相同点和不同点各是什么?
CH3CH2CH2CH2CH3
分子组成相同,链状结构
结构不同,出现带有支链结构
【结论】支链越多,沸点越低!
二、有机化合物的同分异构现象
①同分异构现象:化合物具有相同分子式,不同结构式的现象,叫做同分异构现象。
②同分异构体:具有同分异构现象的化合物之间,互称为同分异构体。
分子组成相同、分子量相同、分子式相同
分子中原子的排列顺序不同或结合方式不同(结构相似 , 但完全不同)
1、有机化合物种类繁多的主要原因:(1)碳原子可与其他原子形成4个共价键,碳原子之间也可相互形成单键、双键或三键,碳原子间还可以形成碳链或碳环;(2)有机化合物中广泛存在同分异构现象。
2、同分异构体不仅存在于有机化合物中,也存在于无机化合物中。甚至有机化合物与无机化合物之间也存在同分异构体,如无机物氰酸铵[NH4CNO]和有机物尿素[CO(NH2)2]。
1828年德国化学家维勒在实验室里给无机物氰酸铵加热制备了有机物尿素。这是人类历史上第一次利用无机物制备的有机物,从此打破了当时认为有机物只能从有机生物体中得到的传统错误观点。
我们如何判断化合物是否为同分异构体呢?
一、下列化合物中,属于同种物质的是_________,属于同分异构体的是______。
运用书写形式变换法:“拉”“转”、“翻”。
下列化合物中,属于同种物质的是_________, 属于同分异构体的是______。
用动画展示A分子的书写形式变换
用动画展示B分子的书写形式变换
用动画展示C分子和D分子的书写形式变换
二、下列物质与A为同种物质的是___________,与A互为同分异构体的是 ______。
下列物质与A为同种物质的是___________,与A互为同分异构体的是 ______。
1、下列各对物质属于同分异构体的是( )
③同分异构体:具有同分异构现象的化合物之间,互称为同分异构体。如正戊烷、异戊烷、新戊烷。
②同素异形体:由同种元素构成的不同单质。如金刚石和石墨、O2和O3、红磷和白磷等。
④同系物:结构相似,分子组成上相差一个或若干个CH2原子团的物质,互称为同系物。如甲烷和乙烷。
同位素所属对象是“原子”;同素异形体所属对象是“单质”;同分异构体和同系物所属对象均为“化合物”。
2、下列化合物中,互为同分异构体的是___________
A、CH3CH2CH2CH3
D、CH2 = CH CH = CH2
E、CH2 = CHCH2CH3
F、CH3 CH = CHCH3
碳原子可以与其他原子形成4个共价键;碳原子之间也可相互形成单键、双键或三键;碳原子间既可以形成较长的碳链,又可以形成碳环。
①书写形式变换法:拉、转、翻
②轴线变换法:画直线,通过平移或翻转判断
有机化合物同分异构体的判断方法:
同分异构体的判断方法不只这两种,其他方法在以后的课程中会陆续学习到。
人教版 (新课标)选修5 有机化学基础第二节 糖类教课课件ppt: 这是一份人教版 (新课标)选修5 有机化学基础第二节 糖类教课课件ppt,共30页。PPT课件主要包含了麦芽糖2分子葡萄糖,同分异构体,蔗糖与麦芽糖,物理性质,白色晶体,发芽的谷粒和麦芽,有甜味100,有甜味32,实验糖类的水解,无砖红色沉淀等内容,欢迎下载使用。
高中化学人教版 (新课标)选修5 有机化学基础第二节 醛课堂教学ppt课件: 这是一份高中化学人教版 (新课标)选修5 有机化学基础第二节 醛课堂教学ppt课件,共34页。PPT课件主要包含了实验3-6,化学性质,2与氢气加成,课堂练习等内容,欢迎下载使用。
人教版 (新课标)选修5 有机化学基础第二节 有机化合物的结构特点图文ppt课件: 这是一份人教版 (新课标)选修5 有机化学基础第二节 有机化合物的结构特点图文ppt课件,共31页。PPT课件主要包含了同分异构体的书写,②主链由长到短,③支链由整到散,④位置由心到边,CCCCC,等效碳不重排,CCCC,同分异构体的类型,CH3,CH2等内容,欢迎下载使用。













