





人教版 (新课标)选修5 有机化学基础第三章 烃的含氧衍生物第三节 羧酸 酯教案配套课件ppt
展开本节课的教学内容是羧酸。首先由课件展示几种自然界中的有机酸,如苹果酸、柠檬酸、草酸、蚁酸等导入新课,然后讲授羧酸的定义、通式、官能团、分类。羧酸的代表物—乙酸的物理性质、分子结构和化学性质。 对于乙酸的电离、乙酸与乙醇的酯化反应,课件中分别插入了动画。对于乙酸与乙醇生成乙酸乙酯的反应,课件中还插入了微课,微课视频操作清楚、现象明显,效果很好。
我们常常会吃到一些酸味较浓的食物,这些食物为什么有酸味?你能举例吗?
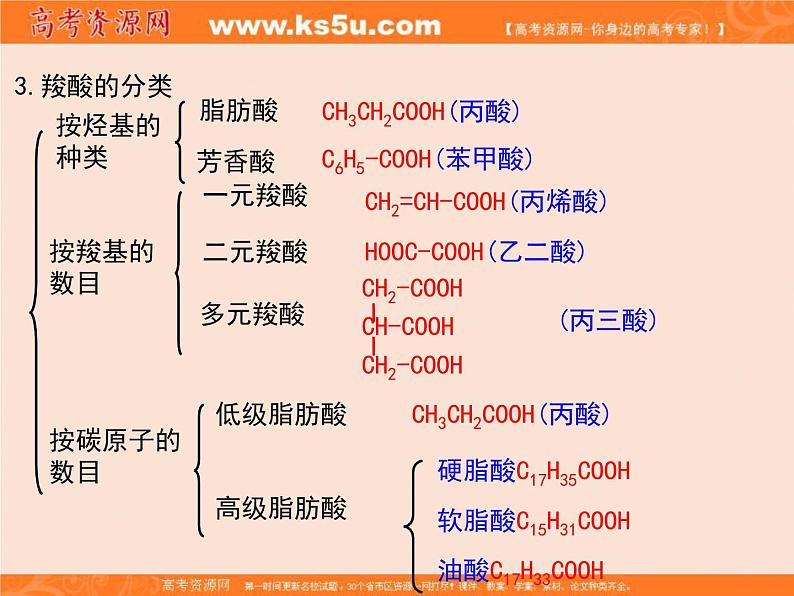
1.羧酸的定义: 羧酸是由烃基与羧基相连构成的有机化合物。
2.通式(饱和一元羧酸) :
CnH2nO2 或 CnH2n+1COOH (n≥1)或 R-COOH
CH3CH2COOH(丙酸)
C6H5-COOH(苯甲酸)
CH2=CH-COOH(丙烯酸)
HOOC-COOH(乙二酸)
硬脂酸C17H35COOH
软脂酸C15H31COOH
油酸C17H33COOH
油酸(C17H33COOH)
硬脂酸(C17H35COOH)
除乙酸外的其它酸:(1)甲酸:HCOOH(2)苯甲酸:C6H5-COOH(3)乙二酸:HOOC-COOH
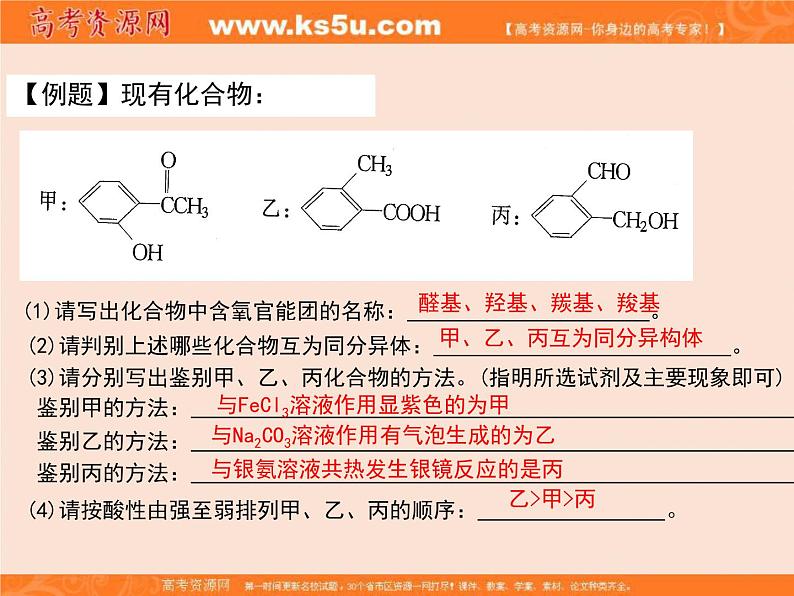
(1)请写出化合物中含氧官能团的名称: 。 (2)请判别上述哪些化合物互为同分异体: 。 (3)请分别写出鉴别甲、乙、丙化合物的方法。(指明所选试剂及主要现象即可) 鉴别甲的方法: ; 鉴别乙的方法: ; 鉴别丙的方法: . (4)请按酸性由强至弱排列甲、乙、丙的顺序: 。
醛基、羟基、羰基、羧基
甲、乙、丙互为同分异构体
与FeCl3溶液作用显紫色的为甲
与Na2CO3溶液作用有气泡生成的为乙
与银氨溶液共热发生银镜反应的是丙
与水、酒精以任意比互溶
熔点:16.6℃,易结成冰一样的晶体。(冰醋酸由此得名)沸点:117.9 ℃
二、羧酸代表物——乙酸
分析氢谱图写出乙酸的结构式。
H O | ‖ H — C — C — O — H | H
羧基:—C—OH(或—COOH)
写出乙酸各类结构表达式
【思考1】请同学们试说出几种可以检验醋酸具有酸性的方法。 ①使石蕊试液变红 ②与活泼金属置换出氢气 ③与碱发生中和反应 ④与碱性氧化物反应 ⑤能与部分盐(如碳酸盐)反应
(1)乙酸的酸的通性:
该动画为乙酸分子电离的动画。
1.利用下图所示仪器和药品,设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液的酸性强弱。
比较两种装置的优缺点、并写出反应的化学方程式。
2CH3COOH+Na2CO3 2CH3COONa+H2O+CO2 CH3COOH+NaHCO3 CH3COONa+H2O+CO2 CO2+H2O+C6H5ONa C6H5OH+NaHCO3
酸性:CH3COOH>H2CO3
除去挥发出来的乙酸蒸气
酸性:H2CO3>C6H5OH
乙酸 > 碳酸 > 苯酚
醇、酚、羧酸中羟基的比较
在一支试管中加入3mL乙醇,然后边摇动试管边慢慢加入2mL浓硫酸和2mL冰醋酸,加入碎瓷片,如图连好装置。用酒精灯小心均匀加热,产生的蒸气经导管通到饱和碳酸钠溶液的液面上。观察现象。
定义:含氧酸和醇起作用,生成酯和水的反应叫做酯化反应。
浓硫酸作用:催化剂、吸水剂
碎磁片的作用:防止暴沸
该微课为乙酸与乙醇反应生成乙酸乙酯的实验微课。
方式1:酸脱氢、醇脱羟基
方式2:酸脱羟基、醇脱氢
探究酯化反应可能的脱水方式
----同位素原子示踪法
酸脱羟基醇脱羟基上的氢原子。
CH3 C 18O C2H5 + H2O
C2H5OH + HNO3→C2H5ONO2 + H2O
注:无机含氧酸也可发生酯化反应(如 H2SO4、HNO3、H3PO4等)
1、药品混合顺序?浓硫酸的作用是:2、得到的反应产物是否纯净? 主要杂质有哪些?3、饱和Na2CO3溶液有什么作用?4、为什么导管不插入饱和Na2CO3溶液中?
不纯净;主要含乙酸、乙醇。
① 中和乙酸 ② 溶解乙醇。③ 降低酯在水中的溶解度,以便使酯分层析出。
防止受热不匀发生倒吸。
5、加热的目的:加快反应速率、及时将产物乙酸乙酯蒸出以利于可逆反应向生成乙酸乙酯的方向移动。(注意:加热时须小火均匀进行,这是为了减少乙醇的挥发,并防止副反应发生生成醚。) 6、试管要与桌面成45°角,且试管中的液体不能超过试管体积的三分之一。 7、导气管兼起冷凝和导气作用。导气管伸到饱和碳酸钠溶液液面上的目的:防止受热不均引起倒吸。
(乙酸乙酯的沸点为77℃)
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?请说明理由。
(1)由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯可提高其产率。
(2)使用过量的乙醇,可提高乙酸转化为乙酸乙酯的产率。
根据化学平衡原理,提高乙酸乙酯产率的措施有:
(3)使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。
重要化工原料,生产醋酸纤维、合成纤维、喷漆溶剂、香料、染料、医药、农药等。
5.乙烯氧化法制乙酸:
(1)酸性(2)酯化反应(3)油酸加成
1.若乙酸分子中的氧都是18O,乙醇分子中的氧都是16O,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )
A 1种 B 2种 C 3 种 D 4种
生成物中水的相对分子质量为 。
2.酯化反应属于( )A.中和反应 B.不可逆反应C.离子反应 D.取代反应
(1)乙酸的酸的通性
人教版 (2019)选择性必修3第四节 羧酸 羧酸衍生物公开课课件ppt: 这是一份人教版 (2019)选择性必修3<a href="/hx/tb_c4002471_t3/?tag_id=26" target="_blank">第四节 羧酸 羧酸衍生物公开课课件ppt</a>,共26页。PPT课件主要包含了羧酸衍生物,酯的组成结构,饱和一元酯通式,CnH2nO2,羧酸酯可表示为,酯的命名,HCOOCH2CH3,乙二酸乙二酯,乙二酸二乙酯,二乙酸乙二酯等内容,欢迎下载使用。
人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯课堂教学ppt课件: 这是一份人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯课堂教学ppt课件,共38页。PPT课件主要包含了学习目标,烃基不同,羧基数目,饱和一元羧酸通式,乙酸的酸性,CH3COOH,H2CO3,科学探究1,酯化反应,科学探究2等内容,欢迎下载使用。
人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯授课课件ppt: 这是一份人教版 (新课标)选修5 有机化学基础第三节 羧酸 酯授课课件ppt,共20页。PPT课件主要包含了CnH2nO2,COOH,RCOOH,苯甲酸,HOOCCOOH,乙二酸,丙烯酸,子结构,C2H4O2,CH3COOH等内容,欢迎下载使用。













